Clear Sky Science · ja
粗視化タンパク質折りたたみのための量子アニーリングの探究
将来の医薬にとってなぜ重要か
タンパク質が折りたたまれてできる形状は、酸素運搬からウイルスの認識まで、生体内での働きを決定します。これらの形状を予測することは創薬に不可欠ですが、すべてのタンパク質について正確に予測するのは依然として非常に難しい課題です。本稿は、新しい種類の計算ハードウェアである量子アニーラが、今日の人工知能や古典的スパコンが苦戦する特に手強い折りたたみ問題を将来解明する助けになり得るかを問いかけます。
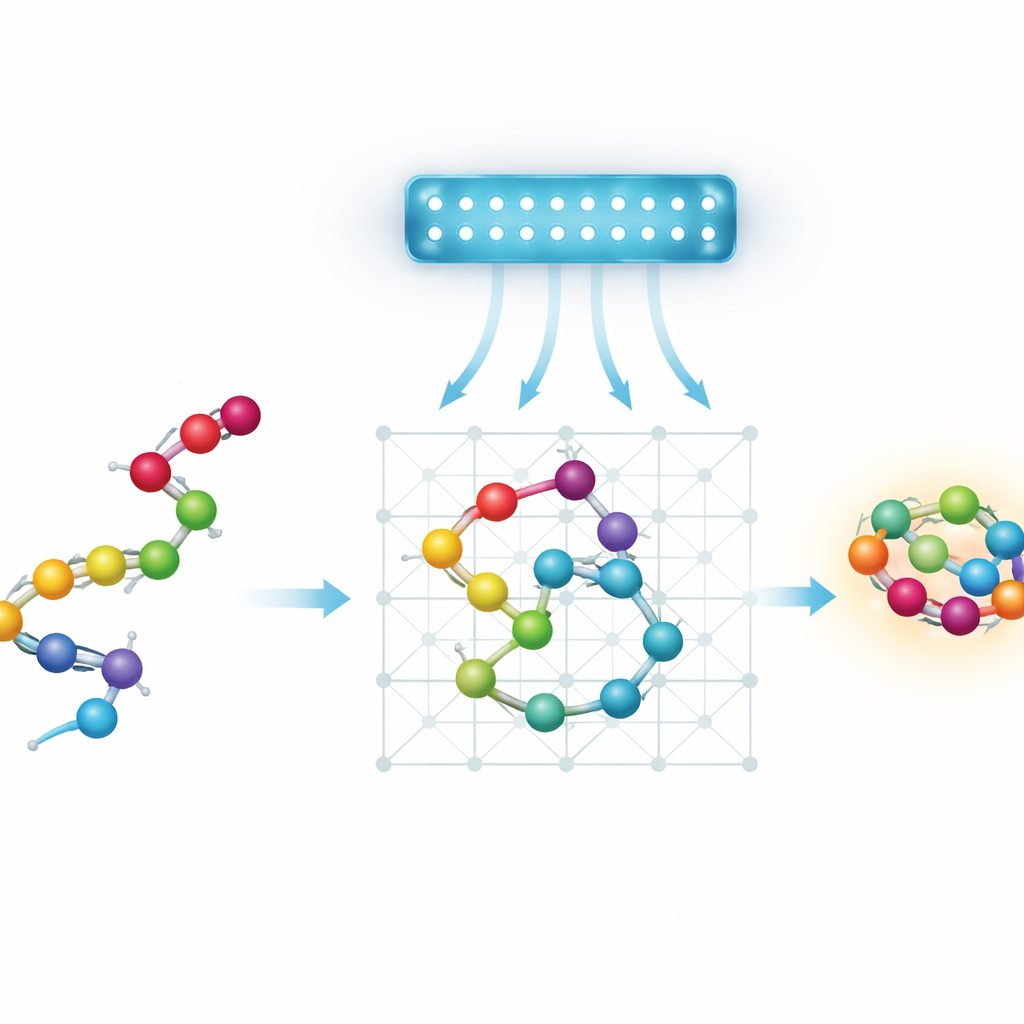
タンパク質、エネルギー景観、そして近道の探索
本質的に、タンパク質の折りたたみは巨大な探索問題です。アミノ酸の鎖は天文学的に多くの形に折りたたまれ得て、それぞれが固有のエネルギーを持ちます。自然は低エネルギーの形を好みますが、「エネルギー景観」は起伏が激しく、深い谷が急な丘で隔てられています。標準的な最適化手法や物理に基づくシミュレーションは局所的な谷に捕らわれて最良の形を見落とすことが多い。量子アニーリングが魅力的に見えるのは、理論的にはトンネリングのような量子効果が、一部の丘を常に乗り越える代わりにすり抜けることを可能にし、良好な折りたたみをより速く見つけられる可能性があるためです。
量子機械向けにタンパク質を単純化する
現在の量子アニーラは規模と接続性に制約があるため、著者らはタンパク質の簡略化、すなわち粗視化モデルで作業します。すべての原子を追跡する代わりに、各アミノ酸を離散格子上のビーズとして表現します。彼らはこの設定を量子アニーラが扱える数学的パズルとして符号化する4つの方法を検討します。二つの「ターンベース」モデルは格子上でチェーンが取るステップの列で鎖を記述します。二つの「座標ベース」モデルは各ビーズを特定の格子位置に割り当てます。各変種は標準的な立方格子か、各ビーズの隣接数が少ないより経済的な四面体格子のいずれかで配置できます。チームはさらに、相互作用を単純に保ちながら交互のビーズを表現するために2つの格子を交互に使う、新しい座標ベースの四面体格子スキームを導入します。
モデルの質と問題の難しさの検証
著者らはまず詳細な「資源監査」を行います:タンパク質長が増すにつれて各モデルが必要とする二値変数(量子ビット)の数、ペアワイズ結合の数、相互作用強度の幅がどれほどかを評価します。いくつかのターンベース符号化は急速に高密度になり、非常に高い数値精度を要求するようになり、これらは現行ハードウェアには不向きであると示します。以前に提案されたターンベースの四面体モデルはより深刻な欠陥を示します:約10残基より長い配列では、明らかに非物理的な自己交差する折りたたみを最低エネルギー解として正当と見なしてしまうことがあります。これに対して座標ベースのスキームは本質的にペアワイズ相互作用に限られ、より規則的なペナルティを用いるため、必要な数値精度が控えめでハードウェアへの写像がよりきれいになります。特に四面体格子上で顕著です。
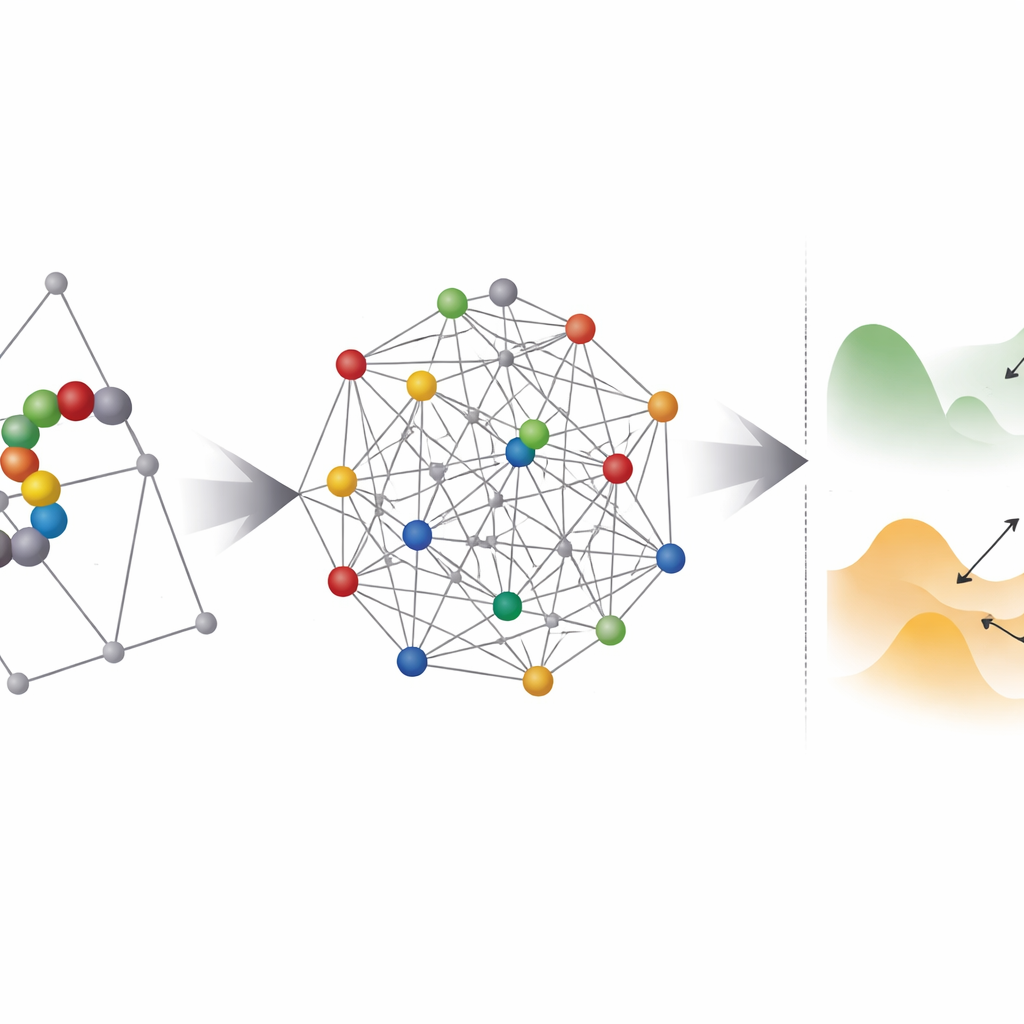
量子ハードウェアが助ける場所――そして苦戦する場所
次にチームは、これらの符号化された問題が任意の最適化器(量子でも古典でも)にとってどれほど「起伏が激しい」ように見えるかを調べます。彼らはパラレルテンパリングという手法を用いて低エネルギー状態の分布を探り、それらの間の障壁がどれほど厚いかを推定します。多くの座標ベースのインスタンスは、理論的には量子トンネリングが近傍の極小点間を越えるのに役立ち得る領域に入ります。しかし実際的な障害が立ちはだかります:現行の量子アニーラはすべての量子ビットを相互に接続できないため、各論理変数はエンベディングと呼ばれる過程で物理量子ビットの鎖に写像されなければなりません。これにより必要な量子ビット数が劇的に膨らみ、しばしば有効なエネルギー景観を粗くして解くのを難しくします。
量子ソルバと古典ソルバの対決
最後に、著者らは短くランダムに選んだアミノ酸鎖について真の最低エネルギー折りたたみを見つけるのに各手法がどれくらい時間を要するか比較します。彼らは高度に最適化されGPU対応のシミュレーテッドアニーリングコードを、商用の二世代の量子アニーラとベンチマークし、最も有望なモデルである四面体格子上の新しい座標ベース符号化に注目します。6〜9残基の小さなテストタンパク質では、両アプローチともサイズに対するスケーリングは類似しますが、絶対的な速度では古典コードが依然として元の問題上で何桁も速いです。しかし、両者に完全に同じ、既にエンベディング済みの問題を解かせた場合、量子アニーラは古典のシミュレーテッドアニーリングより良い性能を示し、エンベディングが主要なボトルネックでなくなれば潜在的なスケーリング上の優位性があることを示唆します。
今後の道筋が意味するもの
一般読者への要点は、量子アニーリングが現時点で現実的なタンパク質の折りたたみへの近道ではないものの、行き止まりでもないということです。研究はスパースな四面体格子上の座標ベースモデルを最も有望な方向性として特定し、モデル設計が結果として生じる問題の難易度を任意のソルバに対して大きく左右することを示しています。今日の量子ハードウェアは接続性と精度が不足しており、概念実証サイズを大きく超えるタンパク質を扱うには不十分であり、一部の既存の折りたたみモデルは基礎的な物理を誤って記述しています。それでも、量子デバイスがより良く接続された量子ビットや低い誤差率を備え、エンコーディングが非物理的な折りたたみを避けエンベディングのオーバーヘッドを減らすよう精練されれば、量子アニーリングは特に起伏の激しい折りたたみ問題に対して競争力を持ち、最終的には古典やAIベース手法を上回る可能性さえ出てくるでしょう。
引用: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
キーワード: 量子アニーリング, タンパク質の折りたたみ, 粗視化モデル, 最適化アルゴリズム, 量子計算ハードウェア