Clear Sky Science · sv
Utforska kvant-annealing för grovskalig proteinfällning
Varför detta är viktigt för framtida läkemedel
De former som proteiner viks till styr hur de fungerar i våra kroppar, från att bära syre till att känna igen virus. Att förutsäga dessa former är avgörande för läkemedelsdesign, men att göra det korrekt för alla proteiner är fortfarande extremt svårt. Den här artikeln ställer frågan om en ny sorts beräkningshårdvara—kvant-annealers—en dag skulle kunna hjälpa till att knäcka särskilt svåra proteinfällningsproblem som utmanar dagens artificiella intelligens och klassiska superdatorer.
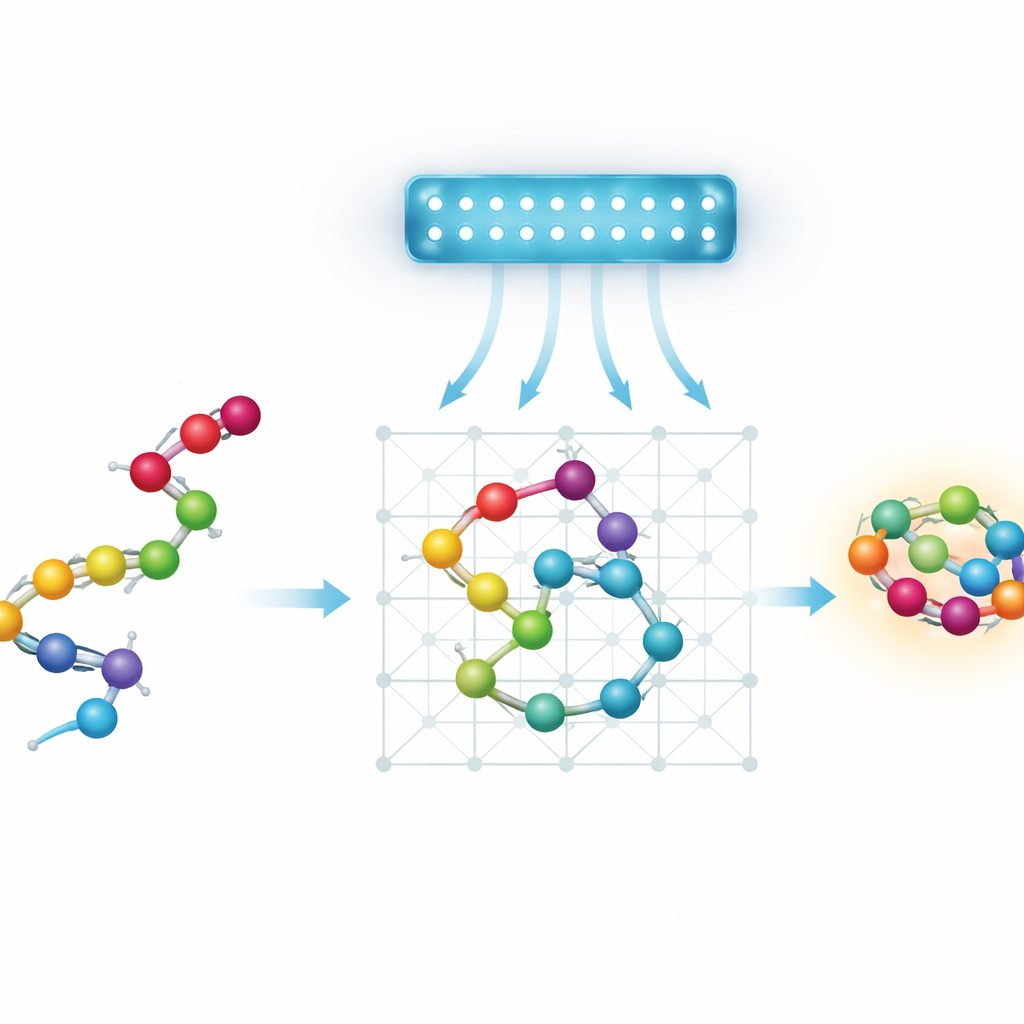
Proteiner, landskap och en jakt efter genvägar
I grunden är proteinveckning ett gigantiskt sökproblem. En kedja av aminosyror kan vika sig till astronomiskt många former, var och en med sin egen energi. Naturen tenderar att välja lågenergiformer, men "energ-landskapet" är ojämnt, fullt av djupa dalar separerade av branta kullar. Standardoptimeringsmetoder och fysikinspirerade simuleringar fastnar ofta i lokala dalar och missar den bästa formen. Kvant-annealing är lockande eftersom kvanteffekter i teorin, såsom tunnling, kan låta ett system smita igenom några av dessa kullar istället för att alltid klättra över dem, vilket potentiellt kan hitta bra vikningar snabbare.
Förenkling av proteiner för kvantmaskiner
Dagens kvant-annealers är begränsade i storlek och kopplingsmönster, så författarna arbetar med förenklade, eller grovskaliga, modeller av proteiner. Istället för att spåra varje atom representerar de varje aminosyra som en pärla på ett diskret rutnät. De undersöker fyra sätt att koda upp detta som ett matematiskt pussel som en kvant-annealer kan hantera. Två "vänder-baserade" modeller beskriver kedjan genom sekvensen av steg den tar på ett rutnät. Två "koordinatbaserade" modeller tilldelar varje pärla en specifik gitterposition. Varje variant kan placeras antingen på ett standard kubiskt rutnät eller ett mer ekonomiskt tetraedriskt rutnät, där varje pärla har färre grannar. Teamet introducerar också ett nytt koordinatbaserat schema på det tetraedriska gitteret, som använder två sammanflätade rutnät för att representera alternerande pärlor samtidigt som interaktionerna hålls enkla.
Testa modellkvalitet och problemhårdhet
Författarna utför först en detaljerad "resursrevision": hur många binära variabler (qubits), hur många parvisa kopplingar och hur brett spann av interaktionsstyrkor varje modell kräver när proteinet blir längre. De visar att vissa vända-baserade kodningar snabbt blir för täta och kräver mycket hög numerisk precision, båda dåliga matchningar för nuvarande hårdvara. En tidigare föreslagen vända-baserad tetraedrisk modell uppvisar ett djupare fel: för sekvenser längre än ungefär tio aminosyror kan den betrakta tydligt ofysikaliska självgenomträngande vikningar som legitima lägsta-energilösningar. I kontrast är de koordinatbaserade schemana naturligt begränsade till parvisa interaktioner och använder mer regelbundna strafftermer, vilket håller den nödvändiga numeriska precisionen modest och kartläggningen till hårdvaran renare, särskilt på det tetraedriska gitteret.
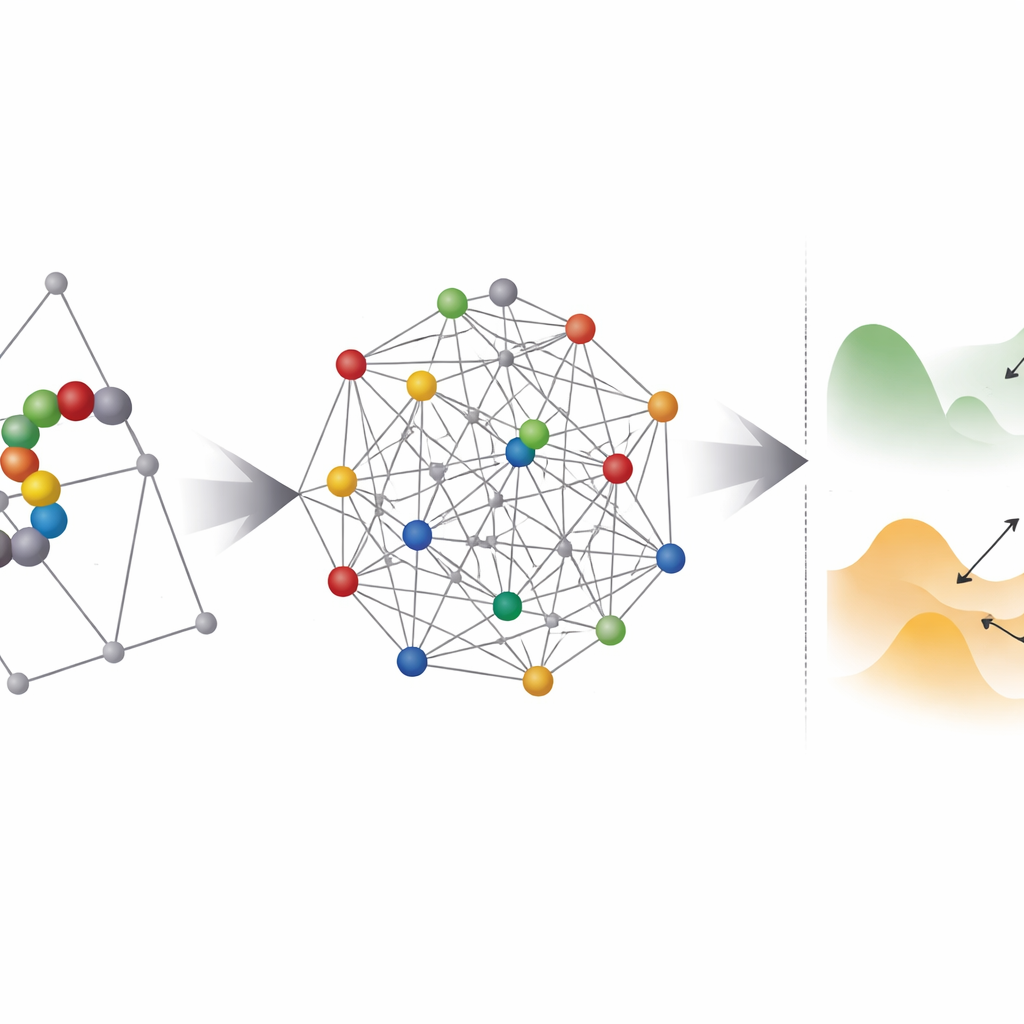
Var kvant-hårdvara hjälper — och var den kämpar
Därefter undersöker teamet hur "rugged" dessa kodade problem ter sig för vilken optimerare som helst, kvant eller klassisk. De använder en teknik kallad parallell temperering för att pröva fördelningen av lågenergistater och uppskatta hur tjocka barriärerna är mellan dem. De flesta av de koordinatbaserade instanserna hamnar i ett regime där kvanttunnling i princip skulle kunna hjälpa till att hoppa mellan närliggande minima. Dock tornar ett praktiskt hinder upp sig: befintliga kvant-annealers kan inte koppla varje qubit till varje annan, så varje logisk variabel måste mappas på en kedja av fysiska qubits i en process kallad embedding. Detta blåser upp antalet qubits dramatiskt och gör ofta det effektiva energilandskapet grövre och svårare att lösa.
Uppgörelse mellan kvant- och klassiska lösare
Slutligen jämför författarna hur lång tid olika metoder tar för att hitta den verkliga lägsta-energi-vikningen för korta, slumpmässigt valda aminosyrakedjor. De benchmarkar en kraftigt optimerad, GPU-accelererad simulering av annealing mot två generationer av kommersiella kvant-annealers, med fokus på den mest lovande modellen: den nya koordinatbaserade kodningen på det tetraedriska gitteret. För små testproteiner på sex till nio rester visar båda tillvägagångssätten liknande skalning med storlek, men i absoluta tal är den klassiska koden fortfarande mycket snabbare—med flera storleksordningar—när den körs på det ursprungliga problemet. Däremot, när båda metoderna får lösa exakt samma redan-embedade version av problemet, presterar kvant-annealern bättre än deras klassiska simulerade annealing, vilket antyder en potentiell skalningsfördel när embedding inte längre är den huvudsakliga flaskhalsen.
Vad detta betyder för vägen framåt
För en allmän läsare är slutsatsen att kvant-annealing ännu inte är en genväg till att vika realistiska proteiner, men det är inte heller en återvändsgränd. Studien identifierar koordinatbaserade modeller på glesa tetraedriska gitter som den mest lovande vägen framåt, och visar att modellutformning starkt påverkar hur svåra de resulterande problemen är för vilken lösare som helst. Dagens kvant-hårdvara saknar kopplingsmöjligheter och precision för att hantera proteiner långt utöver proof-of-concept-storlekar, och vissa befintliga veckningsmodeller missbeskriver till och med grundläggande fysik. Ändå, i takt med att kvantenheter får bättre kopplade qubits och lägre felnivåer, och när kodningar förfinas för att undvika ofysikaliska vikningar och minska embedding-överhead, skulle kvant-annealing kunna bli konkurrenskraftigt—och kanske så småningom överlägset—för särskilt knotiga proteinveckningsutmaningar som belastar klassiska och AI-baserade metoder.
Citering: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
Nyckelord: kvant-annealing, proteinveckning, grovskaliga modeller, optimeringsalgoritmer, kvantberäkningshårdvara