Clear Sky Science · fr
Exploration de l’optimisation quantique par recuit pour le repliement grossièrement modélisé des protéines
Pourquoi cela compte pour les médicaments de demain
Les formes que prennent les protéines déterminent leur fonction dans notre organisme, du transport de l’oxygène à la reconnaissance des virus. Prédire ces conformations est essentiel pour la conception de médicaments, mais y parvenir de façon fiable pour toutes les protéines reste extrêmement difficile. Cet article se demande si un nouveau type de matériel informatique — les recuiteurs quantiques — pourrait un jour aider à résoudre les problèmes de repliement de protéines particulièrement difficiles, ceux qui mettent à l’épreuve l’intelligence artificielle et les supercalculateurs classiques d’aujourd’hui.
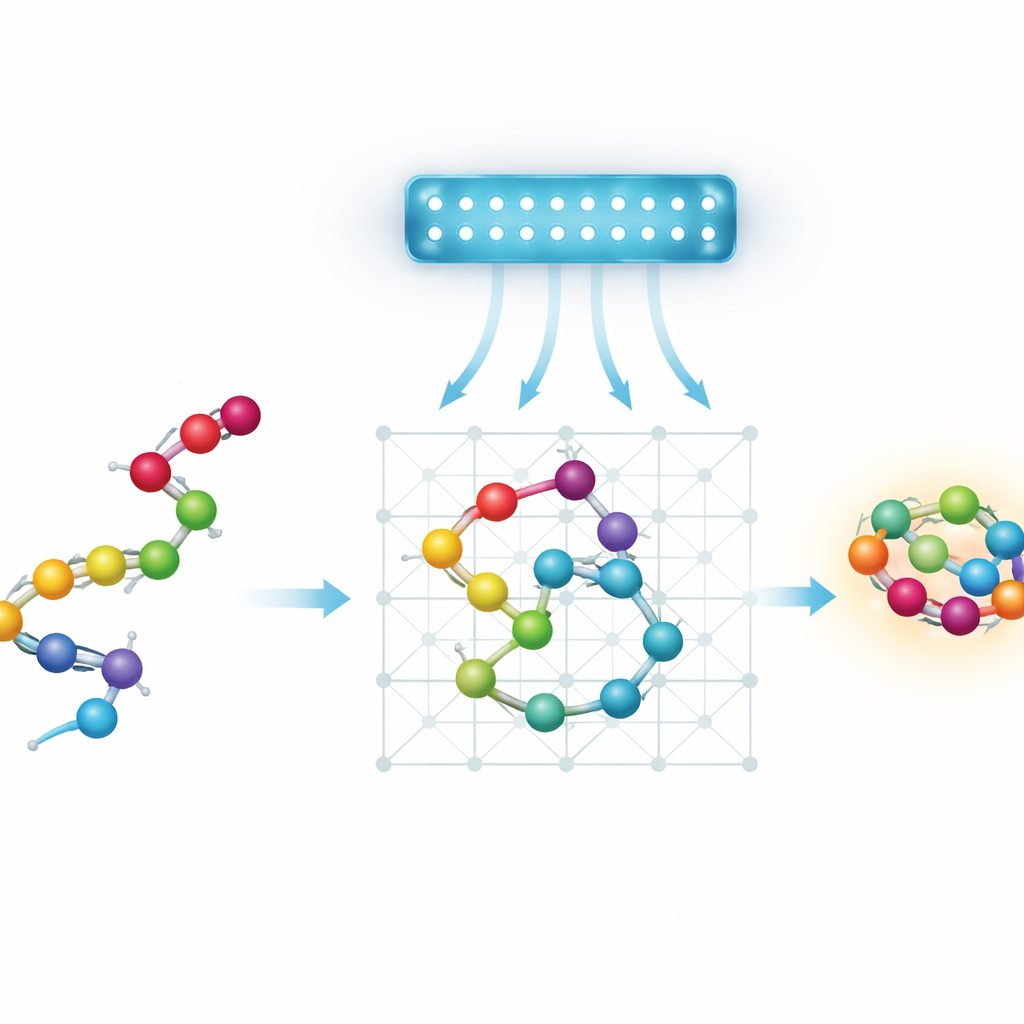
Protéines, paysages énergétiques et recherche de raccourcis
Au fond, le repliement des protéines est un gigantesque problème de recherche. Une chaîne d’acides aminés peut adopter un nombre astronomique de conformations, chacune avec son énergie propre. La nature tend à privilégier les conformations de faible énergie, mais le « paysage énergétique » est accidenté, plein de vallées profondes séparées par des collines abruptes. Les méthodes d’optimisation standard et les simulations inspirées de la physique se retrouvent souvent piégées dans des minima locaux et ratent la meilleure conformation. Le recuit quantique est attractif parce que, en théorie, des effets quantiques comme le tunneling pourraient permettre à un système de traverser certaines de ces barrières au lieu de toujours devoir les franchir, potentiellement en trouvant plus vite de bons repliements.
Simplifier les protéines pour les machines quantiques
Les recuiteurs quantiques actuels sont limités en taille et en connectivité, aussi les auteurs travaillent-ils avec des modèles simplifiés, ou grossièrement résolus, des protéines. Plutôt que de suivre chaque atome, ils représentent chaque acide aminé par une bille sur une grille discrète. Ils examinent quatre manières d’encoder ce dispositif en un casse-tête mathématique que peut traiter un recuiteur quantique. Deux modèles « basés sur les virages » décrivent la chaîne par la séquence des pas qu’elle effectue sur une grille. Deux modèles « basés sur les coordonnées » assignent à chaque bille une position de réseau précise. Chaque variante peut être disposée soit sur une grille cubique standard, soit sur une grille tétraédrique plus économe, où chaque bille a moins de voisins. L’équipe présente aussi un nouveau schéma basé sur les coordonnées sur le réseau tétraédrique, utilisant deux grilles entrelacées pour représenter les billes alternées tout en gardant les interactions simples.
Tester la qualité des modèles et la difficulté des problèmes
Les auteurs réalisent d’abord un « audit des ressources » détaillé : combien de variables binaires (qubits), combien d’accouplements par paires, et quelle amplitude d’intensités d’interaction chaque modèle requiert lorsque la longueur de la protéine augmente. Ils montrent que certains encodages basés sur les virages deviennent rapidement trop denses et exigent une très grande précision numérique, deux caractéristiques mal adaptées au matériel actuel. Un modèle tétraédrique basé sur les virages proposé auparavant présente un défaut plus profond : pour des séquences de plus d’environ dix acides aminés, il peut considérer comme solutions d’énergie minimale des conformations manifestement non physiques avec auto-intersections. En revanche, les schémas basés sur les coordonnées se limitent naturellement aux interactions par paires et utilisent des pénalités plus régulières, ce qui maintient la précision numérique requise modeste et facilite la traduction vers le matériel, en particulier sur la grille tétraédrique.
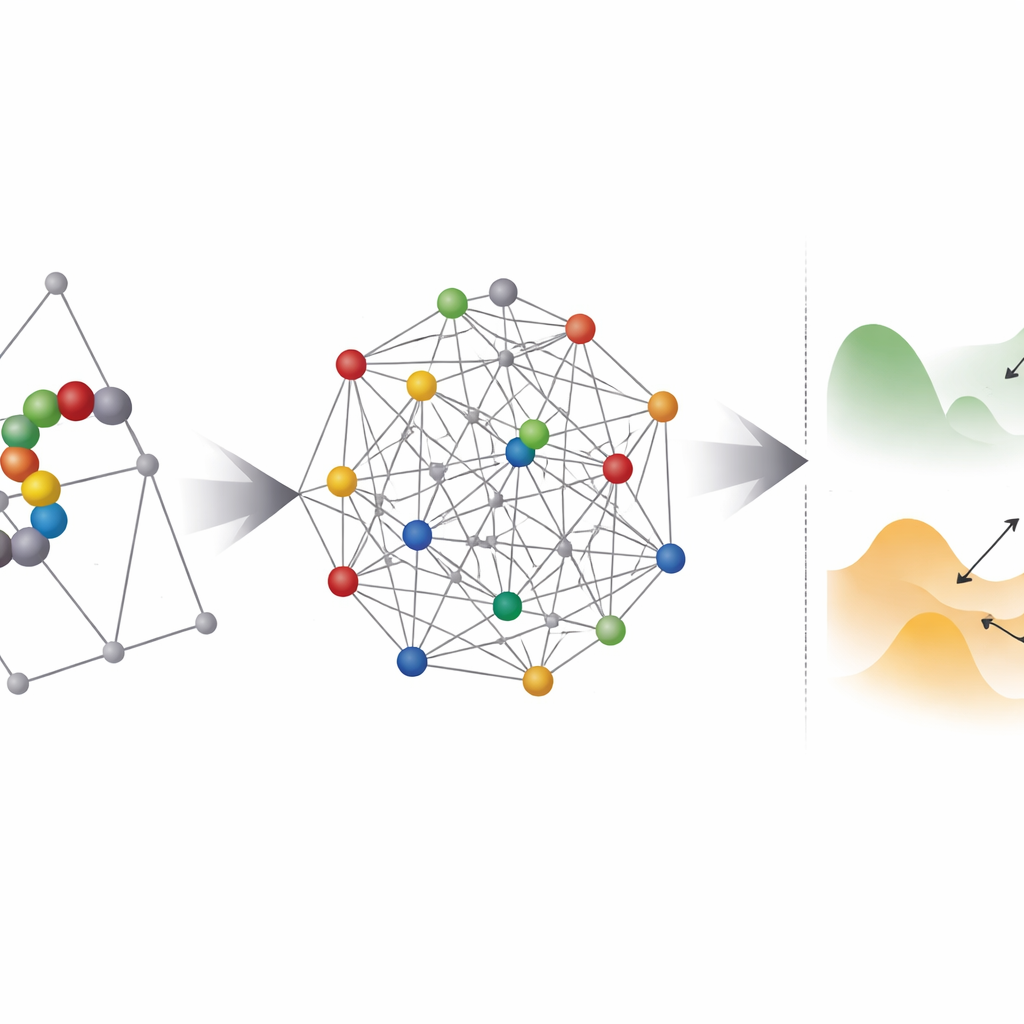
Où le matériel quantique aide — et où il bute
Ensuite, l’équipe étudie à quel point ces problèmes encodés apparaissent « accidentés » pour tout optimiseur, quantique ou classique. Ils utilisent une technique appelée température parallèle (parallel tempering) pour sonder la distribution des états de faible énergie et estimer l’épaisseur des barrières entre eux. La plupart des instances basées sur les coordonnées tombent dans un régime où le tunneling quantique pourrait, en principe, aider à sauter entre des minima voisins. Cependant, un obstacle pratique se profile : les recuiteurs quantiques existants ne peuvent pas connecter chaque qubit à tous les autres, de sorte que chaque variable logique doit être mappée sur une chaîne de qubits physiques dans un processus appelé embedding. Cela gonfle dramatiquement le nombre de qubits et rend souvent le paysage énergétique effectif plus rugueux et plus difficile à résoudre.
Affrontement entre solveurs quantiques et classiques
Enfin, les auteurs comparent le temps nécessaire à différentes méthodes pour trouver la vraie conformation d’énergie minimale pour des chaînes d’acides aminés courtes et choisies aléatoirement. Ils confrontent un code de recuit simulé très optimisé, accéléré par GPU, à deux générations de recuiteurs quantiques commerciaux, en se concentrant sur le modèle le plus prometteur : le nouvel encodage basé sur les coordonnées sur la grille tétraédrique. Pour de petites protéines tests de six à neuf résidus, les deux approches montrent une dépendance à la taille similaire, mais à échelle absolue le code classique reste beaucoup plus rapide — de plusieurs ordres de grandeur — lorsqu’il opère sur le problème original. Toutefois, lorsque les deux méthodes sont invitées à résoudre exactement la même version déjà embeddee du problème, le recuiteur quantique dépasse leur recuit simulé classique, suggérant un avantage d’échelle potentiel dès que l’embedding ne sera plus le goulot d’étranglement principal.
Ce que cela signifie pour la suite
Pour le lecteur général, la conclusion est que le recuit quantique n’est pas encore une solution rapide pour le repliement de protéines réalistes, mais ce n’est pas non plus une impasse. L’étude identifie les modèles basés sur les coordonnées sur des réseaux tétraédriques clairsemés comme la voie la plus prometteuse, et montre que la conception du modèle façonne fortement la difficulté des problèmes pour tout solveur. Le matériel quantique actuel manque de connectivité et de précision pour traiter des protéines bien au-delà de tailles démonstratives, et certains modèles de repliement existants décrivent même mal des aspects physiques fondamentaux. Néanmoins, à mesure que les dispositifs quantiques gagneront des qubits mieux connectés et des taux d’erreur plus faibles, et que les encodages seront raffinés pour éviter les repliements non physiques et réduire le surcoût d’embedding, le recuit quantique pourrait devenir compétitif — et peut-être un jour supérieur — pour les défis de repliement de protéines particulièrement accidentés qui mettent à rude épreuve les méthodes classiques et basées sur l’IA.
Citation: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
Mots-clés: recuit quantique, repliement des protéines, modèles grossièrement résolus, algorithmes d’optimisation, matériel informatique quantique