Clear Sky Science · he
חקר אנילינג קוונטי לקיפול חלבונים בקנה מידה גס
מדוע זה משמעותי עבור תרופות בעתיד
הצורות שאליהן חלבונים מתקפלים קובעות איך הם פועלים בגופנו, החל מנשיאת חמצן ועד זיהוי וירוסים. חיזוי הצורות הללו הוא קריטי לעיצוב תרופות, אך חיזוי מדויק לכל החלבונים נותר מאתגר ביותר. המאמר הזה שואל האם סוג חדש של חומרה — אנילרים קוונטיים — יכול יום אחד לעזור לפרוץ בעיות קיפול חלבונים קשות במיוחד שמציבות אתגר עבור בינה מלאכותית ומחשבים קלאסיים של היום.
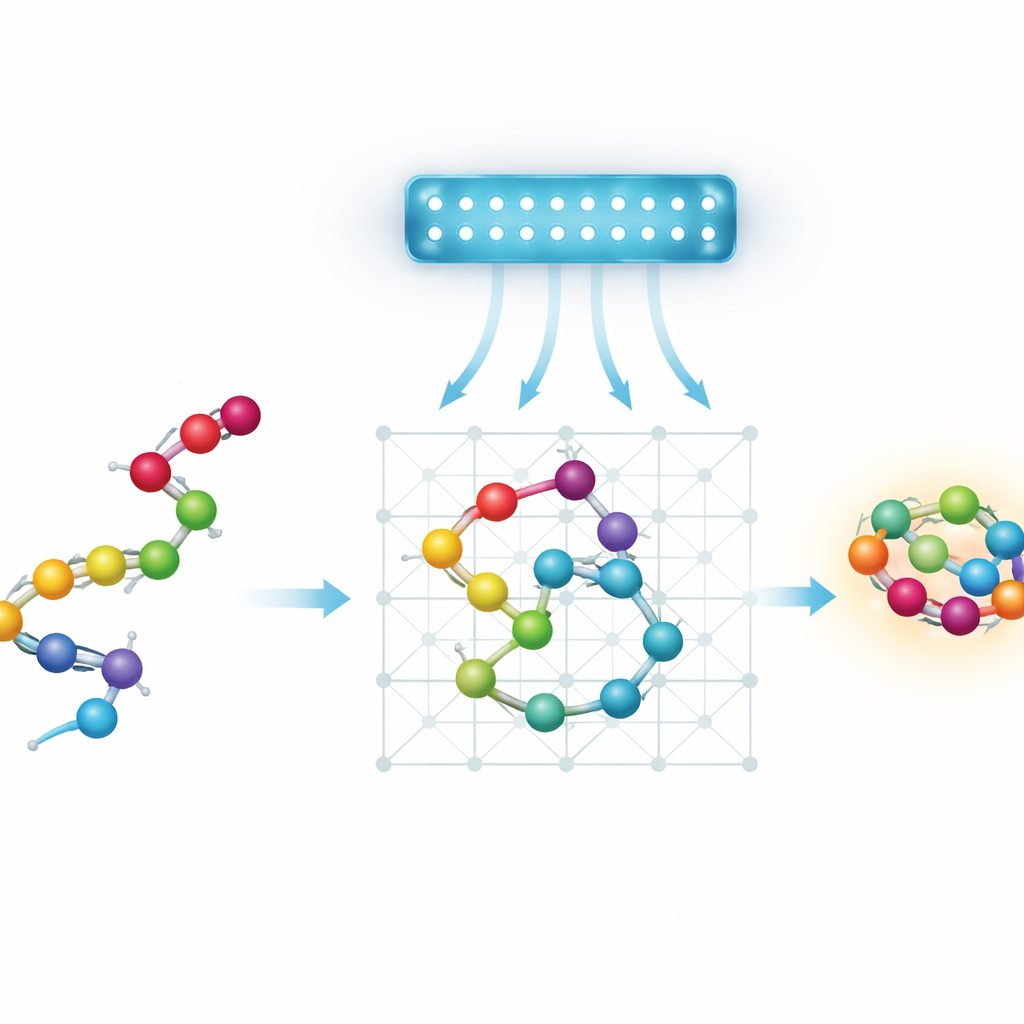
חלבונים, נופים וחיפוש לקיצורי דרך
בבסיסו, קיפול חלבונים הוא בעיית חיפוש ענקית. שרשרת חומצות אמינו יכולה להתקפל למספר אסטרונומי של צורות, שלכל אחת מהן אנרגיה משלה. הטבע נוטה לבחור צורות בעלות אנרגיה נמוכה, אך "נוף האנרגיה" מחוספס, מלא בעמקים עמוקים המופרדים על ידי גבעות תלולות. שיטות אופטימיזציה סטנדרטיות וסימולציות בהשראת פיזיקה לעתים נלכדות בעמקים מקומיים ומחמיצות את הצורה הטובה ביותר. אנילינג קוונטי מעניין כי, תאורטית, אפקטים קוונטיים כמו מנהור עשויים לאפשר למערכת להחליק דרך חלק מהגבעות הללו במקום תמיד לטפס עליהן, ובכך למצוא קיפולים טובים יותר במהירות גבוה יותר.
פישוט חלבונים עבור מכונות קוונטיות
האנילרים הקוונטיים הקיימים מוגבלים בגודל ובקישוריות, ולכן המחברים עובדים עם מודלים מפושטים, או בקנה מידה גס, של חלבונים. במקום לעקוב אחרי כל אטום, הם מייצגים כל חומצת אמינו כחרוז על גריד דיסקרטי. הם בוחנים ארבעה דרכים לקידוד ההגדרה הזו כחידה מתמטית שאנילר קוונטי יכול לטפל בה. שני מודלים "מבוססי פניות" מתארים את השרשרת לפי רצף הצעדים שהיא עושה על הגריד. שני מודלים "מבוססי קואורדינטות" מייחסים לכל חרוז מיקום ספציפי בסריג. כל גרסה יכולה להיות מוצגת או על גריד קובייתי סטנדרטי או על גריד טטרהדרלי חסכוני יותר, שבו לכל חרוז יש פחות שכנים. הצוות גם מציג סכימה חדשה מבוססת קואורדינטות על הגריד הטטרהדרלי, המשתמשת בשני גרידים משולבים לייצוג חרוזים חילופיים תוך שמירה על אינטראקציות פשוטות.
בדיקת איכות המודלים וקושי הבעיות
המחברים מבצעים תחילה "בדיקת משאבים" מפורטת: כמה משתנים בינאריים (קיווביטים), כמה קפלינגים זוגיים, ומה טווח עוצמות האינטראקציות שכל מודל דורש ככל שאורך החלבון גדל. הם מראים כי חלק מקידודים מבוססי-פניות הופכים במהירות לצפופים ודורשים דיוק מספרי מאוד גבוה, שני גורמים שאינם מתאימים לחומרה הנוכחית. מודל טטרהדרלי מבוסס-פניות שהוצע קודם מגלה ליקוי עמוק יותר: עבור רצפים ארוכים בכ־עשר חומצות אמינו ומעלה הוא עשוי להתייחס לקיפולים החותכים את עצמם — שאינם פיזיקליים — כפתרונות בעלי האנרגיה הנמוכה ביותר. לעומת זאת, הסכימות מבוססות הקואורדינטות מוגבלות מטבען לאינטראקציות זוגיות ומשתמשות בעונשים סדירים יותר, מה שמשאיר את דרישות הדיוק המספרי צנועות ואת המיפוי לחומרה נקי יותר, במיוחד על הגריד הטטרהדרלי.
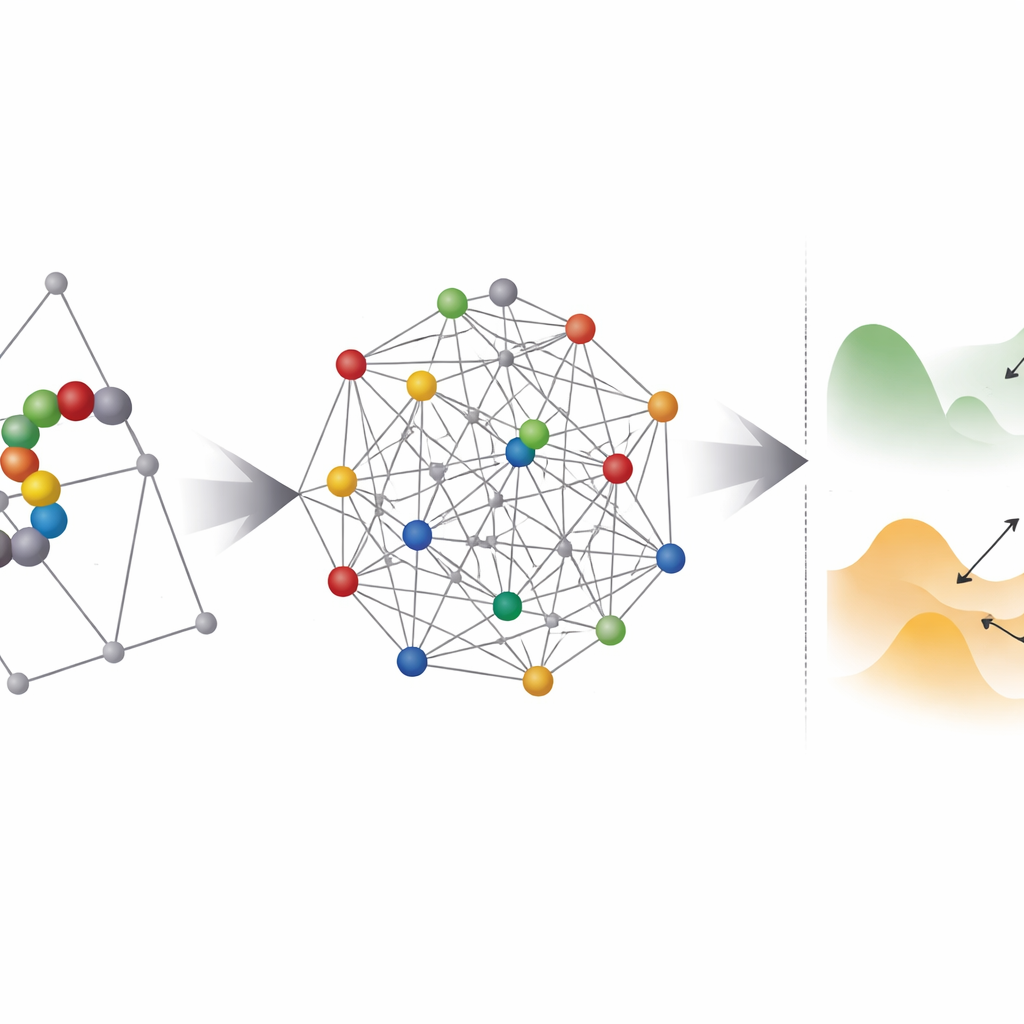
איפה החומרה הקוונטית עוזרת — ואיפה היא נתקעת
בהמשך, הצוות חוקר עד כמה הבעיות המקודדות הללו נראות "מחוספסות" עבור כל מאמצי אופטימיזציה, קוונטיים או קלאסיים. הם משתמשים בטכניקה הנקראת parallel tempering כדי לחקור את התפלגות המצבים בעלי האנרגיה הנמוכה ולהעריך כמה עבים המחסומים ביניהם. רוב המקרים מבוססי הקואורדינטות נופלים לתחום שבו מנהור קוונטי עשוי, בתיאוריה, לעזור לקפוץ בין מינימות סמוכות. עם זאת, מונח מעשי מונח לפניו: האנילרים הקוונטיים הקיימים אינם יכולים לקשר כל קיוubit עם כל אחד אחר, ולכן כל משתנה לוגי חייב להיות ממופה לשרשרת של קיווביטים פיזיים בתהליך הנקרא embedding. זה מנפח את מספר הקיווביטים בצורה דרמטית ולעתים מקרב את נוף האנרגיה האפקטיבי למחוספס יותר וקשה יותר לפתרון.
עימות בין פותרים קוונטיים וקלאסיים
לבסוף, המחברים משווים כמה זמן שיטות שונות זקוקות כדי למצוא את הקיפול האמיתי בעל האנרגיה הנמוכה ביותר עבור שרשראות חומצות אמינו קצרות, שנבחרו באקראי. הם בוחנים קוד סימולייטד אנילינג מאד-ממוטב ומואץ GPU אל מול שתי דורות של אנילרים קוונטיים מסחריים, מתוך התמקדות במודל המבטיח ביותר: הקידוד החדש מבוסס הקואורדינטות על הגריד הטטרהדרלי. עבור חלבונים קטנים של שישה עד תשעה שיירים, שתי הגישות מראות התאמה בסקלינג ביחס לגודל, אך בסקאלה אבסולוטית הקוד הקלאסי מהיר בהרבה — בהפרשים של מספר סדרי גודל — כאשר הוא רץ על הבעיה המקורית. עם זאת, כאשר שתי השיטות מתבקשות לפתור בדיוק את אותו גרסה של הבעיה שכבר מוטמעת (embedded), האנילר הקוונטי מתנהג טוב יותר מהסימולייטד אנילינג הקלאסי שלהם, מרמז על יתרון בקנה מידה פוטנציאלי ברגע שה-embedding לא יהיה המכשול הראשי.
מה זה אומר עבור העתיד
לקורא כללי, המסקנה היא שאנילינג קוונטי עדיין אינו קיצור דרך לקיפול חלבונים ריאליסטיים, אבל הוא גם לא סיפור סגור. המחקר מזהה מודלים מבוססי קואורדינטות על גרידים טטרהדרליים צפופים־דלים כנתיב המבטיח ביותר להמשך, ומראה שעיצוב המודל מעצב במידה רבה עד כמה הבעיות שנוצרות קשות עבור כל פותר. החומרה הקוונטית של היום חסרה בקישוריות ובדיוק כדי להתמודד עם חלבונים שמעבר לגודל הוכחה־עיקרית, וחלק מהמודלים הקיימים אפילו מתארים באופן שגוי פיזיקה בסיסית. עם זאת, ככל שהמכשירים הקוונטיים יוסיפו קיווביטים עם קישוריות טובה יותר ושיעורי שגיאה נמוכים יותר, וככל שהקידודים יעודנו כדי למנוע קיפולים לא פיזיקליים ולהקטין את עלות ה-embedding, אנילינג קוונטי יכול להפוך לתחרותי — ואולי בסופו של דבר עדיף — באתגרי קיפול חלבונים מחוספסים במיוחד שמעמיסים על שיטות קלאסיות ובסיסיות בינה מלאכותית.
ציטוט: Scheiber, T., Heller, M. & Giebel, A. Exploring quantum annealing for coarse-grained protein folding. Sci Rep 16, 12035 (2026). https://doi.org/10.1038/s41598-026-46916-w
מילות מפתח: אנילינג קוונטי, קיפול חלבונים, מודלים בקנה מידה גס, אלגוריתמי אופטימיזציה, חומרת מחשוב קוונטית