Clear Sky Science · tr
Akciğer mTOR aktivasyonu, belirli akciğer hücrelerinin senesansı yoluyla akciğer fibrozisine veya amfizeme yol açar
Neden yaşlanan akciğerler hepimizi ilgilendirir
Yaşlandıkça akciğerlerimiz yavaşça değişir ve bizi amfizem ve fibroz gibi solunum sorunlarına karşı daha savunmasız hale getirir. Bu durumlar, akciğerin hava keseciklerini ve destekleyici dokusunu zedeler; bunun sonucunda insanlar nefes darlığı ve çabuk yorulma yaşar. Bu makalenin temelindeki çalışma basit ama önemli bir soruyu soruyor: bu farklı hasar desenlerine neden olan belirli akciğer hücreleri içinde neler ters gidiyor ve bu hasarlı hücreleri ortadan kaldırmak akciğerin iyileşmesine yardımcı olabilir mi?
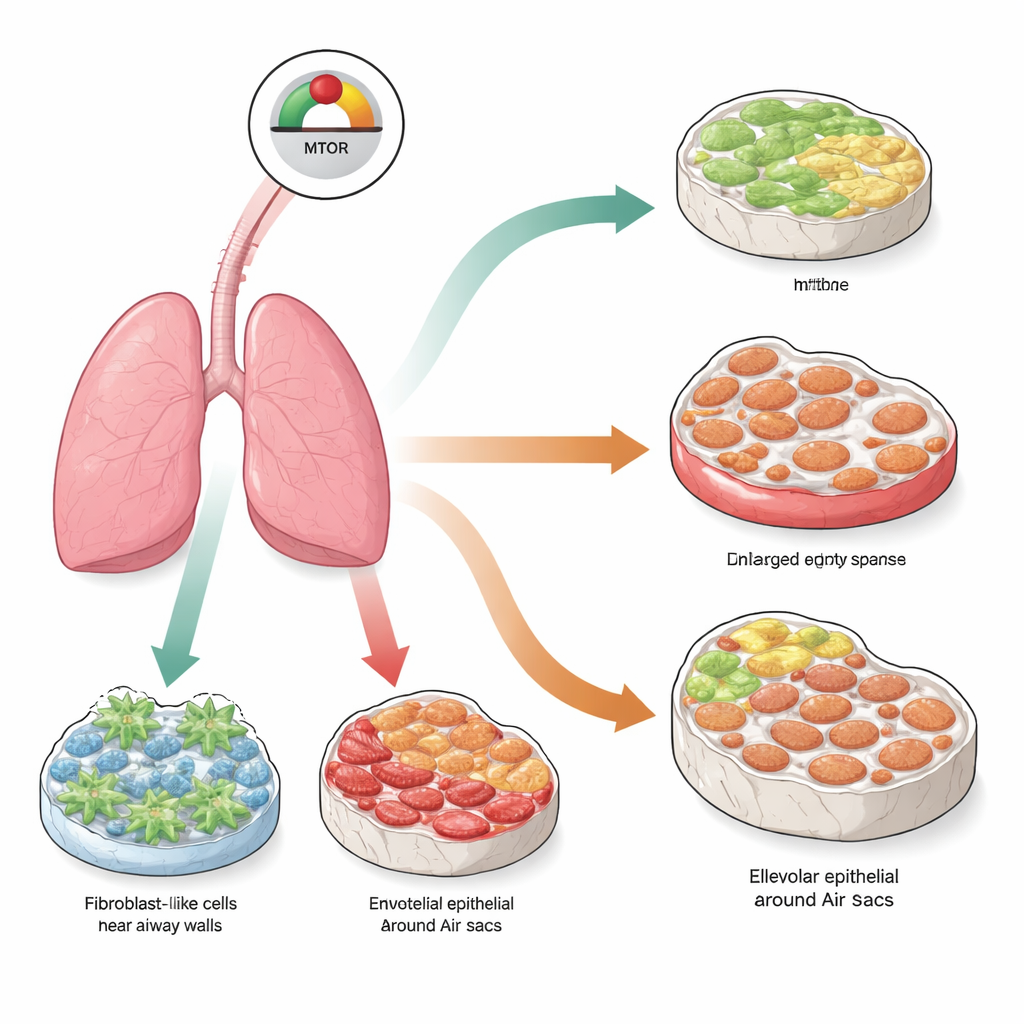
Akciğer hücrelerinde merkezi bir büyüme anahtarı
Bu çalışmanın merkezinde, hücrelerin besinleri algılamasına ve büyüyüp bölünüp bölünmeme kararını vermesine yardımcı olan mTOR adlı moleküler bir kontrol merkezi bulunuyor. Normal dokuda mTOR aktivitesi dikkatle dengelenir. Uzun süre aşırı zorlanırsa, hücreler kalıcı olarak bölünmeyi bıraktıkları ve inflamatuar ile doku yeniden şekillendirici moleküller karışımı salmaya başladıkları bir durum olan senesansa girebilir. Araştırmacılar, mTOR’u farklı akciğer hücre tiplerinde kalıcı aşırı aktive etmenin bu hücreleri senesansa itip itmeyeceğini ve bunun da sıra dışı akciğer hastalıkları oluşturup oluşturmayacağını sordular—yaşlı insanlarda görülenlere benzer biçimde.
Üç hücre tipi, üç akciğer hasarı deseni
Genetik olarak tasarlanmış fareleri kullanarak ekip, mTOR üzerindeki doğal bir fren olan TSC1'i akciğerin üç ana hücre popülasyonunda seçici olarak kaldırdı: destek matriksi üreten fibroblastlar, kan damarlarını döşeyen endotel hücreleri ve hava keseciklerinin yüzeyini oluşturan alveolar epitel hücreleri. Bu hedefli değişiklikten üç ay sonra, üç modelde de güçlü senesans belirtileri ve mTOR yolunun aktivasyonu görüldü. Ancak hangi hücrelerin etkilendiğine bağlı olarak gözlenen akciğer hasarı çarpıcı biçimde farklıydı. mTOR fibroblastlarda aşırı aktif hale geldiğinde akciğerlerde yoğun skarlaşma yani fibroz gelişti; kalın, kollajen zengini duvarlar oluştu. Aynı sinyal endotel hücrelerinde açıldığında ise akciğerler daha çok genişlemiş, parçalanmış hava boşluklarıyla karakterize edilen amfizem geliştirdi ve çok az skar oldu. Alveolar yüzey hücrelerinde mTOR’un açılması ise karışık bir tablo verdi: hem amfizeme benzer yıkım hem de fibrotik kalınlaşma görülerek insanlarda ‘‘kombine pulmoner fibroz ve amfizem’’ olarak bilinen duruma benzerlik gösterdi.
Hasarlı hücrelerin temizlenmesiyle akciğerin kurtarılması
Araştırmacılar daha sonra bu senesans hücrelerini ortadan kaldırmanın hasarı tersine çevirip çeviremeyeceğini test ettiler. Farelere seçici olarak senesans hücrelerin ölümünü tetiklemek üzere tasarlanmış ABT-263 adlı ilaç verildi. Genetik olarak değiştirilmiş üç fare türünün tamamında ABT-263, senesans belirteçlerini azalttı ve mTOR yolundan gelen sinyalleri düşürdü. Bu hücresel temizlik, akciğer yapısında ölçülebilir iyileşmelerle paralel ilerledi. Fibroblast hedefli farelerde skar azaldı, endotel hedefli farelerde amfizem hafifledi ve alveolar yüzey hücreleri değiştirilen farelerde hem skar hem de yıkım iyileşti ama tamamen düzelmedi. Bu sonuçlar, nispeten genç erişkin akciğerlerinde mTOR aşırıaktivitesinin tetiklediği senesans hücrelerinin yapısal hasarın başlıca aktörleri olduğunu ve bunların çıkarılmasının daha sağlıklı hücrelerin dokuyu onarmasına izin verebileceğini gösteriyor.
Doğal yaşlanan akciğerlerde neler olur
Ekip ayrıca normal fareleri bir aydan 20 aya kadar, yani yaşamın erken döneminden yaşlılığa kadar izledi. İlerleyen yaşla birlikte akciğerlerde giderek daha fazla kollajen birikti, daha büyük hava boşlukları gelişti ve senesans belirteçleri ile mTOR sinyallemesi yükseldi. Yaşlı farelere aynı senolitik ilaç verildiğinde hücresel yaşlanma ve mTOR aktivitesi belirteçleri düştü ve skarda ılımlı bir azalma görüldü. Ancak yapısal iyileşmeler genetik olarak değiştirilmiş farelerdekinin çok daha altında kaldı ve amfizem belirgin şekilde düzelmedi. Bu, tamamen yaşlanmış akciğerlerde hasarın daha derinleşmiş ve tersine çevrilmesinin daha zor hale gelmiş olduğunu; bunun nedeni olarak birçok farklı hücre tipinin zaten etkilenmiş olması veya onarım sistemlerinin kendilerinin yıpranmış olması gösterilebilir.
Gelecekteki akciğer sağlığı için ne anlama geliyor
Bir arada ele alındığında çalışma, tek bir büyüme-kontrol anahtarı olan mTOR’un farklı akciğer hücrelerinde çok yüksek düzeye çıkarılmasının çok farklı hastalık desenlerine yol açabileceğini gösteriyor: skarlaşma, hava boşluğu yıkımı veya her ikisinin karışımı. Ayrıca bu zararlı etkilerin senesans hücrelerin birikimiyle yakından ilişkili olduğunu ve bu hücrelerin temizlenmesinin genç erişkin hayvanlarda akciğer yapısını önemli ölçüde—fakat tamamen değil—geri kazandırabileceğini ortaya koyuyor. Yaşlanan akciğerlerde aynı strateji hücresel sinyalleri iyileştiriyor ama doku üzerinde yalnızca sınırlı yeniden şekillenme sağlıyor; bu da erken müdahalenin kritik olabileceğini düşündürüyor. Kronik akciğer hastalıkları riski taşıyan kişiler için bu çalışma, mTOR ve hücresel senesansı merkezi, birbirine bağlı hedefler olarak öne çıkarıyor ve mTOR’u yavaşlatmaya yönelik yaklaşımlar ile senesans hücreleri temizlemeyi birleştiren tedavi stratejilerinin bir gün yaşlılıkta akciğer fonksiyonunu korumaya yardımcı olabileceği olasılığını gündeme getiriyor.
Atıf: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Anahtar kelimeler: akciğer yaşlanması, hücresel senesans, mTOR yolu, pulmoner fibroz, amfizem