Clear Sky Science · pl
Aktywacja mTOR w płucach prowadzi do zwłóknienia lub rozedmy przez starzenie się określonych komórek płuc
Dlaczego starzenie się płuc ma znaczenie dla nas wszystkich
W miarę jak się starzejemy, nasze płuca stopniowo się zmieniają, co zwiększa podatność na problemy z oddychaniem, takie jak rozedma i zwłóknienie. Te schorzenia uszkadzają pęcherzyki płucne i tkankę podporową, powodując duszność i łatwe przemęczenie. Badanie opisane w tym artykule stawia proste, lecz istotne pytanie: co dzieje się w określonych komórkach płuc, co prowadzi do tak różnych wzorców uszkodzeń, i czy usunięcie tych uszkodzonych komórek może pomóc płucom się zregenerować?
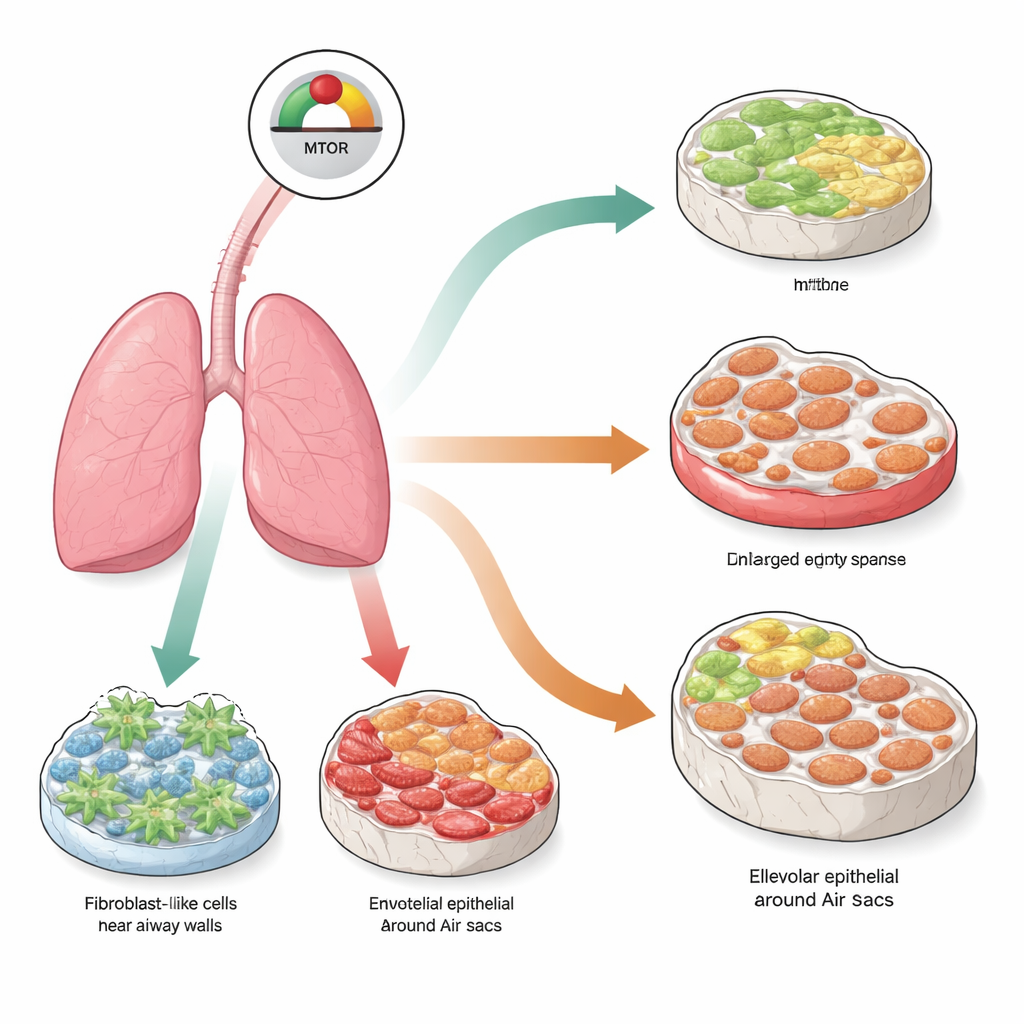
Centralny przełącznik wzrostu w komórkach płuc
W centrum tej pracy znajduje się molekularny węzeł kontrolny zwany mTOR, który pomaga komórkom wyczuwać dostępność składników odżywczych i decydować, czy rosnąć, dzielić się, czy pozostawać w stanie spoczynku. W normalnej tkance aktywność mTOR jest starannie wyważona. Gdy jest nadmiernie pobudzana przez długi czas, komórki mogą wejść w stan zwany senescencją, w którym trwale przestają się dzielić i zaczynają wydzielać mieszaninę molekuł zapalnych i przebudowujących tkankę. Naukowcy zapytali, czy trwałe przestawienie mTOR na nadmierną aktywność w różnych typach komórek płucnych pchnie te komórki w kierunku senescencji i w konsekwencji wywoła różne formy choroby płuc przypominające te obserwowane u osób starszych.
Trzy typy komórek, trzy wzorce uszkodzeń płuc
Używając genetycznie zmodyfikowanych myszy, zespół selektywnie usunął naturalny hamulec mTOR, zwany TSC1, w trzech głównych populacjach komórek płucnych: fibroblastach produkujących macierz podporową, komórkach śródbłonka wyściełających naczynia krwionośne oraz komórkach nabłonka pęcherzykowego tworzących powierzchnię pęcherzyków. Trzy miesiące po tej ukierunkowanej zmianie wszystkie trzy modele wykazywały silne cechy senescencji i aktywację szlaku mTOR. Jednak widoczne uszkodzenia płuc różniły się uderzająco w zależności od tego, które komórki były dotknięte. Gdy mTOR był nadaktywowany we fibroblastach, płuca rozwijały ciężkie bliznowacenie, czyli zwłóknienie, z grubymi, bogatymi w kolagen ścianami. Gdy ten sam sygnał był włączony w komórkach śródbłonka, zamiast tego rozwijała się rozedma — powiększone, uszkodzone przestrzenie powietrzne przy niewielkim bliznowaceniu. Włączenie mTOR w komórkach powierzchni pęcherzyków dało zmieszany obraz: zarówno zniszczenie przypominające rozedmę, jak i pogrubienie związane ze zwłóknieniem, naśladując stan u ludzi znany jako połączone zwłóknienie i rozedma płuc (combined pulmonary fibrosis and emphysema).
Usuwanie uszkodzonych komórek w celu naprawy płuc
Następnie badacze sprawdzili, czy pozbycie się tych senescentnych komórek może odwrócić szkody. Leczyli myszy lekiem ABT-263, zaprojektowanym do selektywnego wywoływania śmierci komórek senescentnych. We wszystkich trzech modyfikowanych genetycznie liniach myszy ABT-263 obniżył markery senescencji i zmniejszył sygnały ze szlaku mTOR. To oczyszczenie komórkowe szło w parze z mierzalnymi poprawami struktury płuc. Bliznowacenie zmalało u myszy z modyfikowanymi fibroblastami, rozedma zmniejszyła się u myszy z modyfikowanymi komórkami śródbłonka, a zarówno bliznowacenie, jak i zniszczenie poprawiły się, choć nie całkowicie, u myszy z zmienionymi komórkami powierzchni pęcherzyków. Wyniki te sugerują, że przynajmniej w stosunkowo młodych dorosłych płucach komórki senescentne napędzane nadaktywnością mTOR są głównymi sprawcami uszkodzeń strukturalnych i że ich usunięcie może umożliwić zdrowszym komórkom naprawę tkanki.
Co dzieje się w naturalnie starzejących się płucach
Zespół badał także normalne myszy w miarę jak starzały się od jednego do 20 miesięcy, co w przybliżeniu obejmuje okres od wczesnego życia do starości. Wraz z wiekiem płuca stopniowo gromadziły więcej kolagenu, rozwijały większe przestrzenie powietrzne i wykazywały wyższe poziomy markerów senescencji oraz silniejszą aktywność mTOR. Gdy starsze myszy leczono tym samym lekiem senolitycznym, markery starzenia komórek i aktywność mTOR spadły, a bliznowacenie zmniejszyło się w niewielkim stopniu. Jednak poprawy strukturalne były znacznie mniej spektakularne niż w modelach genetycznych, a rozedma nie poprawiła się wyraźnie. Sugeruje to, że w całkowicie zestarzałych płucach uszkodzenia stały się głębiej zakorzenione i trudniejsze do odwrócenia, być może dlatego, że wiele różnych typów komórek jest już dotkniętych lub same mechanizmy naprawcze zużyły się.
Co to oznacza dla przyszłego zdrowia płuc
Podsumowując, badanie pokazuje, że nadmierne włączenie jednego przełącznika kontroli wzrostu, mTOR, w różnych komórkach płucnych może prowadzić do bardzo odmiennych wzorców chorobowych: bliznowacenia, zniszczenia przestrzeni powietrznych lub mieszanki obu. Pokazuje też, że te szkodliwe efekty ściśle wiążą się z nagromadzeniem komórek senescentnych i że ich usuwanie może w znacznym stopniu, choć nie całkowicie, przywrócić strukturę płuc u młodszych dorosłych zwierząt. W starzejących się płucach ta sama strategia poprawia sygnały komórkowe, ale tylko nieznacznie zmienia tkankę, co sugeruje, że wczesna interwencja może być kluczowa. Dla osób zagrożonych przewlekłymi chorobami płuc praca ta podkreśla mTOR i senescencję komórkową jako centralne, powiązane cele oraz stwarza możliwość, że terapie łączone mające spowolnić mTOR i usuwać komórki senescentne mogą pewnego dnia pomóc zachować sprawność płuc w starości.
Cytowanie: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Słowa kluczowe: starzenie się płuc, senescencja komórkowa, szlak mTOR, zwłóknienie płuc, rozedma