Clear Sky Science · de
Lungen‑mTOR‑Aktivierung führt über Seneszenz spezifischer Lungenzellen zu Lungenfibrose oder Emphysem
Warum alternde Lungen uns alle betreffen
Mit zunehmendem Alter verändern sich unsere Lungen schrittweise, wodurch wir anfälliger für Atembeschwerden wie Emphysem und Fibrose werden. Diese Erkrankungen schädigen die Lungenbläschen und das stützende Gewebe, sodass Betroffene kurzatmig sind und leicht ermüden. Die Studie hinter diesem Artikel stellt eine einfache, aber wichtige Frage: Was läuft in bestimmten Lungenzellen schief, sodass so unterschiedliche Schadensmuster entstehen, und kann das Entfernen dieser geschädigten Zellen der Lunge helfen, sich zu erholen?
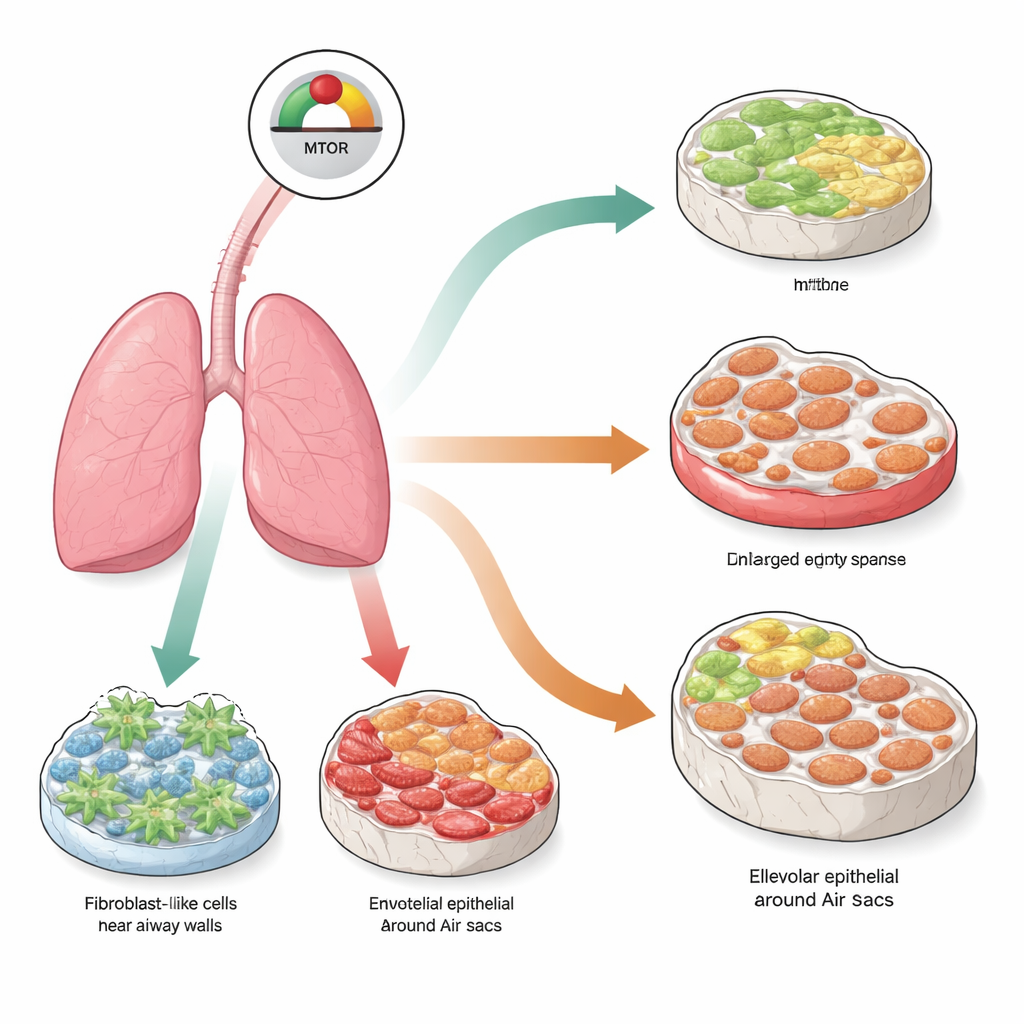
Ein zentraler Wachstums‑Schalter in Lungenzellen
Im Mittelpunkt dieser Arbeit steht eine molekulare Steuerzentrale namens mTOR, die Zellen hilft, Nährstoffe zu erkennen und zu entscheiden, ob sie wachsen, sich teilen oder ruhig bleiben. Im normalen Gewebe ist die mTOR‑Aktivität sorgfältig ausbalanciert. Wird sie zu lange zu stark angeregt, können Zellen in einen Zustand namens Seneszenz eintreten, in dem sie dauerhaft die Teilung einstellen und ein Gemisch aus entzündungsfördernden und geweberemodellierenden Molekülen ausschütten. Die Forschenden fragten, ob das dauerhafte Hochfahren von mTOR in verschiedenen Zelltypen der Lunge diese Zellen in Seneszenz treiben und dadurch unterschiedliche Formen von Lungenerkrankungen hervorrufen würde, die dem ähneln, was bei älteren Menschen beobachtet wird.
Drei Zelltypen, drei Muster des Lungenschadens
Mithilfe genetisch veränderter Mäuse entfernte das Team selektiv eine natürliche Bremse von mTOR, genannt TSC1, in drei wichtigen Lungenzellpopulationen: Fibroblasten, die die Stützmatrix produzieren, Endothelzellen, die Blutgefäße auskleiden, und alveoläre Epithelzellen, die die Oberfläche der Lungenbläschen bilden. Drei Monate nach dieser gezielten Veränderung zeigten alle drei Modelle starke Anzeichen von Seneszenz und eine Aktivierung des mTOR‑Signalwegs. Dennoch war der sichtbare Lungenschaden je nach betroffenen Zellen auffallend unterschiedlich. Bei überaktiven mTOR‑Signal in Fibroblasten entwickelten die Lungen ausgeprägte Narbenbildungen (Fibrose) mit verdickten, kollagenreichen Wänden. Wurde dasselbe Signal in Endothelzellen angeschaltet, entstanden stattdessen Emphyseme mit vergrößerten, zerstörten Lufträumen, aber wenig Narben. Die Aktivierung von mTOR in den alveolären Oberflächenzellen erzeugte ein gemischtes Bild: sowohl emphysemähnliche Zerstörung als auch fibrotische Verdickung, was einer beim Menschen bekannten Erkrankung namens kombinierte pulmonale Fibrose und Emphysem ähnelt.
Entfernen geschädigter Zellen, um die Lunge zu retten
Die Forschenden prüften anschließend, ob das Beseitigen dieser seneszenten Zellen den Schaden rückgängig machen könnte. Sie behandelten die Mäuse mit ABT‑263, einem Wirkstoff, der gezielt den Zelltod seneszenter Zellen auslösen soll. In allen drei genetisch veränderten Mäusestämmen senkte ABT‑263 Seneszenzmarker und reduzierte Signale des mTOR‑Weges. Diese zelluläre „Säuberung“ ging einher mit messbaren Verbesserungen der Lungenstruktur. Die Narbenbildung nahm in den Fibroblasten‑Modellen ab, das Emphysem verringerte sich in den Endothelzielmodellen, und sowohl Narben als auch Zerstörung besserten sich — wenn auch nicht vollständig — in den Mäusen mit veränderten alveolären Oberflächenzellen. Diese Ergebnisse deuten darauf hin, dass in relativ jungen erwachsenen Lungen mTOR‑getriebene seneszente Zellen maßgebliche Treiber struktureller Schäden sind und dass deren Entfernung gesündere Zellen die Gewebereparatur ermöglichen kann.
Was in natürlich alternden Lungen passiert
Das Team untersuchte außerdem normale Mäuse im Alter von einem bis 20 Monaten, was etwa dem Verlauf von frühem Leben bis ins hohe Alter entspricht. Mit zunehmendem Alter sammelten die Lungen schrittweise mehr Kollagen an, entwickelten größere Lufträume und zeigten höhere Werte von Seneszenzmarkern sowie stärkere mTOR‑Signale. Als ältere Mäuse mit demselben senolytischen Wirkstoff behandelt wurden, nahmen Zeichen zellulären Alterns und mTOR‑Aktivität ab, und es zeigte sich eine moderate Reduktion der Narbenbildung. Die strukturellen Verbesserungen waren jedoch weit weniger dramatisch als in den genetisch veränderten Mäusen, und das Emphysem besserte sich nicht deutlich. Das deutet darauf hin, dass in vollständig gealterten Lungen die Schäden tiefer verwurzelt und schwerer umkehrbar sind — möglicherweise weil bereits viele Zelltypen betroffen sind oder weil die Reparatursysteme selbst verschlissen sind.
Was das für die künftige Lungengesundheit bedeutet
In der Summe zeigt die Studie, dass das zu starke Hochdrehen eines einzigen Wachstumsreglers, mTOR, in verschiedenen Lungenzellen sehr unterschiedliche Krankheitsbilder hervorrufen kann: Narbenbildung, Zerstörung der Lufträume oder eine Mischung aus beidem. Sie zeigt außerdem, dass diese schädlichen Effekte eng mit der Ansammlung seneszenter Zellen verbunden sind und dass deren Entfernung die Lungenstruktur bei jüngeren erwachsenen Tieren erheblich, wenn auch nicht vollständig, wiederherstellen kann. In alternden Lungen verbessert dieselbe Strategie die zellulären Signale, formt das Gewebe aber nur geringfügig um — ein Hinweis darauf, dass frühe Interventionen wichtig sein könnten. Für Personen mit Risiko für chronische Lungenerkrankungen rücken mTOR und zelluläre Seneszenz damit als zentrale, miteinander verknüpfte Ziele in den Fokus und eröffnen die Möglichkeit, dass Kombinationstherapien, die mTOR bremsen und seneszente Zellen entfernen, eines Tages dazu beitragen könnten, die Lungenfunktion bis ins hohe Alter zu erhalten.
Zitation: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Schlüsselwörter: Lungenalterung, zelluläre Seneszenz, mTOR‑Signalweg, pulmonale Fibrose, Emphysem