Clear Sky Science · sv
Aktivering av mTOR i lungan leder till lungfibros eller emfysem via senescens i specifika lungceller
Varför åldrande lungor berör oss alla
När vi blir äldre förändras våra lungor långsamt, vilket gör oss mer sårbara för andningsproblem som emfysem och fibros. Dessa tillstånd skadar alveolerna och det stödjande vävnadsstommen i lungan, vilket gör att människor blir andfådda och lätt trötta. Studien bakom den här artikeln ställer en enkel men viktig fråga: vad går fel inne i specifika lungceller som orsakar så skilda skademönster, och kan borttagning av dessa skadade celler hjälpa lungan att återhämta sig?
En central tillväxtbrytare i lungceller
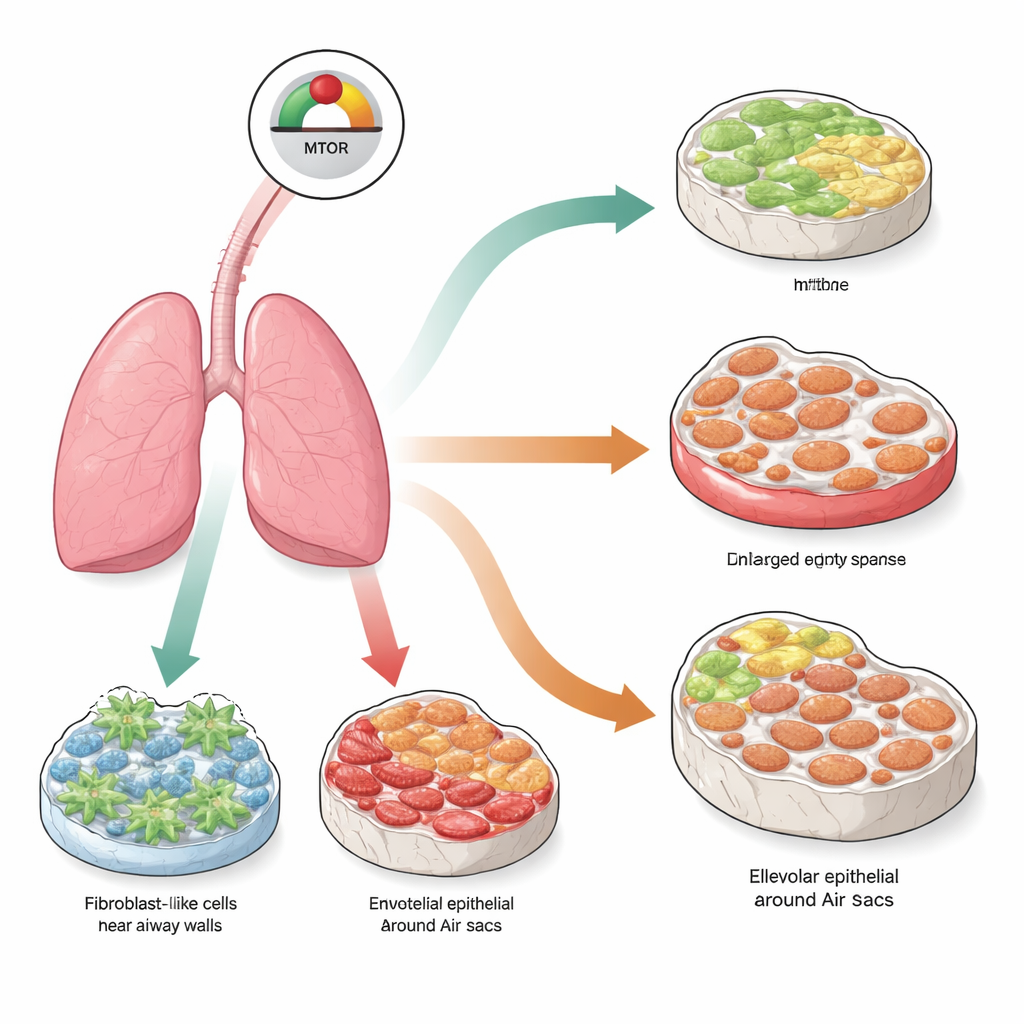
I kärnan av detta arbete finns en molekylär kontrollpunkt kallad mTOR, som hjälper celler att känna av näring och avgöra om de ska växa, dela sig eller förbli stilla. I normal vävnad är mTOR-aktiviteten noggrant avvägd. När den pressas för hårt under för lång tid kan celler gå in i ett tillstånd som kallas senescens, där de permanent slutar dela sig och börjar släppa ut en blandning av inflammatoriska och vävnadsombyggande molekyler. Forskarna undrade om att sätta mTOR i permanent övervarv i olika lungcellstyper skulle driva dessa celler till senescens och därigenom skapa olika former av lungsjukdom som liknar det som ses hos äldre människor.
Tre celltyper, tre mönster av lungskada
Med hjälp av genetiskt modifierade möss tog teamet selektivt bort en naturlig broms på mTOR, kallad TSC1, i tre stora lungcellspopulationer: fibroblaster som producerar det stödjande matrixet, endotelceller som bekläder blodkärlen, och alveolära epitelceller som bildar ytan av luftblåsorna. Tre månader efter denna målinriktade förändring visade alla tre modeller starka tecken på senescens och aktivering av mTOR-vägen. Trots detta var den synliga lungskadan påfallande olika beroende på vilka celler som drabbades. När mTOR var överaktivt i fibroblaster utvecklade lungorna omfattande ärrbildning, eller fibros, med tjocka kollagenrika väggar. När samma signal aktiverades i endotelceller utvecklade lungorna istället emfysem, med förstorade, sönderdelade luftutrymmen men lite ärrbildning. Att slå på mTOR i alveolens ytceller gav en blandad bild: både emfysemliknande nedbrytning och fibrotisk förtjockning, vilket efterliknar ett tillstånd hos människor känt som kombinerad pulmonell fibros och emfysem.
Rensa skadade celler för att rädda lungan
Forskarna testade sedan om avlägsnande av dessa senescenta celler kunde vända skadan. De behandlade mössen med ABT-263, ett läkemedel utvecklat för att selektivt utlösa död hos senescenta celler. I alla tre de genetiskt modifierade musextyrerna sänkte ABT-263 markörer för senescens och minskade signaler från mTOR-vägen. Denna cellulära städning gick hand i hand med mätbara förbättringar i lungstrukturen. Ärrbildningen minskade hos de möss där fibroblaster riktats in, emfysemet minskade hos mössen med endotelceller påverkade, och både ärr och nedbrytning förbättrades, om än inte helt, hos mössen med förändrade alveolära ytceller. Dessa resultat tyder på att, åtminstone i relativt unga vuxna lungor, är senescenta celler drivna av mTOR-överaktivitet viktiga aktörer i att orsaka strukturell skada och att borttagning av dem kan tillåta friskare celler att reparera vävnaden.
Vad som händer i naturligt åldrande lungor
Teamet studerade också normala möss när de åldrades från en månad till 20 månader, ungefär från tidig ålder till hög ålder. Med stigande ålder ackumulerade lungorna gradvis mer kollagen, utvecklade större luftutrymmen och visade högre nivåer av senescensmarkörer tillsammans med starkare mTOR-signalering. När äldre möss behandlades med samma senolytiska läkemedel minskade markörer för cellåldrande och mTOR-aktivitet, och det skedde en måttlig minskning av ärrbildning. De strukturella förbättringarna var dock långt mindre dramatiska än i de genetiskt modifierade mössen, och emfysemet förbättrades inte tydligt. Detta tyder på att i fullt åldrande lungor har skadan blivit mer djupt rotad och svårare att återställa, kanske eftersom många olika celltyper redan är påverkade eller eftersom reparationssystemen själva har försvagats.
Vad detta innebär för framtida lunghälsa
Tillsammans visar studien att att höja en enda tillväxtkontrollbrytare, mTOR, för högt i olika lungceller kan leda till mycket olika sjukdomsmönster: ärrbildning, förstörelse av luftutrymmen eller en blandning av båda. Den visar också att dessa skadliga effekter är nära knutna till uppbyggnaden av senescenta celler och att rensning av sådana celler i hög grad, om än inte fullständigt, kan återställa lungstrukturen hos yngre vuxna djur. I åldrande lungor förbättrar samma strategi cellulära signaler men formar bara vävnaden i liten grad, vilket antyder att tidig intervention kan vara avgörande. För personer i riskzonen för kroniska lungsjukdomar lyfter detta arbete fram mTOR och cellulär senescens som centrala, sammankopplade mål och väcker möjligheten att kombinationsbehandlingar som syftar till att dämpa mTOR och avlägsna senescenta celler en dag skulle kunna hjälpa till att bevara lungfunktionen på ålderns höst.
Citering: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Nyckelord: lungåldrande, cellulär senescens, mTOR-vägen, pulmonell fibros, emfysem