Clear Sky Science · nl
Activering van mTOR in de long leidt via veroudering van specifieke longcellen tot longfibrose of emfyseem
Waarom verouderende longen ons allemaal aangaan
Naarmate we ouder worden, veranderen onze longen langzaam, waardoor we kwetsbaarder worden voor ademhalingsproblemen zoals emfyseem en fibrose. Deze aandoeningen beschadigen de luchtzakjes en het ondersteunende weefsel van de long, waardoor mensen kortademig en snel vermoeid raken. De studie achter dit artikel stelt een eenvoudige maar belangrijke vraag: wat gaat er mis in specifieke longcellen waardoor zulke verschillende schadepatronen ontstaan, en kan het verwijderen van die beschadigde cellen het herstel van de long bevorderen?
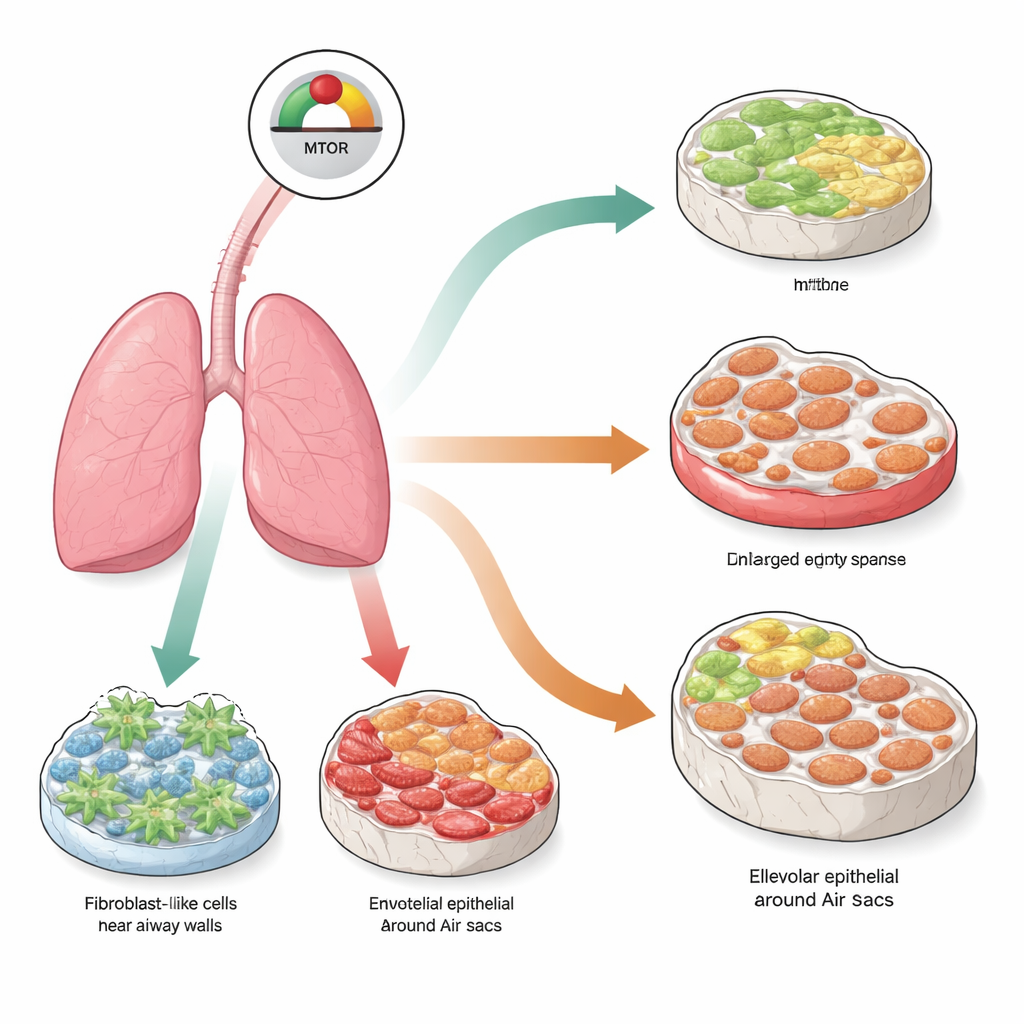
Een centraal groeiregelpunt in longcellen
Centraal in dit werk staat een moleculair regelpunt genaamd mTOR, dat cellen helpt voedingsstoffen te detecteren en te beslissen of ze moeten groeien, delen of in rust blijven. In normaal weefsel is de activiteit van mTOR zorgvuldig in balans. Als het te lang te sterk geactiveerd wordt, kunnen cellen in een toestand terechtkomen die senescentie wordt genoemd: ze stoppen permanent met delen en beginnen een mengsel van ontstekings- en weefselherstelende stoffen af te scheiden. De onderzoekers vroegen zich af of het permanent overactiveren van mTOR in verschillende longceltypes die cellen in senescentie zou duwen en daardoor verschillende vormen van longziekte zou veroorzaken die lijken op wat bij oudere mensen wordt gezien.
Drie celtypes, drie patronen van longschade
Met genetisch gemodificeerde muizen verwijderde het team selectief een natuurlijke rem op mTOR, genaamd TSC1, in drie belangrijke longcelpopulaties: fibroblasten die het ondersteunende matrix produceren, endotheelcellen die bloedvaten bekleden, en alveolaire epitheelcellen die het oppervlak van de luchtzakjes vormen. Drie maanden na deze gerichte wijziging vertoonden alle drie modellen sterke tekenen van senescentie en activatie van de mTOR-route. Toch was de zichtbare longschade sterk verschillend afhankelijk van welke cellen waren aangedaan. Wanneer mTOR overactief was in fibroblasten, ontwikkelden de longen zware littekenvorming, of fibrose, met dikke collageenrijke wanden. Toen hetzelfde signaal werd geactiveerd in endotheelcellen, ontstond in plaats daarvan emfyseem, met vergrote, gescheurde luchtruimten maar weinig littekenvorming. Het aanzetten van mTOR in de alveolaire oppervlaktcellen gaf een gemengd beeld: zowel emfyseemachtige destructie als fibrotische verdikking, hetgeen lijkt op een bij mensen bekende aandoening genaamd gecombineerde pulmonale fibrose en emfyseem.
Beschadigde cellen verwijderen om de long te redden
De onderzoekers testten vervolgens of het verwijderen van deze senescentie-cellen de schade kon omkeren. Ze behandelden de muizen met ABT-263, een middel dat is ontworpen om selectief de dood van senescente cellen teweeg te brengen. In alle drie de gemodificeerde muizenstammen verlaagde ABT-263 senescentie-indicatoren en verminderde het signalen van de mTOR-route. Deze cellulaire schoonmaak ging samen met meetbare verbeteringen in de longstructuur. De littekens namen af bij de muizen met gerichte fibroblasten, het emfyseem verminderde bij de muizen met aangetaste endotheelcellen, en zowel littekenvorming als destructie verbeterden, zij het niet volledig, bij de muizen met gewijzigde alveolaire oppervlaktcellen. Deze resultaten suggereren dat, althans in relatief jonge volwassen longen, senescente cellen gedreven door overactiviteit van mTOR belangrijke veroorzakers zijn van structurele schade en dat het verwijderen ervan gezondere cellen in staat kan stellen het weefsel te herstellen.
Wat er gebeurt in natuurlijk verouderende longen
Het team bestudeerde ook normale muizen terwijl ze ouder werden van één maand tot 20 maanden, wat ruwweg het spectrum van jong naar oud beslaat. Met toenemende leeftijd bouwden de longen geleidelijk meer collageen op, ontwikkelden ze grotere luchtruimten en vertoonden ze hogere niveaus van senescentie-indicatoren samen met sterkere mTOR-signalisatie. Toen oudere muizen met hetzelfde senolytische middel werden behandeld, daalden de markers van celdelingveroudering en mTOR-activiteit, en was er een bescheiden vermindering van littekenvorming. Echter, de structurele verbeteringen waren veel minder dramatisch dan bij de genetisch gemodificeerde muizen, en het emfyseem verbeterde niet duidelijk. Dit suggereert dat in volledig verouderde longen de schade dieper verankerd is en moeilijker te herstellen, mogelijk omdat veel verschillende celtypes al zijn aangedaan of omdat herstelmechanismen zelf achteruit zijn gegaan.
Wat dit betekent voor toekomstige longgezondheid
Samengevat laat de studie zien dat het te sterk opendraaien van één groeiregelaar, mTOR, in verschillende longcellen kan leiden tot zeer uiteenlopende ziektepatronen: littekenvorming, vernietiging van luchtruimten, of een mix van beide. Het toont ook aan dat deze schadelijke effecten nauw samenhangen met de ophoping van senescente cellen en dat het verwijderen van zulke cellen de longstructuur in jongere volwassen dieren aanzienlijk, zij het niet volledig, kan herstellen. In verouderende longen verbetert dezelfde strategie de cellulaire signalen maar verandert het weefsel slechts licht, wat erop wijst dat vroege interventie cruciaal kan zijn. Voor mensen met risico op chronische longaandoeningen benadrukt dit werk mTOR en cellulaire senescentie als centrale, onderling verbonden aanknopingspunten en opent het de mogelijkheid dat gecombineerde therapieën om mTOR te remmen en senescente cellen te verwijderen ooit kunnen helpen longfunctie tot op hoge leeftijd te behouden.
Bronvermelding: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Trefwoorden: longveroudering, cellulaire senescentie, mTOR-route, pulmonale fibrose, emfyseem