Clear Sky Science · ru
Активация mTOR в лёгких приводит к фиброзу или эмфиземе через сенесценцию отдельных типов клеток лёгкого
Почему старение лёгких важно для всех нас
По мере старения наши лёгкие постепенно меняются, и мы становимся более уязвимыми к проблемам с дыханием, таким как эмфизема и фиброз. Эти состояния повреждают альвеолы и поддерживающую ткань лёгкого, из‑за чего люди испытывают одышку и быстро устают. Исследование, лежащее в основе этой статьи, задаёт простой, но важный вопрос: что идёт не так внутри отдельных типов клеток лёгкого, что приводит к таким разным типам повреждений, и можно ли удалить эти повреждённые клетки, чтобы лёгкое восстановилось?
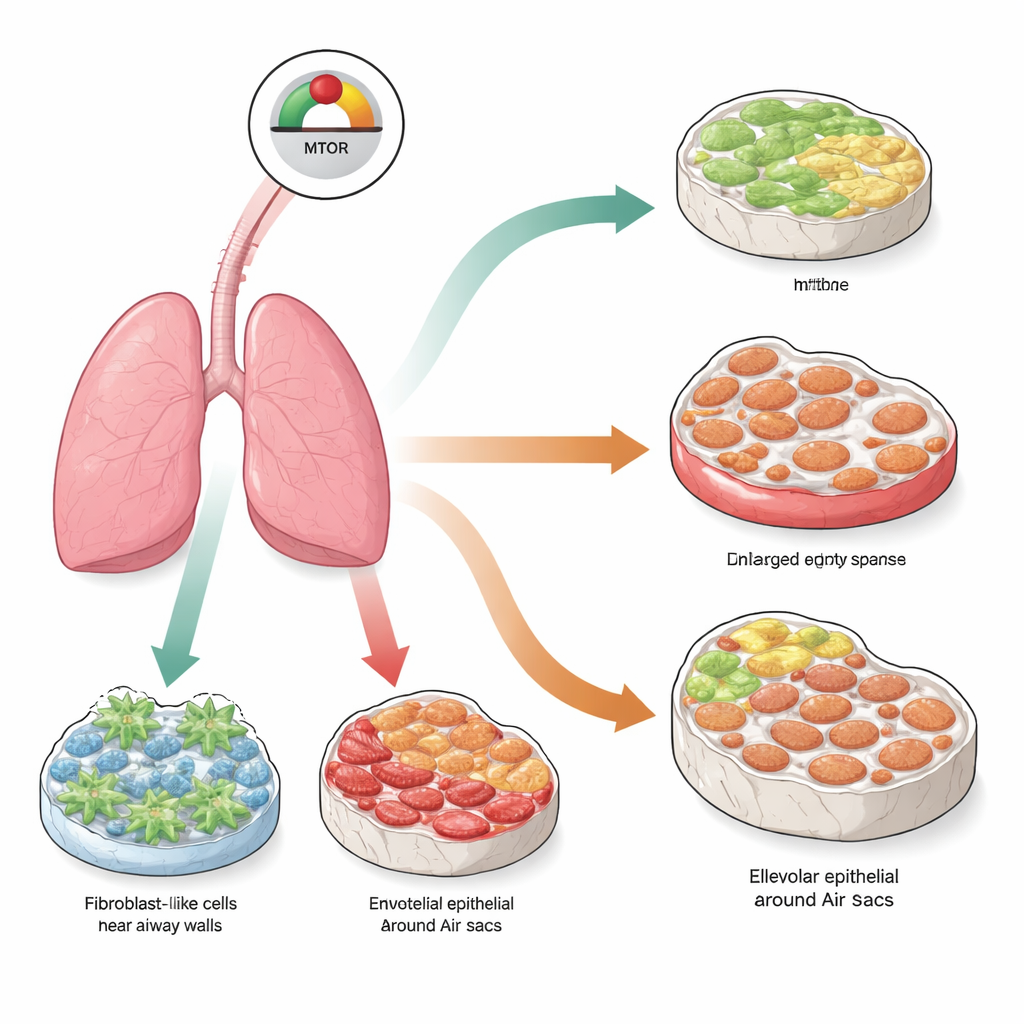
Центральный переключатель роста в клетках лёгкого
В центре этой работы — молекулярный контролёр под названием mTOR, который помогает клеткам ощущать наличие питательных веществ и решать: расти, делиться или оставаться в покое. В нормальной ткани активность mTOR тщательно уравновешена. Когда её чрезмерно стимулируют слишком долго, клетки могут войти в состояние, называемое сенесценцией: они навсегда прекращают делиться и начинают выделять смесь воспалительных и ремоделирующих ткань молекул. Исследователи спросили, приведёт ли перевод mTOR в состояние постоянной гиперактивности в разных типах клеток лёгкого к их сенесценции и, как следствие, к различным формам лёгочных заболеваний, похожих на те, что наблюдаются у пожилых людей.
Три типа клеток — три модели повреждения лёгких
Используя генетически модифицированных мышей, команда выборочно убирала природный тормоз mTOR, называемый TSC1, в трёх основных популяциях клеток лёгкого: фибробластах, производящих опорный матрикс; эндотелиальных клетках, выстилающих кровеносные сосуды; и альвеолярных эпителиальных клетках, формирующих поверхность альвеол. Через три месяца после этой целенаправленной модификации все три модели демонстрировали выраженные признаки сенесценции и активации пути mTOR. Однако видимые повреждения лёгких заметно различались в зависимости от затронутых клеток. При гиперактивности mTOR в фибробластах лёгкие развивали выраженный рубцовый процесс — фиброз с утолщёнными коллаген‑богатыми стенками. При активации того же сигнала в эндотелиальных клетках развивалась эмфизема: расширенные, разрушенные воздушные пространства и мало рубцевания. Активация mTOR в альвеолярных поверхностных клетках давала смешанную картину: как разрушение, похожее на эмфизему, так и фибротическое утолщение, имитируя у людей состояние, известное как комбинированный пульмональный фиброз и эмфизема.
Очистка повреждённых клеток для восстановления лёгкого
Затем исследователи проверили, можно ли обратить повреждение, избавившись от этих сенесцентных клеток. Мышей лечили ABT-263 — препаратом, предназначенным для избирательного запуска гибели сенесцентных клеток. Во всех трёх генетически изменённых линиях ABT-263 снижал маркеры сенесценции и уменьшал сигналы пути mTOR. Эта клеточная «уборка» сопровождалась измеримыми улучшениями в структуре лёгких. В моделях с нацеленными на фибробласты изменениями рубцевание уменьшалось, при нацеливании на эндотелий эмфизема ослабевала, а в моделях с изменёнными альвеолярными клетками и рубцевание, и деструкция улучшались, хоть и не полностью. Эти результаты указывают на то, что по крайней мере в относительно молодых взрослых лёгких сенесцентные клетки, вызванные гиперактивностью mTOR, являются ключевыми факторами структурного повреждения и что их удаление позволяет здоровым клеткам восстановить ткань.
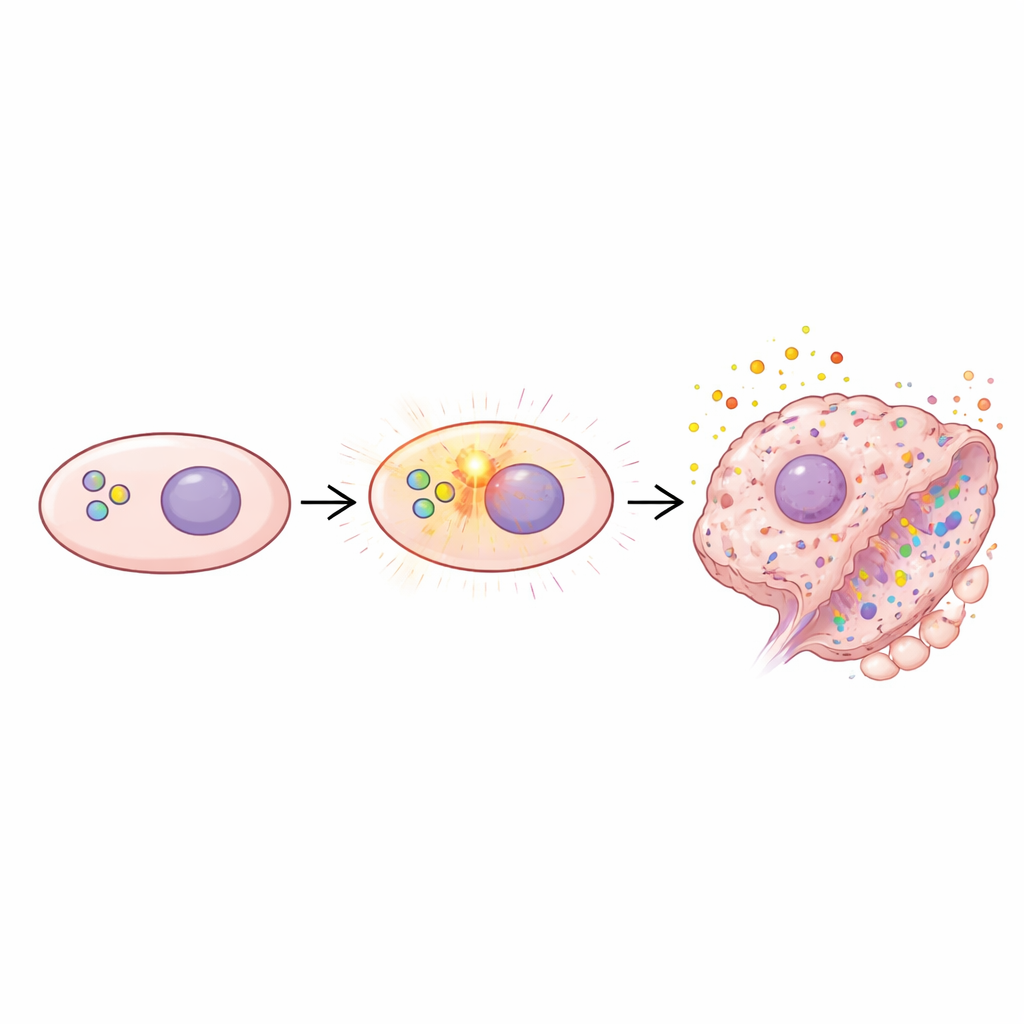
Что происходит в естественно стареющих лёгких
Команда также изучала обычных мышей в процессе естественного старения от одного до двадцати месяцев, охватывая примерно раннюю жизнь до старости. По мере старения лёгкие постепенно накапливали больше коллагена, развивались более крупные воздушные пространства и повышались уровни маркеров сенесценции вместе с усилением сигнала mTOR. Когда старых мышей лечили тем же сенолитиком, маркеры клеточного старения и активность mTOR снижались, и наблюдалось умеренное уменьшение рубцевания. Однако структурные улучшения были значительно менее впечатляющими, чем в генетических моделях, и эмфизема явно не улучшилась. Это говорит о том, что в полностью постаревших лёгких повреждение стало более глубоко укоренившимся и труднее обратимым, возможно потому, что уже затронуты многие типы клеток или потому, что сами репаративные системы истощены.
Что это значит для будущего здоровья лёгких
В сумме исследование показывает: чрезмерное повышение одного переключателя контроля роста — mTOR — в разных клетках лёгких может приводить к очень разным картинам болезни: к фиброзу, разрушению воздушных пространств или к сочетанию того и другого. Оно также демонстрирует, что эти вредные эффекты тесно связаны с накоплением сенесцентных клеток и что их устранение может в значительной степени, хотя и не полностью, восстановить структуру лёгких у молодых взрослых животных. В стареющих лёгких та же стратегия улучшает клеточные сигналы, но лишь слегка меняет ткань, что указывает на важность раннего вмешательства. Для людей, рискующих хронических заболеваний лёгких, эта работа выделяет mTOR и клеточную сенесценцию как центральные взаимосвязанные мишени и ставит гипотезу, что комбинированные подходы, направленные на замедление mTOR и удаление сенесцентных клеток, однажды помогут сохранить функцию лёгких в пожилом возрасте.
Цитирование: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Ключевые слова: старение лёгких, клеточная сенесценция, путь mTOR, пульмональный фиброз, эмфизема