Clear Sky Science · es
La activación de mTOR en el pulmón conduce a fibrosis o enfisema pulmonar a través de la senescencia de células pulmonares específicas
Por qué nos importan los pulmones que envejecen
A medida que envejecemos, nuestros pulmones cambian lentamente, volviéndonos más vulnerables a problemas respiratorios como el enfisema y la fibrosis. Estas enfermedades dañan los alvéolos y el tejido de sostén del pulmón, dejando a las personas con falta de aire y con facilidad para fatigarse. El estudio que sustenta este artículo plantea una pregunta simple pero importante: ¿qué falla dentro de células pulmonares específicas que provoca patrones de daño tan distintos, y puede la eliminación de esas células dañadas ayudar a que el pulmón se recupere?
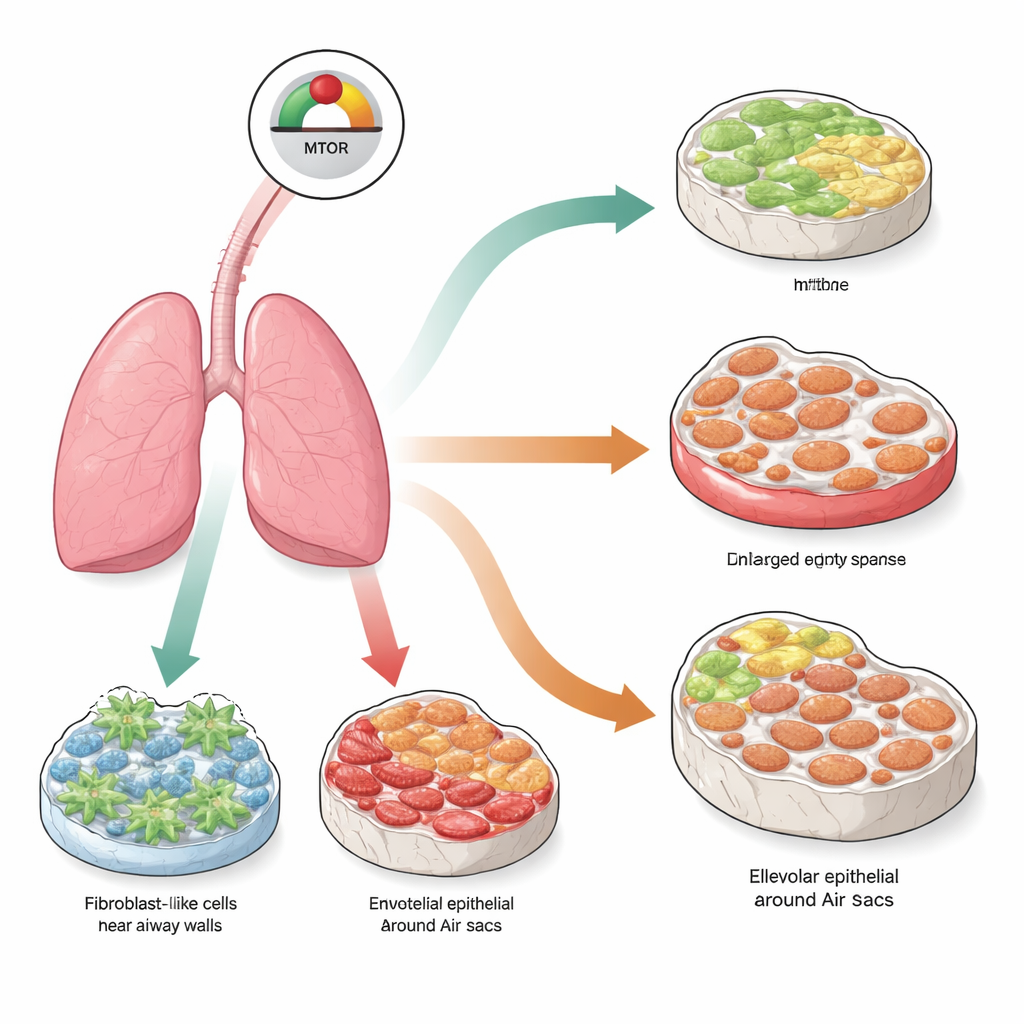
Un interruptor central de crecimiento en las células pulmonares
En el centro de este trabajo está un centro de control molecular llamado mTOR, que ayuda a las células a detectar nutrientes y decidir si crecer, dividirse o mantenerse inactivas. En el tejido normal, la actividad de mTOR está cuidadosamente equilibrada. Cuando se impulsa demasiado durante mucho tiempo, las células pueden entrar en un estado llamado senescencia, en el que dejan de dividirse de forma permanente y comienzan a liberar una mezcla de moléculas inflamatorias y moduladoras de la matriz tisular. Los investigadores se preguntaron si forzar mTOR en un estado de sobreactividad permanente en distintos tipos celulares pulmonares empujaría a esas células hacia la senescencia y, a su vez, generaría distintas formas de enfermedad pulmonar que se asemejan a las que se observan en personas mayores.
Tres tipos celulares, tres patrones de daño pulmonar
Usando ratones genéticamente diseñados, el equipo eliminó selectivamente un freno natural de mTOR, llamado TSC1, en tres poblaciones celulares principales del pulmón: fibroblastos que producen la matriz de sostén, células endoteliales que recubren los vasos sanguíneos y células epiteliales alveolares que forman la superficie de los alvéolos. Tres meses después de este cambio dirigido, los tres modelos mostraron fuertes signos de senescencia y activación de la vía mTOR. Sin embargo, el daño visible en el pulmón fue notablemente distinto según las células afectadas. Cuando mTOR estaba sobreactivo en los fibroblastos, los pulmones desarrollaron un marcado tejido cicatricial, o fibrosis, con paredes gruesas ricas en colágeno. Cuando la misma señal se activó en las células endoteliales, los pulmones desarrollaron en cambio enfisema, con espacios aéreos agrandados y dañados pero poca fibrosis. Activar mTOR en las células de la superficie alveolar produjo un cuadro mixto: tanto destrucción tipo enfisema como engrosamiento fibrótico, imitando una condición humana conocida como fibrosis y enfisema pulmonar combinados.
Eliminar células dañadas para rescatar el pulmón
Los investigadores probaron luego si deshacerse de esas células senescentes podía revertir el daño. Trataron a los ratones con ABT-263, un fármaco diseñado para inducir selectivamente la muerte de células senescentes. En las tres cepas de ratones modificadas, ABT-263 redujo los marcadores de senescencia y disminuyó las señales de la vía mTOR. Esta limpieza celular fue acompañada de mejoras medibles en la estructura pulmonar. La fibrosis disminuyó en los ratones con diana en fibroblastos, el enfisema se atenúo en los ratones con diana en células endoteliales, y tanto la fibrosis como la destrucción mejoraron, aunque no por completo, en los ratones con alteración de las células de la superficie alveolar. Estos resultados sugieren que, al menos en pulmones de adultos jóvenes, las células senescentes impulsadas por la sobreactividad de mTOR son actores principales en el daño estructural y que su eliminación puede permitir que células más sanas reparen el tejido.
Qué ocurre en pulmones que envejecen de forma natural
El equipo también estudió ratones normales a medida que envejecían de un mes a 20 meses, abarcando aproximadamente desde la vida temprana hasta la vejez. Con el avance de la edad, los pulmones acumularon gradualmente más colágeno, desarrollaron espacios aéreos mayores y mostraron niveles más altos de marcadores de senescencia junto con una señalización mTOR más intensa. Cuando ratones mayores fueron tratados con el mismo fármaco senolítico, los marcadores de envejecimiento celular y la actividad de mTOR disminuyeron, y hubo una reducción modesta de la fibrosis. Sin embargo, las mejoras estructurales fueron mucho menos llamativas que en los ratones modificados, y el enfisema no mejoró de forma evidente. Esto sugiere que, en pulmones completamente envejecidos, el daño está más arraigado y es más difícil de revertir, quizá porque ya están afectadas muchas poblaciones celulares o porque los propios sistemas de reparación se han deteriorado.
Qué significa esto para la salud pulmonar futura
En conjunto, el estudio muestra que aumentar demasiado la actividad de un único interruptor de control del crecimiento, mTOR, en distintas células pulmonares puede conducir a patrones de enfermedad muy distintos: fibrosis, destrucción de los espacios aéreos o una combinación de ambos. También demuestra que estos efectos nocivos están estrechamente vinculados a la acumulación de células senescentes y que eliminar dichas células puede restaurar de forma sustancial, aunque no total, la estructura pulmonar en animales adultos jóvenes. En pulmones envejecidos, la misma estrategia mejora las señales celulares pero solo modifica levemente el tejido, lo que sugiere que la intervención temprana puede ser crucial. Para las personas con riesgo de enfermedades pulmonares crónicas, este trabajo destaca a mTOR y la senescencia celular como objetivos centrales e interconectados y plantea la posibilidad de que terapias combinadas destinadas a frenar mTOR y eliminar células senescentes podrían algún día ayudar a preservar la función pulmonar hasta la vejez.
Cita: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Palabras clave: envejecimiento pulmonar, senescencia celular, vía mTOR, fibrosis pulmonar, enfisema