Clear Sky Science · fr
L’activation de mTOR dans les poumons conduit à une fibrose ou un emphysème via la sénescence de cellules pulmonaires spécifiques
Pourquoi le vieillissement des poumons nous concerne tous
En vieillissant, nos poumons se transforment lentement, nous rendant plus vulnérables à des troubles respiratoires comme l’emphysème et la fibrose. Ces maladies endommagent les alvéoles et le tissu de soutien du poumon, provoquant essoufflement et fatigue facile. L’étude décrite ici pose une question simple mais importante : qu’est‑ce qui dysfonctionne à l’intérieur de cellules pulmonaires précises pour produire des schémas de lésions si différents, et l’élimination de ces cellules endommagées peut‑elle favoriser la récupération pulmonaire ?
Un interrupteur de croissance central dans les cellules pulmonaires
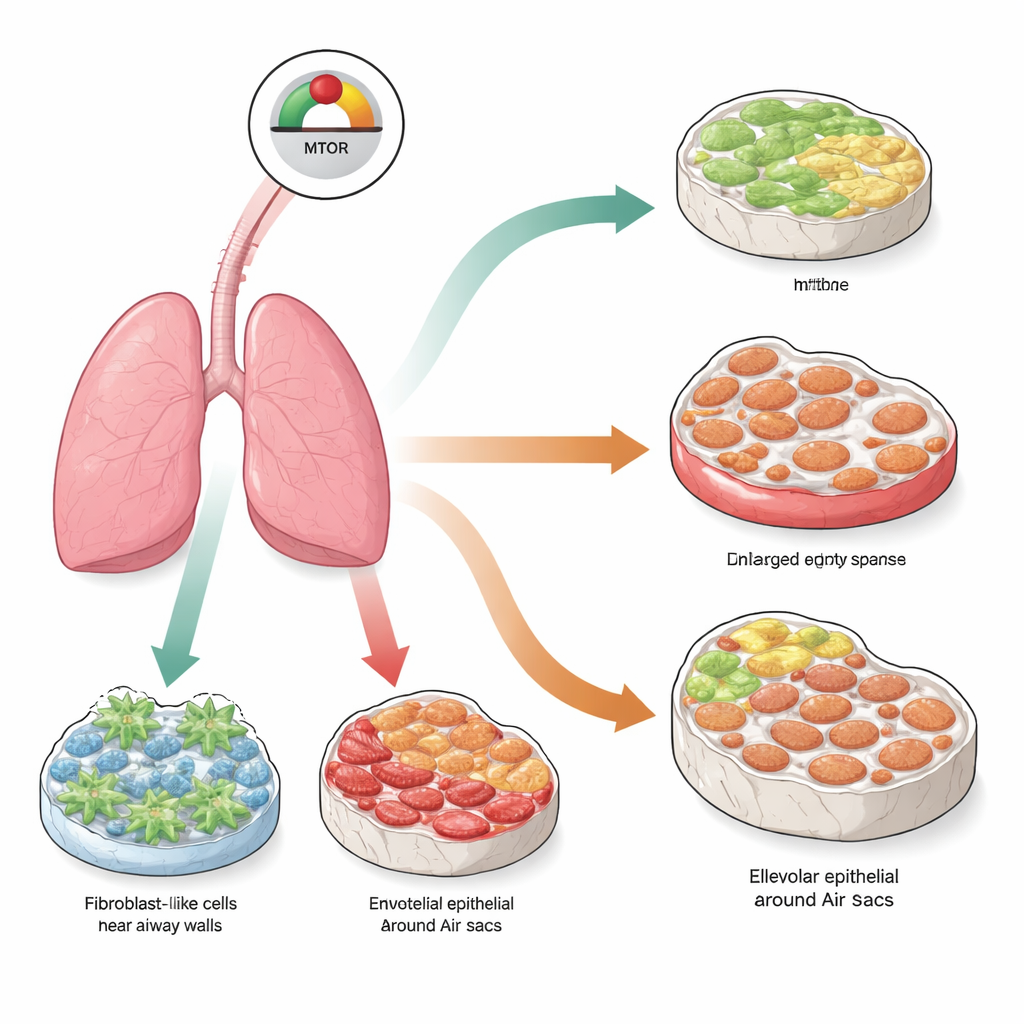
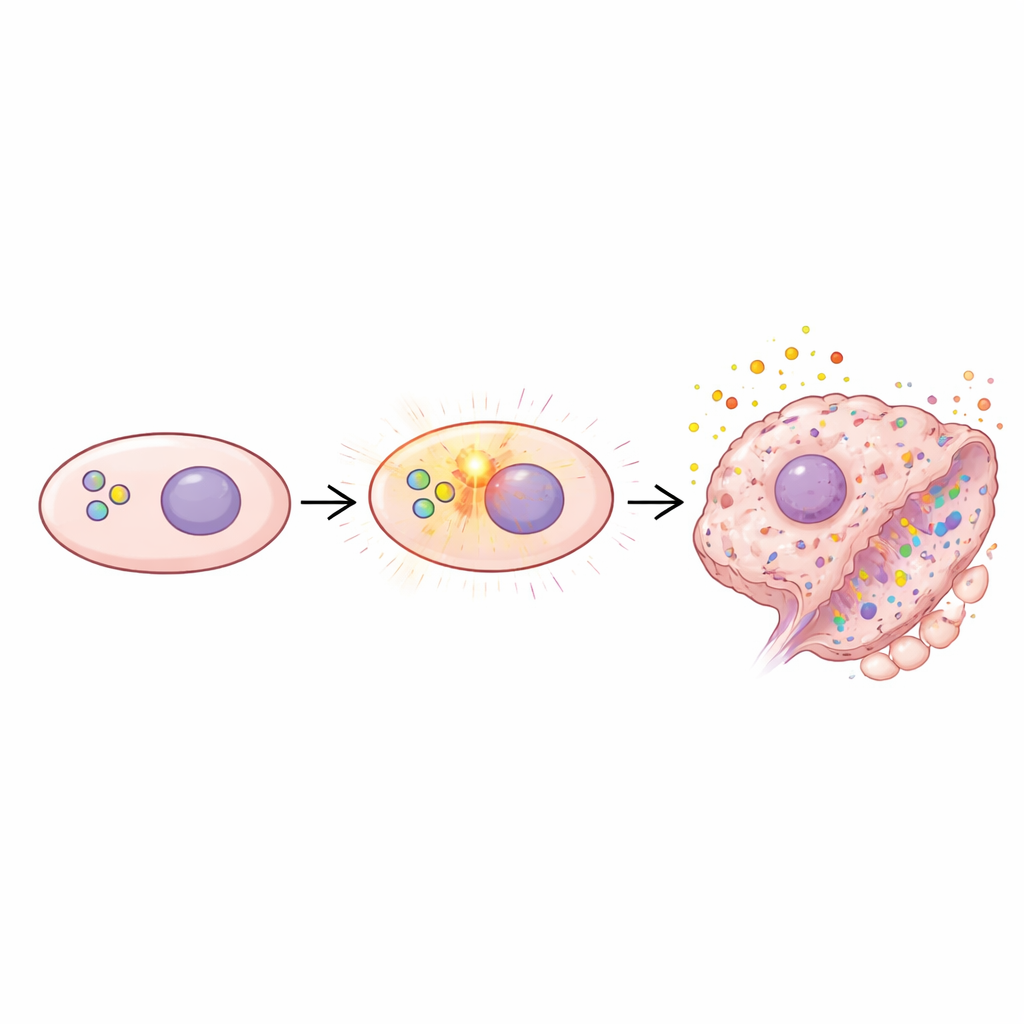
Au centre de ce travail se trouve un nœud de contrôle moléculaire appelé mTOR, qui aide les cellules à détecter les nutriments et à décider de croître, se diviser ou rester au repos. Dans les tissus normaux, l’activité de mTOR est finement régulée. Lorsqu’elle est suractivée de façon prolongée, les cellules peuvent entrer dans un état nommé sénescence, où elles arrêtent définitivement de se diviser et commencent à sécréter un mélange de molécules inflammatoires et de remodelage tissulaire. Les chercheurs ont voulu savoir si la mise en surcharge permanente de mTOR dans différents types cellulaires pulmonaires pousserait ces cellules à la sénescence et provoquerait, selon le type cellulaire touché, des formes variées de maladie pulmonaire rappelant celles observées chez les personnes âgées.
Trois types cellulaires, trois profils de lésions pulmonaires
À partir de souris génétiquement modifiées, l’équipe a supprimé sélectivement un frein naturel de mTOR, appelé TSC1, dans trois populations cellulaires pulmonaires majeures : les fibroblastes qui produisent la matrice de soutien, les cellules endothéliales qui tapissent les vaisseaux sanguins, et les cellules épithéliales alvéolaires qui constituent la surface des alvéoles. Trois mois après cette modification ciblée, les trois modèles présentaient des signes marqués de sénescence et d’activation de la voie mTOR. Pourtant, les lésions pulmonaires visibles différaient fortement selon les cellules affectées. Lorsque mTOR était hyperactif dans les fibroblastes, les poumons développaient une importante cicatrisation, ou fibrose, avec des parois épaissies riches en collagène. Quand le même signal était activé dans les cellules endothéliales, les poumons développaient plutôt un emphysème, avec des espaces aériens agrandis et détruits mais peu de cicatrisation. L’activation de mTOR dans les cellules de surface alvéolaire produisait un tableau mixte : à la fois une destruction de type emphysémateux et un épaississement fibreux, imitant une affection humaine dite fibrose pulmonaire et emphysème combinés.
Éliminer les cellules endommagées pour sauver le poumon
Les chercheurs ont ensuite testé si l’élimination de ces cellules sénescentes pouvait inverser les lésions. Ils ont traité les souris avec l’ABT‑263, un médicament conçu pour déclencher sélectivement la mort des cellules sénescentes. Dans les trois lignées de souris modifiées, l’ABT‑263 a réduit les marqueurs de sénescence et atténué les signaux de la voie mTOR. Ce nettoyage cellulaire s’est accompagné d’améliorations mesurables de la structure pulmonaire. La cicatrisation a diminué chez les souris ciblant les fibroblastes, l’emphysème s’est atténué chez les souris ciblant les cellules endothéliales, et à la fois la fibrose et la destruction se sont améliorées, quoique pas complètement, chez les souris avec altération des cellules de surface alvéolaire. Ces résultats suggèrent que, du moins dans des poumons d’adultes relativement jeunes, les cellules sénescentes induites par la suractivité de mTOR sont des acteurs majeurs des dommages structurels et que leur élimination permet à des cellules plus saines de réparer le tissu.
Que se passe‑t‑il dans les poumons qui vieillissent naturellement
L’équipe a aussi étudié des souris normales vieillissant d’un mois à 20 mois, ce qui couvre approximativement de la petite enfance à un âge avancé. Avec l’âge, les poumons accumulaient progressivement davantage de collagène, développaient des espaces aériens plus grands et présentaient des niveaux plus élevés de marqueurs de sénescence ainsi qu’une signalisation mTOR plus forte. Lorsque des souris âgées ont été traitées par le même sénolytique, les marqueurs de vieillissement cellulaire et l’activité de mTOR ont diminué, et on a observé une réduction modeste de la fibrose. Cependant, les améliorations structurelles étaient bien moins spectaculaires que chez les souris modifiées, et l’emphysème ne s’est pas nettement amélioré. Cela suggère que, dans des poumons pleinement âgés, les lésions sont devenues plus enracinées et plus difficiles à inverser, peut‑être parce que de nombreux types cellulaires sont déjà affectés ou parce que les systèmes de réparation eux‑mêmes sont usés.
Ce que cela signifie pour la santé pulmonaire future
Dans l’ensemble, l’étude montre que l’activation excessive d’un unique interrupteur de contrôle de croissance, mTOR, dans différents types cellulaires pulmonaires peut conduire à des schémas de maladie très divergents : fibrose, destruction des espaces aériens ou un mélange des deux. Elle montre aussi que ces effets nuisibles sont étroitement liés à l’accumulation de cellules sénescentes et que l’élimination de ces cellules peut restaurer de manière substantielle, quoique incomplète, la structure pulmonaire chez de jeunes animaux adultes. Dans les poumons vieillissants, la même stratégie améliore les signaux cellulaires mais ne remodèle que légèrement le tissu, laissant entendre que l’intervention précoce pourrait être cruciale. Pour les personnes à risque de maladies pulmonaires chroniques, ce travail met en évidence mTOR et la sénescence cellulaire comme des cibles centrales et interconnectées et ouvre la possibilité que des thérapies combinées visant à freiner mTOR et à éliminer les cellules sénescentes puissent un jour aider à préserver la fonction pulmonaire jusqu’à un âge avancé.
Citation: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Mots-clés: vieillissement pulmonaire, sénescence cellulaire, voie mTOR, fibrose pulmonaire, emphysème