Clear Sky Science · it
L’attivazione di mTOR nel polmone porta a fibrosi o enfisema via la senescenza di cellule polmonari specifiche
Perché i polmoni che invecchiano ci riguardano tutti
Man mano che invecchiamo, i nostri polmoni cambiano lentamente, rendendoci più vulnerabili a problemi respiratori come enfisema e fibrosi. Queste condizioni danneggiano gli alveoli e il tessuto di sostegno del polmone, lasciando le persone a corto di fiato e facilmente affaticabili. Lo studio alla base di questo articolo pone una domanda semplice ma importante: cosa va storto all’interno di specifiche cellule polmonari che genera schemi così diversi di danno, e rimuovere quelle cellule danneggiate può aiutare il polmone a recuperare?
Un interruttore centrale della crescita nelle cellule polmonari
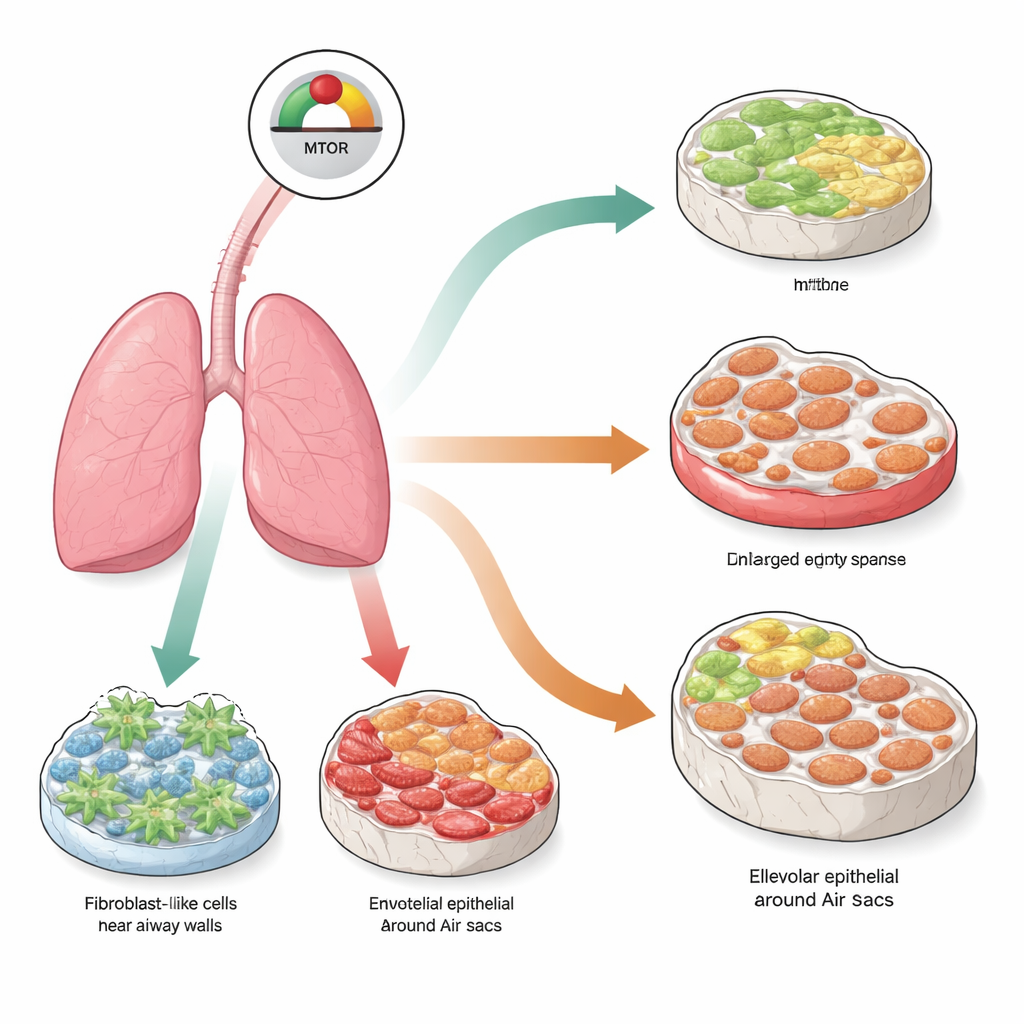
Al centro di questo lavoro c’è un nodo di controllo molecolare chiamato mTOR, che aiuta le cellule a percepire i nutrienti e a decidere se crescere, dividersi o restare quiescenti. Nei tessuti normali l’attività di mTOR è attentamente bilanciata. Quando viene spinta troppo a lungo, le cellule possono entrare in uno stato chiamato senescenza, in cui smettono di dividersi in modo permanente e cominciano a rilasciare un mix di molecole infiammatorie e rimodellanti del tessuto. I ricercatori si sono chiesti se mettere mTOR in sovraattivazione permanente in diversi tipi cellulari polmonari spingesse quelle cellule verso la senescenza e, di conseguenza, generasse diverse forme di malattia polmonare simili a quelle osservate negli anziani.
Tre tipi di cellule, tre pattern di danno polmonare
Usando topi ingegnerizzati geneticamente, il team ha rimosso selettivamente un freno naturale su mTOR, chiamato TSC1, in tre popolazioni cellulari polmonari principali: i fibroblasti che producono la matrice di sostegno, le cellule endoteliali che rivestono i vasi sanguigni e le cellule epiteliali alveolari che formano la superficie degli alveoli. Tre mesi dopo questa modifica mirata, tutti e tre i modelli mostravano forti segni di senescenza e attivazione della via mTOR. Tuttavia il danno polmonare visibile era sorprendentemente diverso a seconda delle cellule coinvolte. Quando mTOR era iperattivo nei fibroblasti, i polmoni sviluppavano una marcata cicatrizzazione, o fibrosi, con pareti spesse ricche di collagene. Quando lo stesso segnale veniva acceso nelle cellule endoteliali, i polmoni sviluppavano invece enfisema, con spazi aerei ingranditi e rotti ma poca cicatrizzazione. Attivare mTOR nelle cellule di superficie alveolare produceva un quadro misto: sia distruzione simile all’enfisema sia ispessimento fibrotico, riproducendo una condizione umana nota come fibrosi polmonare e enfisema combinati.
Eliminare le cellule danneggiate per salvare il polmone
I ricercatori hanno quindi verificato se eliminare queste cellule senescenti potesse invertire il danno. Hanno trattato i topi con ABT-263, un farmaco progettato per indurre selettivamente la morte delle cellule senescenti. In tutti e tre i ceppi di topi ingegnerizzati, ABT-263 ha ridotto i marcatori di senescenza e attenuato i segnali della via mTOR. Questa pulizia cellulare è andata di pari passo con miglioramenti misurabili nella struttura polmonare. La cicatrizzazione è diminuita nei topi con fibroblasti bersaglio, l’enfisema è diminuito nei topi con cellule endoteliali bersaglio e sia la cicatrizzazione sia la distruzione sono migliorate, seppur non completamente, nei topi con alterazione delle cellule di superficie alveolare. Questi risultati suggeriscono che, almeno nei polmoni di adulti relativamente giovani, le cellule senescenti spinte dalla sovraattivazione di mTOR sono protagoniste nel causare danno strutturale e che la loro rimozione può permettere a cellule più sane di riparare il tessuto.
Cosa succede nei polmoni che invecchiano naturalmente
Il gruppo ha anche studiato topi normali mentre invecchiavano da un mese fino a 20 mesi, coprendo grosso modo dalla prima età alla vecchiaia. Con l’avanzare dell’età, i polmoni accumulavano gradualmente più collagene, sviluppavano spazi aerei più grandi e mostravano livelli più alti di marcatori di senescenza insieme a un’intensificazione della segnalazione mTOR. Quando i topi anziani sono stati trattati con lo stesso farmaco senolitico, i marcatori di invecchiamento cellulare e l’attività di mTOR sono diminuiti e si è osservata una modesta riduzione della cicatrizzazione. Tuttavia i miglioramenti strutturali sono stati molto meno pronunziati rispetto ai topi ingegnerizzati e l’enfisema non è migliorato in modo chiaro. Questo suggerisce che, nei polmoni completamente invecchiati, il danno è diventato più radicato e più difficile da invertire, forse perché molti tipi cellulari sono già coinvolti o perché i sistemi di riparazione stessi si sono indeboliti.
Cosa significa per la salute polmonare futura
Nel complesso, lo studio mostra che l’eccessiva attivazione di un singolo interruttore di controllo della crescita, mTOR, in diverse cellule polmonari può portare a modelli di malattia molto diversi: cicatrizzazione, distruzione degli spazi aerei o una combinazione di entrambi. Mostra anche che questi effetti nocivi sono strettamente legati all’accumulo di cellule senescenti e che la loro eliminazione può ripristinare in maniera sostanziale, se non completa, la struttura polmonare negli animali adulti giovani. Nei polmoni invecchiati, la stessa strategia migliora i segnali cellulari ma rimodella il tessuto solo marginalmente, suggerendo che un intervento precoce potrebbe essere cruciale. Per le persone a rischio di malattie polmonari croniche, questo lavoro evidenzia mTOR e la senescenza cellulare come bersagli centrali e interconnessi e apre la possibilità che terapie combinate volte a rallentare mTOR e rimuovere le cellule senescenti possano un giorno contribuire a preservare la funzione polmonare fino alla vecchiaia.
Citazione: Houssaini, A., Marcos, E., Gros, V. et al. Lung mTOR activation leads to lung fibrosis or emphysema via senescence of specific lung cells. Sci Rep 16, 13822 (2026). https://doi.org/10.1038/s41598-026-43628-z
Parole chiave: invecchiamento polmonare, senescenza cellulare, via mTOR, fibrosi polmonare, enfisema