Clear Sky Science · tr
VSIR'in kapsamlı karakterizasyonu, hematolojik malignitelerde çift epigenetik düzenleme ve bağışıklık ortamını ortaya koyuyor
Kan hastalığı olan hastalar için bunun önemi nedir
Hekimlerin birçok katı tümör için güçlü yeni immün tedavileri var, ancak benzer atılımlar lösemi ve lenfoma gibi kan kanserlerinde geride kaldı. Bu çalışma, VSIR adlı bir gen tarafından kontrol edilen, VISTA olarak bilinen daha az bilinen bir immün frenine odaklanıyor. Araştırmacılar, VSIR’in farklı kan kanserlerinde nerede ve nasıl açıldığını, bunun hasta sonuçları ve tedavi yanıtıyla nasıl ilişkili olduğunu haritalayarak, hastaları immünoterapiye uygun şekilde eşleştirmenin ve daha akıllı ilaç kombinasyonları tasarlamanın yeni yollarını işaret ediyor.
Bu immün freninin vücutta nerede göründüğü
Ekip önce temel bir soru sordu: sağlıklı insanlarda bu immün freni normalde hangi hücreler taşır? Binlerce örneğin gen aktivitesi verilerini içeren büyük kamu veri setlerini analiz ederek, VSIR’in nötrofiller ve monositler gibi miyeloid aile beyaz kan hücrelerinde en aktif olduğunu ve birçok diğer dokuda çok daha az aktif olduğunu buldular. Onlarca kanser türü arasında incelediklerinde çarpıcı bir desen ortaya çıktı: tüm kanserler arasında akut miyeloblastik lösemi (AML), VSIR’deki en güçlü artışı gösteriyordu; diğer miyeloid kan hastalıkları da yüksekken, çoğu katı tümörde daha düşük veya hatta azalmış düzeyler vardı. Bu durum AML’i, VISTA freninin özellikle önemli olabileceği bir hastalık olarak öne çıkardı.
Kanser hücreleri VSIR genini nasıl yeniden düzenliyor
Sonraki adımda araştırmacılar bu anormal artışı gerçekten neyin tetiklediğini öğrenmek istedi. VSIR’deki klasik DNA mutasyonlarının nadir olduğunu ve değişikliği açıklayamayacağını buldular. Bunun yerine ana suçlular, DNA’nın ne kadar sıkı paketlendiğini ve genlerin erişilebilir olup olmadığını kontrol eden kimyasal işaretler ve protein kompleksleri olan epigenetik değişikliklerdi. AML ve ilişkili kan bozukluklarında, VSIR’e yakın önemli kontrol bölgeleri genellikle genleri susturan bir kimyasal işaret türü olan metil gruplarını kaybediyordu. Bu metilasyon kaybı birkaç hasta kohortunda ve 168 klinik örnekten oluşan özel bir sette doğrulandı; sağlıklı kemik iliğinden miyelodisplastik sendromlara ve tam gelişmiş AML’e doğru kademeli bir düşüş gösteriyordu. Metilasyon azaldıkça VSIR aktivitesi arttı ve bu epigenetik değişimi genin aşırı aktivasyonu ile doğrudan ilişkilendirdi.
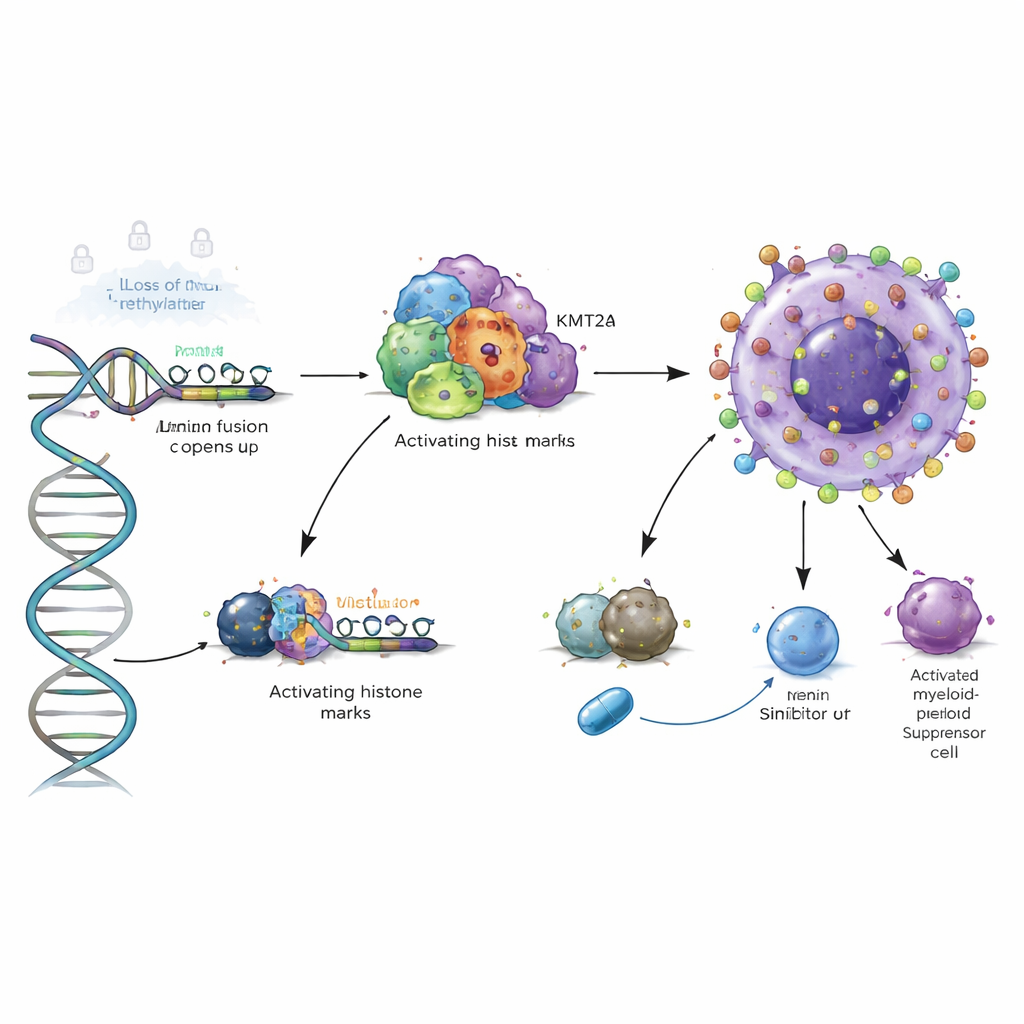
Yüksek riskli lösemide güçlü bir kromatin anahtarı
Çalışma, DNA üzerinde oturan 3 boyutlu protein iskelesini inceleyerek bir katman daha derine indi. KMT2A gen füzyonları veya NPM1 mutasyonları taşıyan yüksek riskli AML tiplerinde, yazarlar füzyon proteinlerinin ve yardımcıları Menin’in doğrudan VSIR kontrol bölgesine bağlandığını ve yerel kromatini açan “aktivasyon” histon işaretlerini getirdiklerini gösterdiler. Hücre modellerinde deneysel Menin inhibitörleri kullanmak bu işaretleri azalttı ve VSIR düzeylerini düşürdü; mutant NPM1’in degradasiyonu benzer etki gösterdi. Bu, VSIR’in bu tehlikeli lösemilerde tesadüfi olarak aktif olmayıp, hedeflenebilir inhibitörlerle potansiyel olarak kapatılabilecek onkojenik bir kromatin programına doğrudan bağlı olduğunu gösteriyor.
VSIR’in tümörün immün komşuluğu için anlamı
VISTA immün hücreler üzerinde etkili olduğundan, yazarlar VSIR düzeylerinin tümör mikroçevresiyle nasıl ilişkili olduğunu incelediler. Birçok kan kanserinden elde edilen hem toplu (bulk) hem de tek hücre verilerini kullanarak, VSIR’in monositler ve makrofajlarda yoğunlaştığını ve ayrıca bazı öldürücü T hücreleri ve doğal öldürücü hücrelerde de bulunduğunu buldular. VSIR-yüksek tümörler genellikle güçlü immün aktivite ve inflamasyon imzaları gösterdi, ancak yardımcı ve zararlı yanıtlar arasındaki denge hastalığa göre farklılık gösteriyordu. AML’de VSIR, T hücresi saldırısını baskılayan hücreler ve yollarla ilişkilendirildi; bu, immün kaçışa yatkın bir lösemi nişini destekliyor. Buna karşılık bazı lenfoid kanserlerde yüksek VSIR, daha etkili immün gözetim özellikleriyle birlikte görünüyordu.
Kimlerin immünoterapiden yararlanacağını tahmin etmek
Ekip daha sonra VSIR’in bir hastanın immün kontrol noktası ilaçlarına nasıl yanıt verebileceğini işaretleyip işaretleyemeyeceğini sordu. İmmünoterapiye yanıtı tahmin eden bir hesaplamalı araç ve melanom ile pankreas kanseri hastalarından gerçek dünya verilerini kullanarak, daha yüksek VSIR ekspresyonuna sahip tümörlerin yanıt verme olasılığının daha yüksek olduğunu ve bu hastaların daha uzun yaşadığını buldular. Kan kanserlerinde, modeller VSIR-yüksek AML, miyelodisplastik sendromlar, myeloma ve birkaç lösemi hastasının kontrol noktası blokajından özellikle fayda sağlayabileceğini öne sürdü; ancak bunun doğrudan klinik testlerle doğrulanması gerekiyor. İlginç bir şekilde, VSIR’in hayatta kalım üzerindeki etkisi hastalığa özgüydü: AML’de daha yüksek VSIR daha kötü sonuçları işaret ederken ve diğer risk faktörleri kontrol edildikten sonra bile bu geçerliydi; oysa diffüz büyük B hücreli lenfoma ve myelomada daha iyi sağkalım ile ilişkilendirildi.
Bu bulgular bakım uygulamalarını nasıl değiştirebilir
Bir arada ele alındığında, bu çalışma VSIR’i iki ana yol aracılığıyla belirli kan kanserlerinde ele geçirilen, ince ayarlı bir immün freni olarak resmediyor: DNA metilasyonunun kaybı ve Menin içeren kromatin kompleksleri tarafından doğrudan aktivasyon. Agresif AML’de bu durum, lösemi hücrelerinin immün saldırıdan korunmasına yardımcı oluyor ve hastaları daha yüksek riskte işaretliyor; ancak aynı zamanda tümörlerin immünoterapiye yanıt vermeye hazır olduğuna işaret edebilir. Çalışma, Menin inhibitörlerini VISTA’yı engelleyen ilaçlarla birleştirmenin özellikle KMT2A yeniden düzenlenmiş ve NPM1-mutant AML’de umut verici bir strateji olabileceğini öne sürüyor. Daha geniş anlamda, VSIR ölçümü hekimlerin her bir kan kanserinin özgül biyolojisine göre immün temelli tedavileri uyarlamasına yardımcı olabilir.
Atıf: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Anahtar kelimeler: VISTA immün kontrol noktası, akut miyeloblastik lösemi, epigenetik düzenleme, Menin KMT2A NPM1, kanser immünoterapisi