Clear Sky Science · it
Caratterizzazione completa di VSIR rivela doppia regolazione epigenetica e paesaggio immunitario nelle neoplasie ematologiche
Perché questo è importante per i pazienti con tumori del sangue
I medici dispongono di potenti nuove terapie immunitarie per molti tumori solidi, ma progressi analoghi sono stati più lenti nei tumori ematologici come leucemie e linfomi. Questo studio si concentra su un freno meno noto del sistema immunitario chiamato VISTA, regolato dal gene VSIR. Mappando dove e come VSIR viene attivato nelle diverse neoplasie del sangue e come ciò si relazione con gli esiti dei pazienti e la risposta alle terapie, i ricercatori indicano nuovi modi per abbinare i pazienti all’immunoterapia e progettare combinazioni farmacologiche più intelligenti.
Dove si trova questo freno immunitario nell’organismo
Il team ha posto innanzitutto una domanda di base: nelle persone sane, quali cellule portano normalmente questo freno immunitario? Analizzando ampi dataset pubblici di espressione genica provenienti da migliaia di campioni, hanno riscontrato che VSIR è più attivo nei globuli bianchi della linea mieloide, come neutrofili e monociti, e molto meno attivo in molti altri tessuti. Guardando attraverso dozzine di tipi tumorali è emerso un pattern netto: tra tutti i tumori, la leucemia mieloide acuta (LMA) mostrava l’aumento più marcato di VSIR, con altre neoplasie mieloidi del sangue anch’esse elevate, mentre la maggior parte dei tumori solidi aveva livelli inferiori o addirittura ridotti. Questo distingue la LMA come una malattia in cui il freno VISTA potrebbe essere particolarmente rilevante.
Come le cellule tumorali riorientano il gene VSIR
I ricercatori hanno poi voluto capire cosa guidasse questo aumento anomalo. Hanno osservato che le mutazioni classiche del DNA in VSIR sono rare e non spiegano il fenomeno. I responsabili principali sono invece cambiamenti epigenetici—marchi chimici e complessi proteici che controllano il grado di compattamento del DNA e l’accessibilità dei geni. Nella LMA e nei disturbi mielodisplastici correlati, regioni chiave di controllo vicine a VSIR perdono gruppi metile, un tipo di marca chimica che di norma mantiene i geni silenti. Questa perdita di metilazione è stata confermata in più coorti di pazienti e in un set dedicato di 168 campioni clinici, mostrando una diminuzione graduale dal midollo osseo sano attraverso le sindromi mielodisplastiche fino alla LMA pienamente sviluppata. Con la riduzione della metilazione, è aumentata l’attività di VSIR, collegando direttamente questo spostamento epigenetico alla sovraattivazione del gene.
Un potente interruttore di cromatina nelle leucemie ad alto rischio
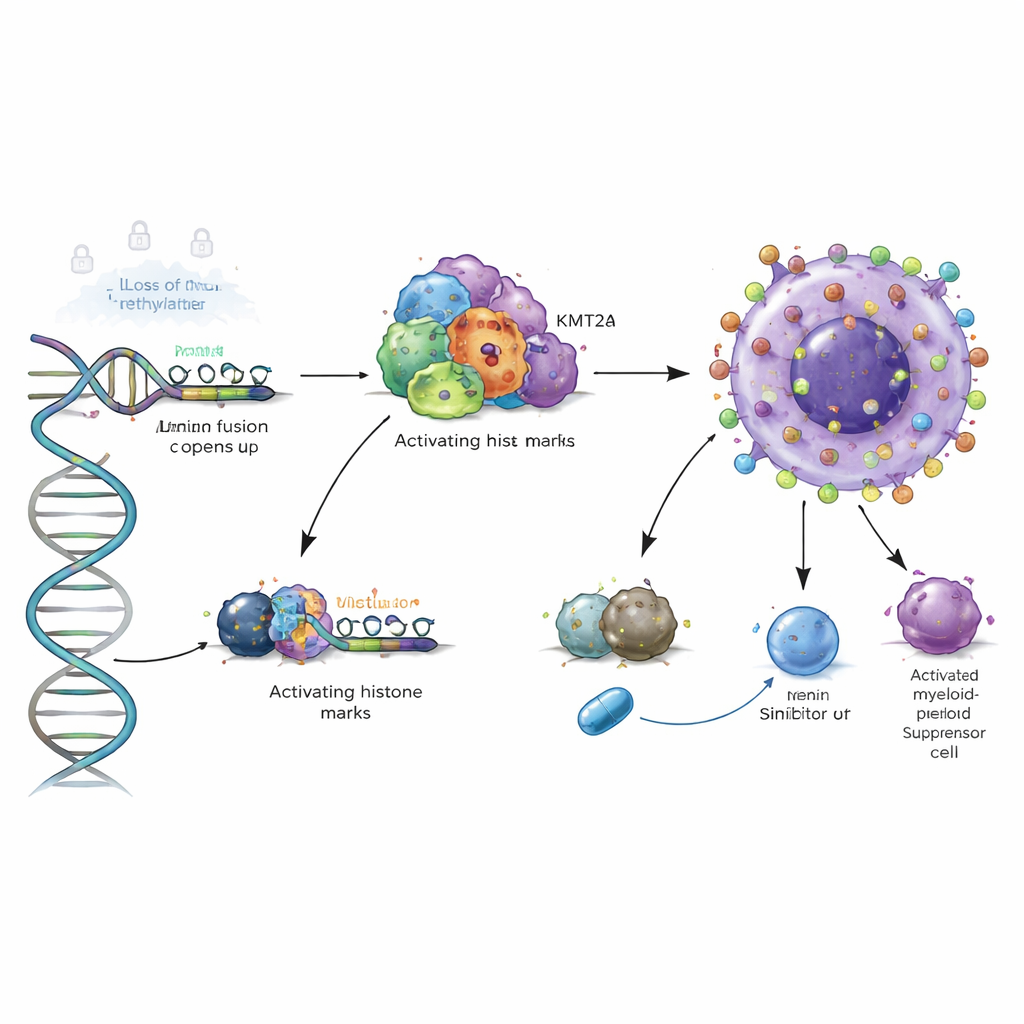
Lo studio ha approfondito ulteriormente esaminando gli impalcature proteiche 3D che si posano sul DNA. Nei tipi di LMA ad alto rischio che presentano fusioni del gene KMT2A o mutazioni di NPM1, gli autori hanno mostrato che le proteine di fusione e il loro cofattore Menin si legano direttamente alla regione di controllo di VSIR, portando marche istoniche “attivanti” che aprono la cromatina locale. Bloccare Menin con farmaci sperimentali in modelli cellulari ha ridotto queste marche e abbassato i livelli di VSIR, e degradare la forma mutante di NPM1 ha avuto un effetto simile. Questo significa che VSIR non è solo incidentalmente attivo in queste leucemie pericolose; è direttamente integrato in un programma cromatinico oncogenico che può potenzialmente essere spento con inibitori mirati.
Cosa significa VSIR per il microambiente immunitario del tumore
Poiché VISTA agisce sulle cellule immunitarie, gli autori hanno studiato come i livelli di VSIR si correlino con il microambiente tumorale. Utilizzando dati sia bulk sia single‑cell provenienti da numerosi tumori del sangue, hanno rilevato che VSIR è concentrato su monociti e macrofagi, ed è presente anche su alcune cellule T citotossiche e cellule natural killer. I tumori con alto VSIR tendevano a mostrare forti firme di attività immunitaria e infiammazione, ma l’equilibrio tra risposte utili e dannose differiva a seconda della malattia. Nella LMA, VSIR era associato a cellule e vie che sopprimono l’attacco delle cellule T, coerente con un nicchia leucemica a-evasiva dell’immunità. Al contrario, in alcune neoplasie linfoidali l’alto VSIR compariva insieme a caratteristiche di sorveglianza immunitaria più efficace.
Prevedere chi trae beneficio dall’immunoterapia
Il team si è poi chiesto se VSIR potesse segnalare quanto bene un paziente potrebbe rispondere ai farmaci che bloccano i checkpoint immunitari. Usando uno strumento computazionale che predice la risposta all’immunoterapia e dati real‑world di pazienti con melanoma e carcinoma pancreatico, hanno scoperto che i tumori con maggiore espressione di VSIR avevano maggior probabilità di rispondere e che questi pazienti vivevano più a lungo. Nei tumori del sangue, i modelli prevedevano che i pazienti VSIR‑high con LMA, sindromi mielodisplastiche, mieloma e diverse leucemie potrebbero trarre particolare beneficio dal blocco dei checkpoint, sebbene ciò richieda ancora verifiche cliniche dirette. È interessante che l’impatto di VSIR sulla sopravvivenza fosse specifico per la malattia: nella LMA un VSIR più alto segnava esiti peggiori anche dopo aver considerato altri fattori di rischio, mentre nel linfoma diffuso a grandi cellule B e nel mieloma era associato a una sopravvivenza migliore.
Come questi risultati potrebbero cambiare la cura
Nel complesso, il lavoro delinea VSIR come un freno immunitario finemente regolato che viene dirottato in certe neoplasie del sangue attraverso due vie principali: perdita di metilazione del DNA e attivazione diretta da complessi cromatinici contenenti Menin. Nella LMA aggressiva questo aiuta le cellule leucemiche a proteggersi dall’attacco immunitario e identifica pazienti a rischio più elevato, ma allo stesso tempo può segnalare quelli i cui tumori sono pronti a rispondere all’immunoterapia. Lo studio suggerisce che combinare inibitori di Menin con farmaci che bloccano VISTA potrebbe essere una strategia promettente, in particolare nelle LMA con riarrangiamenti KMT2A e mutazioni NPM1. Più in generale, misurare VSIR potrebbe aiutare i medici a personalizzare i trattamenti immunitari in base alla biologia specifica di ciascun tumore del sangue.
Citazione: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Parole chiave: checkpoint immunitario VISTA, leucemia mieloide acuta, regolazione epigenetica, Menin KMT2A NPM1, immunoterapia oncologica