Clear Sky Science · nl
Uitgebreide karakterisering van VSIR onthult dubbele epigenetische regulatie en immuunsamenstelling in hematologische maligniteiten
Waarom dit belangrijk is voor patiënten met bloedkanker
Artsen beschikken over krachtige nieuwe immuuntherapieën voor veel solide tumoren, maar vergelijkbare doorbraken bleven in bloedkankers zoals leukemie en lymfoom achter. Deze studie richt zich op een minder bekende rem op het immuunsysteem, VISTA, aangestuurd door het gen VSIR. Door in kaart te brengen waar en hoe VSIR in verschillende bloedkankers wordt aangezet, en hoe dit samenhangt met uitkomst en behandelrespons, wijzen de onderzoekers op nieuwe manieren om patiënten op immuuntherapie af te stemmen en slimmer combinaties van geneesmiddelen te ontwerpen.
Waar deze immuunrem in het lichaam verschijnt
Het team begon met een eenvoudige vraag: bij gezonde mensen welke cellen dragen normaal gesproken deze immuunrem? Door grote openbare datasets met genexpressie uit duizenden monsters te analyseren, vonden ze dat VSIR het meest actief is in myeloïde witte bloedcellen, zoals neutrofielen en monocyten, en veel minder actief is in veel andere weefsels. Bij vergelijking over tientallen kankertypes ontstond een opvallend patroon: van alle kankers vertoonde acute myeloïde leukemie (AML) de sterkste toename van VSIR, met ook hoge niveaus in andere myeloïde bloedkankers, terwijl de meeste solide tumoren lagere of zelfs verminderde niveaus hadden. Dit onderscheidt AML als een ziekte waarin de VISTA-rem mogelijk bijzonder belangrijk is.
Hoe kankercellen het VSIR-gen hereindelen
Vervolgens wilden de onderzoekers weten wat deze abnormale toename daadwerkelijk veroorzaakt. Ze vonden dat klassieke DNA-mutaties in VSIR zeldzaam zijn en de verandering niet kunnen verklaren. In plaats daarvan zijn epigenetische veranderingen de belangrijkste boosdoeners—chemische labels en eiwitcomplexen die regelen hoe strak DNA is verpakt en of genen toegankelijk zijn. Bij AML en verwante bloedziekten verliezen belangrijke regelgebieden nabij VSIR methylgroepen, een type chemische markering die genen doorgaans stilhoudt. Dit verlies van methylatie werd bevestigd in meerdere patiëntengroepen en in een speciale reeks van 168 klinische monsters, en laat een stapsgewijze daling zien van gezond beenmerg via myelodysplastische syndromen naar volwaardige AML. Naarmate de methylatie afnam, nam de VSIR-activiteit toe, waarmee deze epigenetische verschuiving direct aan de overactivatie van het gen werd gekoppeld.
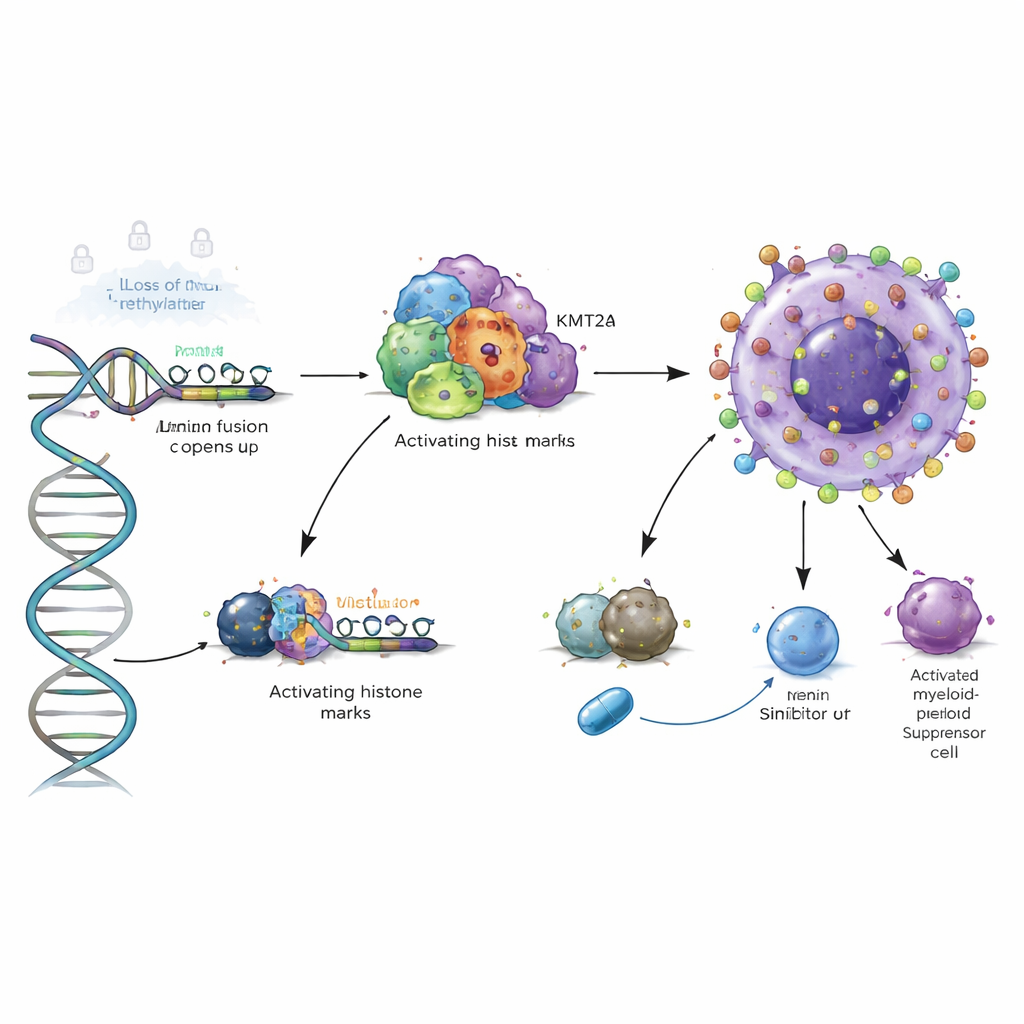
Een krachtige chromatineschakelaar in hoogrisicoleukemie
De studie ging een laag dieper door de 3D-eiwitscaffolds die op DNA zitten te onderzoeken. In hoogrisico-AML-typen met KMT2A-genfusies of NPM1-mutaties toonden de auteurs aan dat fusie-eiwitten en hun cofactor Menin direct binden aan het VSIR-regelgebied, waardoor "activerende" histonmerken worden binnengebracht die het lokale chromatine openen. Het blokkeren van Menin met experimentele middelen in celmodellen verminderde deze merken en verlaagde VSIR-niveaus, en het degraderen van mutant NPM1 had een vergelijkbaar effect. Dit betekent dat VSIR niet slechts bijzaak is in deze gevaarlijke leukemieën; het is direct ingebed in een oncogeen chromatineprogramma dat mogelijk uitgeschakeld kan worden met gerichte remmers.
Wat VSIR betekent voor het immuurneighborhood van de tumor
Aangezien VISTA werkt op immuuncellen, onderzochten de auteurs hoe VSIR-niveaus samenhangen met het tumormicrobioom. Met zowel bulk- als single-celldata uit veel bloedkankers vonden ze dat VSIR geconcentreerd is op monocyten en macrofagen, en ook aanwezig is op sommige cytotoxische T-cellen en natural killer-cellen. VSIR-hoge tumoren toonden vaak sterke tekenen van immuunactiviteit en ontsteking, maar de balans tussen nuttige en schadelijke reacties verschilde per ziekte. In AML was VSIR gekoppeld aan cellen en routes die T-celaanval onderdrukken, in overeenstemming met een immuunevasieve leukemieniche. Daarentegen leek in sommige lymfoïde kankers hoge VSIR samen te gaan met kenmerken van effectievere immuurbewaking.
Voorspellen wie baat heeft bij immunotherapie
Het team vroeg vervolgens of VSIR kan aangeven hoe goed een patiënt mogelijk op immuuncheckpointmiddelen reageert. Met een computationeel hulpmiddel dat respons op immunotherapie voorspelt en met real-world data van patiënten met melanoom en alvleesklierkanker vonden ze dat tumoren met hogere VSIR-expressie vaker reageerden en dat deze patiënten langer leefden. In bloedkankers voorspelden modellen dat VSIR-hoge patiënten met AML, myelodysplastische syndromen, myeloom en verschillende leukemieën mogelijk bijzonder profiteren van checkpoint-blokkade, hoewel dit nog directe klinische toetsing behoeft. Interessant is dat de invloed van VSIR op overleving ziekte-specifiek was: bij AML markeerde hogere VSIR slechtere uitkomsten, zelfs na correctie voor andere risicofactoren, terwijl het bij diffuus groot B-cellymfoom en myeloom geassocieerd was met betere overleving.
Hoe deze bevindingen de zorg zouden kunnen veranderen
Samengevat schetst het werk VSIR als een fijn afgestemde immuunrem die in bepaalde bloedkankers wordt gekaapt via twee hoofdwegen: verlies van DNA-methylatie en directe activatie door Menin-bevattende chromatinecomplexen. In agressieve AML helpt dit leukemiecellen zichzelf te beschermen tegen immuunaanval en markeert het patiënten met een hoger risico, maar tegelijkertijd kan het ook diegenen aanwijzen wier tumoren gereed zijn voor immunotherapie. De studie suggereert dat het combineren van Menin-remmers met middelen die VISTA blokkeren een veelbelovende strategie kan zijn, met name bij KMT2A-herstelde en NPM1-mutante AML. Algemener kan het meten van VSIR artsen helpen immuungerichte behandelingen af te stemmen op de specifieke biologie van elke bloedkanker.
Bronvermelding: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Trefwoorden: VISTA immuuncontrolepunt, acute myeloïde leukemie, epigenetische regulatie, Menin KMT2A NPM1, kankerimmunotherapie