Clear Sky Science · fr
Caractérisation complète de VSIR révèle une double régulation épigénétique et le paysage immunitaire des hémopathies malignes
Pourquoi cela importe pour les patients atteints de cancers du sang
Les médecins disposent aujourd’hui de nouvelles immunothérapies puissantes pour de nombreux cancers solides, mais des percées équivalentes tardent à apparaître pour les hémopathies comme les leucémies et les lymphomes. Cette étude se concentre sur un frein immunitaire moins connu, appelé VISTA, contrôlé par le gène VSIR. En cartographiant où et comment VSIR est activé dans différentes hémopathies, et comment cela se rapporte au pronostic et à la réponse au traitement, les auteurs ouvrent la voie à de nouvelles stratégies pour orienter les patients vers l’immunothérapie et concevoir des combinaisons médicamenteuses plus pertinentes.
Où ce frein immunitaire apparaît dans l’organisme
L’équipe a d’abord posé une question fondamentale : chez des sujets sains, quelles cellules portent normalement ce frein ? En analysant de larges jeux de données publics d’expression génique réunissant des milliers d’échantillons, ils ont constaté que VSIR est le plus actif dans les globules blancs de la lignée myéloïde, comme les neutrophiles et les monocytes, et beaucoup moins dans de nombreux autres tissus. À l’échelle de dizaines de types de cancers, un schéma marquant est apparu : parmi tous les cancers, la leucémie myéloïde aiguë (LMA) présentait l’augmentation la plus nette de VSIR, d’autres hémopathies myéloïdes étant également élevées, tandis que la plupart des tumeurs solides montraient des niveaux plus faibles voire réduits. Cela distingue la LMA comme une maladie où le frein VISTA pourrait être particulièrement important.
Comment les cellules cancéreuses réorientent le gène VSIR
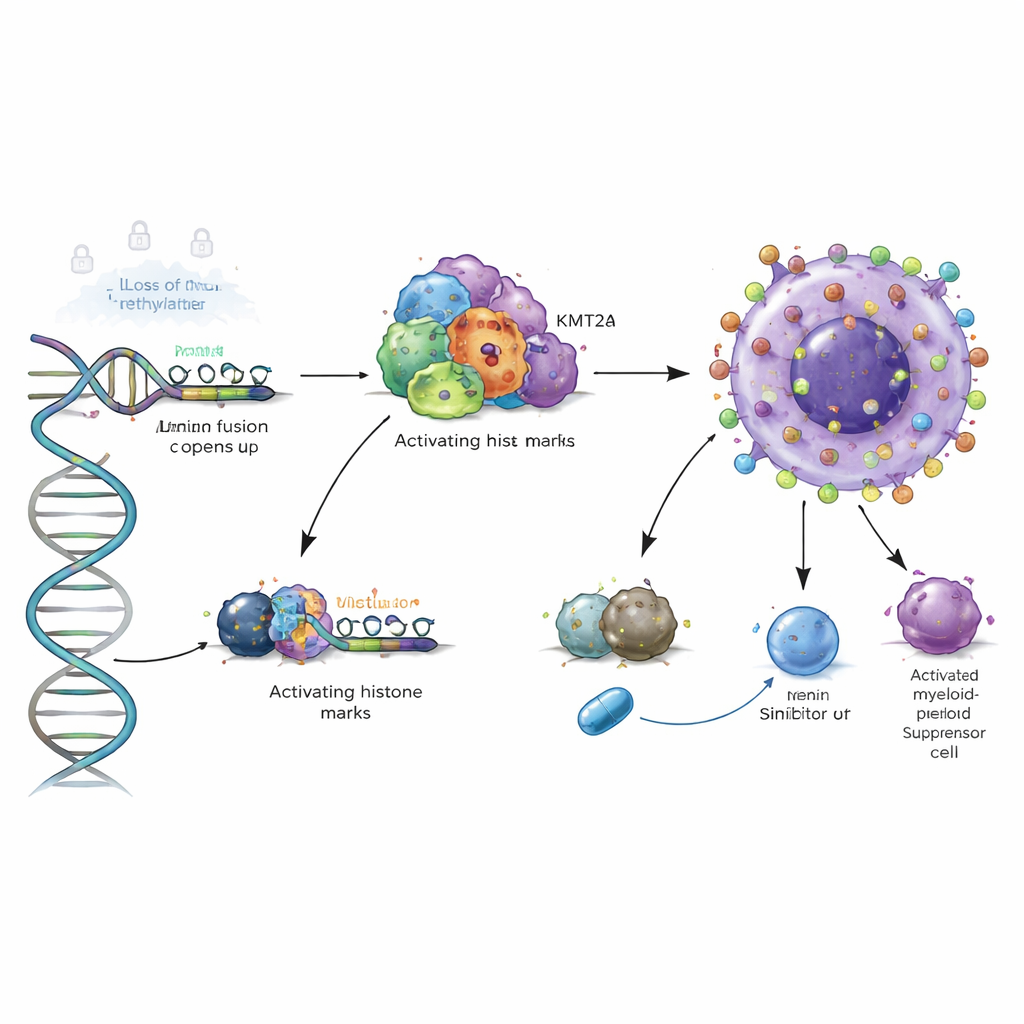
Ensuite, les chercheurs ont voulu savoir ce qui provoque réellement cette augmentation anormale. Ils ont montré que les mutations classiques de l’ADN dans VSIR sont rares et n’expliquent pas l’effet. Les principaux responsables sont plutôt des modifications épigénétiques : des marques chimiques et des complexes protéiques qui gouvernent le compactage de l’ADN et l’accès aux gènes. Dans la LMA et les troubles myélodysplasiques apparentés, des régions de régulation clés proches de VSIR perdent des groupes méthyle, un type de marque chimique qui maintient généralement les gènes silencieux. Cette perte de méthylation a été confirmée dans plusieurs cohortes de patients et dans un jeu dédié de 168 échantillons cliniques, montrant une diminution progressive de la moelle osseuse saine vers les syndromes myélodysplasiques puis la LMA manifeste. À mesure que la méthylation tombait, l’expression de VSIR augmentait, reliant directement ce basculement épigénétique à la suractivation du gène.
Un commutateur chromatinien puissant dans les leucémies à haut risque
L’étude est allée plus loin en examinant les échafaudages protéiques tridimensionnels associés à l’ADN. Dans les types de LMA à haut risque porteurs de fusion du gène KMT2A ou de mutations NPM1, les auteurs montrent que les protéines de fusion et leur cofacteur Menin se lient directement sur la région de contrôle de VSIR, apportant des marques d’histones « activatrices » qui ouvrent la chromatine locale. Le blocage de Menin par des composés expérimentaux dans des modèles cellulaires réduit ces marques et abaisse les niveaux de VSIR, et la dégradation de NPM1 mutant produit un effet similaire. Cela signifie que VSIR n’est pas seulement accessoirement actif dans ces leucémies agressives ; il est directement intégré à un programme chromatinien oncogénique susceptible d’être éteint par des inhibiteurs ciblés.
Ce que VSIR signifie pour le microenvironnement immunitaire de la tumeur
Parce que VISTA agit sur les cellules immunitaires, les auteurs ont étudié comment les niveaux de VSIR se corrèlent avec le microenvironnement tumoral. En utilisant à la fois des données en masse et en cellule unique provenant de nombreuses hémopathies, ils ont trouvé que VSIR se concentre sur les monocytes et les macrophages, et est aussi présent sur certains lymphocytes T cytotoxiques et cellules NK. Les tumeurs riches en VSIR montraient souvent des signatures prononcées d’activité immunitaire et d’inflammation, mais l’équilibre entre réponses utiles et délétères variait selon la maladie. Dans la LMA, VSIR était associé à des cellules et des voies qui suppriment l’attaque des lymphocytes T, cohérent avec un microenvironnement leucémique favorisant l’évasion immunitaire. En revanche, dans certaines hémopathies lymphoïdes, un VSIR élevé s’accompagnait de traits évoquant une surveillance immunitaire plus efficace.
Prédire qui bénéficie de l’immunothérapie
L’équipe a ensuite évalué si VSIR pouvait indiquer la probabilité de réponse aux inhibiteurs de points de contrôle immunitaires. À l’aide d’un outil computationnel prédisant la réponse à l’immunothérapie et de données issues de patients atteints de mélanome et de cancer du pancréas, ils ont constaté que les tumeurs exprimant plus de VSIR avaient davantage de chances de répondre et que ces patients vivaient plus longtemps. Pour les cancers du sang, des modèles ont prédit que les patients VSIR‑élevés atteints de LMA, de syndromes myélodysplasiques, de myélome et de plusieurs leucémies pourraient tirer un bénéfice particulier du blocage des points de contrôle, bien que cela nécessite encore des essais cliniques directs. Fait intéressant, l’impact de VSIR sur la survie dépendait du type de maladie : dans la LMA, un VSIR plus élevé prédominait pour un pronostic plus défavorable même après ajustement pour d’autres facteurs de risque, tandis que dans le lymphome diffus à grandes cellules B et le myélome, il s’associait à une meilleure survie.
Comment ces résultats pourraient modifier la prise en charge
Dans l’ensemble, ces travaux présentent VSIR comme un frein immunitaire finement réglé, détourné dans certaines hémopathies par deux voies principales : la perte de méthylation de l’ADN et l’activation directe par des complexes chromatiniennes contenant Menin. Dans les LMA agressives, cela aide les cellules leucémiques à se protéger de l’attaque immunitaire et identifie des patients à risque plus élevé, mais cela pourrait aussi signaler ceux dont les tumeurs sont prêtes à répondre à l’immunothérapie. L’étude suggère que combiner des inhibiteurs de Menin avec des médicaments bloquant VISTA pourrait être une stratégie prometteuse, en particulier dans les LMA réarrangées KMT2A et porteuses de mutations NPM1. Plus largement, la mesure de VSIR pourrait aider les cliniciens à adapter les traitements immunologiques à la biologie spécifique de chaque cancer du sang.
Citation: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Mots-clés: Point de contrôle immunitaire VISTA, leucémie myéloïde aiguë, régulation épigénétique, Menin KMT2A NPM1, immunothérapie du cancer