Clear Sky Science · pl
Kompleksowa charakterystyka VSIR ujawnia podwójną epigenetyczną regulację i krajobraz odpornościowy w nowotworach krwi
Dlaczego ma to znaczenie dla pacjentów z nowotworami krwi
Lekarze dysponują dziś potężnymi terapiami immunologicznymi wobec wielu nowotworów litych, jednak podobne przełomy w nowotworach krwi, takich jak białaczki i chłoniaki, pojawiają się wolniej. W pracy skoncentrowano się na mniej znanym „hamulcu” układu odpornościowego zwanym VISTA, kontrolowanym przez gen VSIR. Mapując, gdzie i jak VSIR jest aktywowany w różnych nowotworach krwi oraz jak to wiąże się z wynikami pacjentów i odpowiedzią na leczenie, badacze wskazują nowe sposoby dopasowania pacjentów do immunoterapii i projektowania bardziej przemyślanych kombinacji leków.
Gdzie ten immunologiczny hamulec się pojawia w organizmie
Zespół najpierw postawił podstawowe pytanie: które komórki u zdrowych osób zwykle niosą ten hamulec? Analizując obszerne publiczne zbiory danych aktywności genów z tysięcy próbek, stwierdzili, że VSIR jest najbardziej aktywny w białych krwinkach z rodziny mieloidalnej, takich jak neutrofile i monocyty, i znacznie mniej aktywny w wielu innych tkankach. Przy porównaniu dziesiątek typów nowotworów wyłonił się wyraźny wzorzec: spośród wszystkich nowotworów ostra białaczka szpikowa (AML) wykazywała najsilniejszy wzrost ekspresji VSIR, inne mieloidalne nowotwory krwi także były wysokie, podczas gdy większość guzów litych miała niższe albo nawet zredukowane poziomy. To wyróżnia AML jako chorobę, w której hamulec VISTA może mieć szczególne znaczenie.
Jak komórki nowotworowe przesterowują gen VSIR
Następnie badacze chcieli wiedzieć, co właściwie napędza tę nieprawidłową nadaktywność. Stwierdzili, że klasyczne mutacje DNA w VSIR są rzadkie i nie wyjaśniają tego zjawiska. Zamiast nich głównymi sprawcami są zmiany epigenetyczne — chemiczne znaczniki i kompleksy białkowe kontrolujące, jak ciasno upakowane jest DNA i czy geny są dostępne. W AML i powiązanych zaburzeniach krwi kluczowe regiony kontrolne wokół VSIR tracą grupy metylowe, rodzaj chemicznego znaku, który zwykle utrzymuje geny w stanie wyciszenia. Utrata tej metylacji została potwierdzona w kilku kohortach pacjentów oraz w dedykowanym zestawie 168 próbek klinicznych, ukazując stopniowy spadek od zdrowej szpiku kostnego przez zespoły mielodysplastyczne do pełnoobjawowej AML. Wraz z obniżaniem się metylacji aktywność VSIR rosła, łącząc tę epigenetyczną zmianę bezpośrednio z nadaktywacją genu.
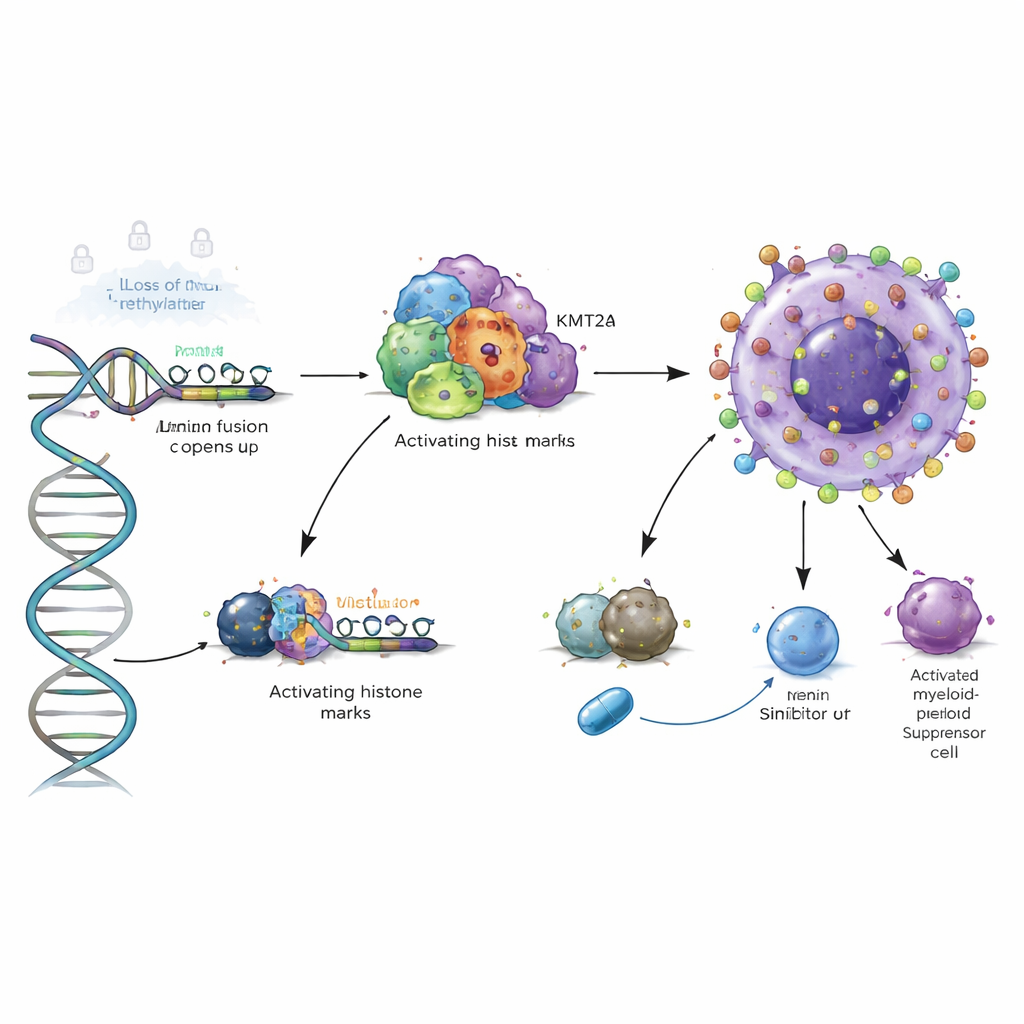
Silny przełącznik chromatyny w białaczce wysokiego ryzyka
Badanie poszło o krok dalej, analizując trójwymiarowe rusztowania białkowe obecne na DNA. W agresywnych podtypach AML z fuzjami genu KMT2A lub mutacjami NPM1 autorzy pokazali, że białka fuzyjne i ich kofaktor Menin wiążą się bezpośrednio w regionie kontrolnym VSIR, przyciągając „aktywujące” znaki histonowe, które otwierają lokalną chromatynę. Hamowanie Menin eksperymentalnymi lekami w modelach komórkowych zmniejszało te znaki i obniżało poziom VSIR, a degradacja zmutowanego NPM1 dawała podobny efekt. To oznacza, że VSIR nie jest przypadkowo aktywny w tych agresywnych białaczkach; jest bezpośrednio włączony w onkogeniczny program chromatynowy, który potencjalnie można wyłączyć za pomocą ukierunkowanych inhibitorów.
Co VSIR oznacza dla immunologicznego sąsiedztwa guza
Ponieważ VISTA działa na komórki odpornościowe, autorzy zbadali, jak poziomy VSIR korelują ze środowiskiem mikroguza. Korzystając zarówno z danych zbiorczych, jak i jednonkomórkowych z wielu nowotworów krwi, stwierdzili, że VSIR koncentruje się w monocytach i makrofagach, a także występuje na niektórych komórkach T cytotoksycznych i komórkach NK. Guzy o wysokim VSIR zwykle wykazywały silne sygnatury aktywności immunologicznej i zapalenia, ale równowaga między odpowiedziami pomocnymi a szkodliwymi różniła się w zależności od choroby. W AML VSIR wiązał się z komórkami i szlakami, które tłumią atak komórek T, co jest spójne z immuno‑ucieczkową niszą białaczki. Natomiast w niektórych nowotworach limfoidalnych wysoki VSIR pojawiał się obok cech skuteczniejszego nadzoru immunologicznego.
Przewidywanie, kto skorzysta z immunoterapii
Zespół zapytał następnie, czy VSIR może sygnalizować, jak dobrze pacjent może odpowiedzieć na leki blokujące punkty kontrolne odporności. Korzystając z narzędzia obliczeniowego przewidującego odpowiedź na immunoterapię oraz z rzeczywistych danych pacjentów z czerniakiem i rakiem trzustki, stwierdzili, że guzy o wyższej ekspresji VSIR miały większe prawdopodobieństwo odpowiedzi, a ci pacjenci żyli dłużej. W nowotworach krwi modele przewidywały, że pacjenci z wysokim VSIR z AML, zespołami mielodysplastycznymi, szpiczakiem mnogim i kilkoma białaczkami mogą szczególnie zyskać na blokadzie punktów kontrolnych, choć wymaga to bezpośrednich testów klinicznych. Co ciekawe, wpływ VSIR na przeżycie był specyficzny dla choroby: w AML wyższe VSIR oznaczało gorsze rokowanie nawet po uwzględnieniu innych czynników ryzyka, podczas gdy w chłoniaku rozlanym z dużych komórek B i w szpiczaku wiązało się to z lepszym przeżyciem.
Jak te odkrycia mogą zmienić opiekę
Łącznie praca przedstawia VSIR jako precyzyjnie ustawiony immunologiczny hamulec, który zostaje przechwycony w niektórych nowotworach krwi poprzez dwa główne mechanizmy: utratę metylacji DNA oraz bezpośrednią aktywację przez kompleksy chromatyny zawierające Menin. W agresywnej AML pomaga to komórkom białaczkowym chronić się przed atakiem immunologicznym i oznacza pacjentów o wyższym ryzyku, ale równocześnie może wskazywać tych, których guzy są przygotowane do odpowiedzi na immunoterapię. Badanie sugeruje, że łączenie inhibitorów Menin z lekami blokującymi VISTA może być obiecującą strategią, szczególnie w AML z rearrangowaniem KMT2A i mutacją NPM1. W szerszym kontekście pomiar VSIR mógłby pomóc lekarzom dostosować terapie oparte na układzie odpornościowym do specyficznej biologii każdego nowotworu krwi.
Cytowanie: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Słowa kluczowe: punkt kontrolny immunologiczny VISTA, ostra białaczka szpikowa, regulacja epigenetyczna, Menin KMT2A NPM1, immunoterapia nowotworowa