Clear Sky Science · sv
Omfattande karaktärisering av VSIR avslöjar dubbel epigenetisk reglering och immunlandskap över hematologiska maligniteter
Varför detta är viktigt för patienter med blodcancer
Läkare har fått kraftfulla nya immunterapier för många solida tumörer, men liknande genombrott har halkat efter vid blodcancer såsom leukemi och lymfom. Denna studie fokuserar på en mindre känd broms för immunsystemet kallad VISTA, styrd av genen VSIR. Genom att kartlägga var och hur VSIR slås på i olika blodcancerformer, och hur detta relaterar till patientutfall och behandlingssvar, pekar forskarna på nya sätt att matcha patienter till immunterapi och att utforma smartare läkemedelskombinationer.
Var denna immunbroms visar sig i kroppen
Teamet ställde först en grundläggande fråga: hos friska personer, vilka celler bär normalt denna immunbroms? Genom att analysera stora offentliga datamängder om genaktivitet från tusentals prov fann de att VSIR är mest aktiv i vita blodkroppar av myeloid typ, såsom neutrofiler och monocyter, och mycket mindre aktiv i många andra vävnader. När de tittade över dussintals cancertyper framträdde ett slående mönster: bland alla cancerformer uppvisade akut myeloisk leukemi (AML) den starkaste ökningen av VSIR, med andra myeloida blodcancerformer också höga, medan de flesta solida tumörer hade lägre eller till och med reducerade nivåer. Detta skiljde AML åt som en sjukdom där VISTA‑bromsen kan vara särskilt betydelsefull.
Hur cancerceller omkopplar VSIR‑genen
Nästa steg var att ta reda på vad som faktiskt driver denna onormala ökning. De fann att klassiska DNA‑mutationer i VSIR är sällsynta och inte kan förklara förändringen. Istället är de huvudsakliga bovarna epigenetiska förändringar—kemiska markörer och proteinkomplex som styr hur tätt DNA är packat och om gener är åtkomliga. I AML och besläktade blodrubbningar tappar nyckelreglerande regioner i närheten av VSIR metylgrupper, en typ av kemisk markör som vanligtvis håller gener tysta. Denna förlust av metylering bekräftades i flera patientkohorter och i ett dedikerat set om 168 kliniska prover, vilket visade ett stegvis fall från frisk benmärg via myelodysplastiska syndrom till fullskalig AML. När metyleringen föll ökade VSIR‑aktiviteten, vilket knöt denna epigenetiska förändring direkt till genens överaktivering.
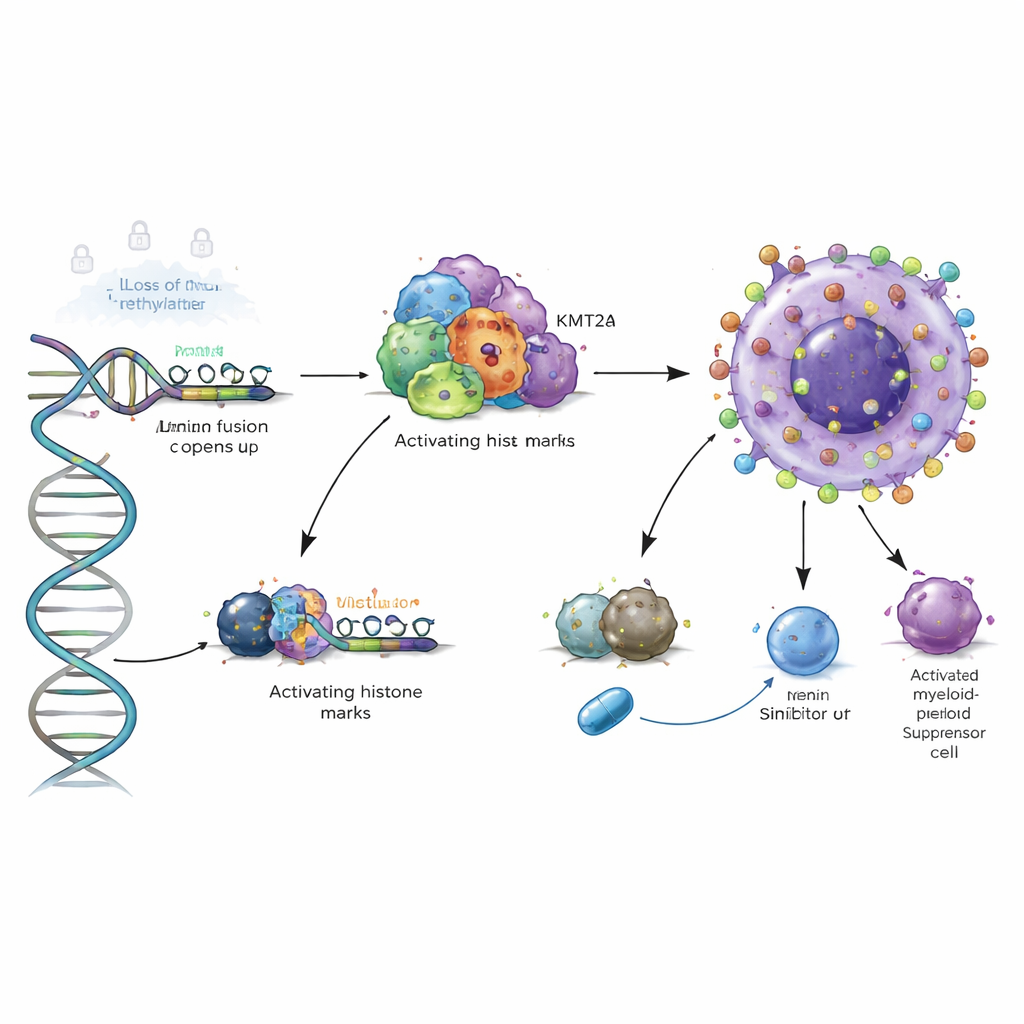
En kraftfull kromatinswitch i hög‑riskleukemi
Studien gick ett lager djupare genom att undersöka de tredimensionella proteinställningar som sitter på DNA. I hög‑risk‑AML‑typer som bär KMT2A‑genfusioner eller NPM1‑mutationer visade författarna att fusionsproteiner och deras kofaktor Menin binder direkt vid VSIRs kontrollregion och rekryterar “aktiverande” histonmarkörer som öppnar den lokala kromatinen. Att blockera Menin med experimentella läkemedel i cellmodeller minskade dessa markörer och sänkte VSIR‑nivåerna, och att degradera muterat NPM1 gav en liknande effekt. Det innebär att VSIR inte bara är passivt aktivt i dessa aggressiva leukemier; det är direkt kopplat till ett onkogent kromatinprogram som potentiellt kan stängas av med riktade hämmare.
Vad VSIR betyder för tumörens immumiljö
Eftersom VISTA verkar på immunceller studerade författarna hur VSIR‑nivåer samvarierar med tumörens mikro‑miljö. Med både bulk‑ och single‑celldata från många blodcancerformer fann de att VSIR koncentreras till monocyter och makrofager, och också finns på vissa cytotoxiska T‑celler och naturliga mördarceller (NK‑celler). VSIR‑höga tumörer tenderade att visa starka signaturer av immunaktivitet och inflammation, men balansen mellan hjälpsamma och skadliga svar skilde sig åt mellan sjukdomarna. I AML kopplades VSIR till celler och pathways som undertrycker T‑cellsattacker, i linje med en immun‑undvikande leukeminisch. I kontrast framträdde i vissa lymfoida cancerformer hög VSIR tillsammans med kännetecken för mer effektiv immunövervakning.
Att förutsäga vem som gynnas av immunterapi
Teamet undrade sedan om VSIR kunde signalera hur väl en patient kan svara på läkemedel mot immunkontrollpunkter. Med ett beräkningsverktyg som predicerar svar på immunterapi och verkliga data från patienter med melanom och pankreascancer fann de att tumörer med högre VSIR‑uttryck var mer benägna att svara och att dessa patienter levde längre. I blodcancer förutspådde modeller att VSIR‑höga patienter med AML, myelodysplastiska syndrom, myelom och flera leukemier kan få särskild nytta av checkpoint‑blockad, även om detta fortfarande kräver direkt klinisk prövning. Intressant nog var VSIRs inverkan på överlevnad sjukdomsspecifik: i AML markerade högre VSIR sämre utfall även efter att andra riskfaktorer beaktats, medan det i diffus stor B‑cellslymfom och myelom associerades med bättre överlevnad.
Hur dessa fynd kan förändra vården
Tillsammans målar arbetet upp VSIR som en finjusterad immunbroms som kapats i vissa blodcancerformer via två huvudsakliga vägar: förlust av DNA‑metylering och direkt aktivering av Menin‑innehållande kromatincomplex. I aggressiv AML hjälper detta leukemiceller att skärma av sig från immunangrepp och markerar patienter med högre risk, men samtidigt kan det signalera dem vars tumörer är förberedda att svara på immunterapi. Studien föreslår att kombinera Menin‑hämmare med läkemedel som blockerar VISTA kan vara en lovande strategi, särskilt vid KMT2A‑omarrangerad och NPM1‑mutant AML. Mer generellt kan mätning av VSIR hjälpa läkare att skräddarsy immunbaserade behandlingar efter den specifika biologin i varje blodcancer.
Citering: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Nyckelord: VISTA immunkontrollpunkt, akut myeloisk leukemi, epigenetisk reglering, Menin KMT2A NPM1, cancerimmunterapi