Clear Sky Science · ru
Всеобъемлющая характеристика VSIR выявляет двойную эпигенетическую регуляцию и иммунный ландшафт при гематоонкологических заболеваниях
Почему это важно для пациентов с раком крови
Врачи получили мощные новые иммунные терапии для многих солидных опухолей, но аналогичные прорывы в заболеваниях крови — таких как лейкоз и лимфома — отстают. В этом исследовании внимание сосредоточено на менее известном «тормозе» иммунной системы — белке VISTA, кодируемом геном VSIR. Нанализировав, где и как включается VSIR в разных гематоонкологических заболеваниях и как это соотносится с исходом болезни и ответом на лечение, авторы указывают на новые способы подобрать пациентов для иммунотерапии и разработать более разумные комбинации лекарств.
Где этот иммунный «тормоз» проявляется в организме
Команда сначала задала базовый вопрос: в каких клетках у здоровых людей этот механизм обычно присутствует? Проанализировав крупные общедоступные наборы данных активности генов из тысяч образцов, они обнаружили, что VSIR наиболее активен в клетках миелоидного ряда белых кровяных клеток, таких как нейтрофилы и моноциты, и значительно менее активен во многих других тканях. При сравнении десятков типов рака проявилась заметная закономерность: среди всех опухолей острый миелоидный лейкоз (ОМЛ) показал наибольшее повышение экспрессии VSIR, другие миелоидные гемоболезни также были высоки, тогда как у большинства солидных опухолей уровни были ниже или даже снижены. Это выделило ОМЛ как заболевание, где тормоз VISTA может иметь особое значение.
Как раковые клетки перенастраивают ген VSIR
Далее исследователи хотели понять, что на самом деле вызывает это аномальное увеличение. Они установили, что классические ДНК‑мутации в VSIR редки и не объясняют изменения. Вместо этого основными виновниками оказались эпигенетические изменения — химические метки и белковые комплексы, которые регулируют упаковку ДНК и доступность генов. При ОМЛ и связанных с ним заболеваниях ключевые регуляторные области рядом с VSIR теряют метильные группы — тип химической метки, который обычно поддерживает гены в неактивном состоянии. Эта потеря метилирования была подтверждена в нескольких когортах пациентов и в отдельной серии из 168 клинических образцов, показав постепенное снижение от здорового костного мозга через миелодиспластические синдромы до манифестного ОМЛ. По мере снижения метилирования активность VSIR возрастала, что напрямую связывает эту эпигенетическую перестройку с чрезмерной активацией гена.
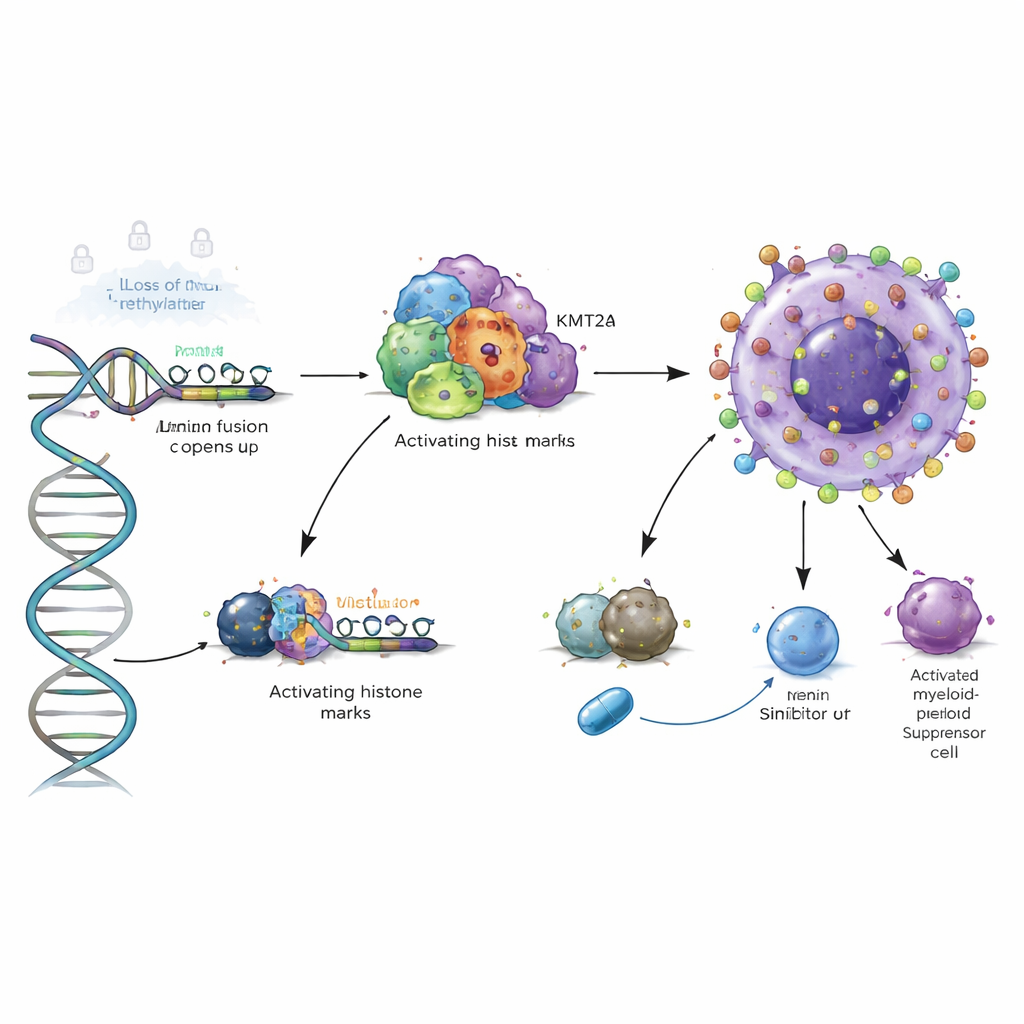
Мощный хроматиновый переключатель в лейкозах высокого риска
Исследование углубилось, изучив 3D‑белковые каркасы, связанные с ДНК. В агрессивных формах ОМЛ, несущих слияния гена KMT2A или мутации NPM1, авторы показали, что белки слияния и их ко‑фактор Menin непосредственно связываются с регуляторной областью VSIR, привлекая «активирующие» гистоновые метки, которые открывают локальный хроматин. Блокирование Menin экспериментальными препаратами в клеточных моделях уменьшало эти метки и снижало уровни VSIR, а деградация мутантного NPM1 давала похожий эффект. Это означает, что VSIR активирован не случайно в этих высокоонкогенных лейкозах — он напрямую включён в онкогенную хроматиновую программу, которую потенциально можно отключить с помощью целевых ингибиторов.
Что VSIR означает для иммунного окружения опухоли
Поскольку VISTA действует на иммунные клетки, авторы изучили, как уровни VSIR коррелируют с микросредой опухоли. Используя как бульк‑, так и одно‑клеточные данные из многих гематоонкологических болезней, они обнаружили, что VSIR сосредоточен в моноцитах и макрофагах, а также присутствует на некоторых цитотоксических Т‑клетках и натуральных киллерах. Опухоли с высоким уровнем VSIR, как правило, демонстрировали сильные признаки иммунной активности и воспаления, но соотношение полезных и вредных реакций варьировало в зависимости от заболевания. В ОМЛ VSIR связывался с клетками и путями, подавляющими Т‑клеточную атаку, что согласуется с иммунно‑эвазивной нишей лейкоза. Напротив, в некоторых лимфоидных опухолях высокий VSIR встречался наряду с признаками более эффективного иммунного надзора.
Прогнозирование, кто выиграет от иммунотерапии
Далее команда выясняла, может ли VSIR сигнализировать о том, насколько хорошо пациент отреагирует на препараты, блокирующие контрольные точки иммунитета. Используя вычислительный инструмент для прогнозирования ответа на иммунотерапию и данные из реальной практики у пациентов с меланомой и раком поджелудочной железы, они обнаружили, что опухоли с более высокой экспрессией VSIR с большей вероятностью отвечали на лечение и такие пациенты жили дольше. В гематоонкологии модели предсказывали, что пациенты с высоким VSIR при ОМЛ, миелодиспластических синдромах, миеломе и нескольких лейкозах могут особенно выиграть от блокады контрольных точек, хотя это требует прямого клинического подтверждения. Интересно, что влияние VSIR на выживаемость было специфично для заболевания: в ОМЛ более высокий VSIR указывал на худший прогноз даже с учётом других факторов риска, тогда как при диффузной крупноклеточной В‑клеточной лимфоме и миеломе он ассоциировался с лучшей выживаемостью.
Как эти результаты могут изменить лечение
В совокупности работа рисует образ VSIR как тонко настроенного иммунного «тормоза», который в некоторых гематоонкологических заболеваниях захватывается двумя основными путями: потерей метилирования ДНК и прямой активацией хроматиновыми комплексами с Menin. В агрессивном ОМЛ это помогает лейкозным клеткам скрываться от иммунной атаки и обозначает пациентов с более высоким риском, но одновременно может указывать на тех, чьи опухоли готовы ответить на иммунотерапию. Исследование предлагает, что комбинация ингибиторов Menin и препаратов, блокирующих VISTA, может быть перспективной стратегией, особенно при KMT2A‑перестановках и мутациях NPM1. В более широком смысле измерение VSIR может помочь врачам точнее подбирать иммунно‑ориентированное лечение в соответствии с биологией конкретного заболевания крови.
Цитирование: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Ключевые слова: контрольный иммунный механизм VISTA, острый миелоидный лейкоз, эпигенетическая регуляция, Menin KMT2A NPM1, иммунотерапия рака