Clear Sky Science · pt
Caracterização abrangente de VSIR revela dupla regulação epigenética e panorama imune nas malignidades hematológicas
Por que isso importa para pacientes com câncer sanguíneo
Médicos dispõem de novas terapias imunes poderosas para muitos tumores sólidos, mas avanços semelhantes ficaram atrasados em cânceres do sangue como leucemia e linfoma. Este estudo foca um freio menos conhecido do sistema imune chamado VISTA, controlado por um gene chamado VSIR. Ao mapear onde e como o VSIR é ligado em diferentes cânceres hematológicos, e como isso se relaciona com desfechos dos pacientes e resposta ao tratamento, os pesquisadores apontam novas formas de ajustar pacientes à imunoterapia e projetar combinações de drogas mais inteligentes.
Onde esse freio imune aparece no corpo
A equipe começou com uma pergunta básica: em pessoas saudáveis, quais células normalmente carregam esse freio imune? Ao analisar grandes bancos públicos de atividade gênica com milhares de amostras, encontraram que o VSIR é mais ativo nas células brancas da linhagem mieloide, como neutrófilos e monócitos, e muito menos ativo em muitos outros tecidos. Ao examinar dezenas de tipos de câncer, surgiu um padrão marcante: entre todos os cânceres, a leucemia mieloide aguda (LMA) mostrou o aumento mais forte de VSIR, com outros cânceres mieloides do sangue também altos, enquanto a maioria dos tumores sólidos apresentou níveis mais baixos ou até reduzidos. Isso distingue a LMA como uma doença em que o freio VISTA pode ser especialmente relevante.
Como as células cancerosas reprogramam o gene VSIR
Em seguida, os pesquisadores quiseram saber o que realmente impulsiona esse aumento anormal. Constataram que mutações clássicas no DNA do VSIR são raras e não explicam a mudança. Em vez disso, os principais culpados são alterações epigenéticas — marcas químicas e complexos proteicos que controlam o grau de empacotamento do DNA e se genes ficam acessíveis. Na LMA e em desordens hematológicas relacionadas, regiões regulatórias críticas próximas ao VSIR perdem grupos metil, um tipo de marca química que normalmente silencia genes. Essa perda de metilação foi confirmada em vários coortes de pacientes e em um conjunto dedicado de 168 amostras clínicas, mostrando uma queda gradual da medula óssea saudável, passando por síndromes mielodisplásicas até a LMA franca. À medida que a metilação diminuía, a atividade de VSIR aumentava, vinculando essa alteração epigenética diretamente à superativação do gene.
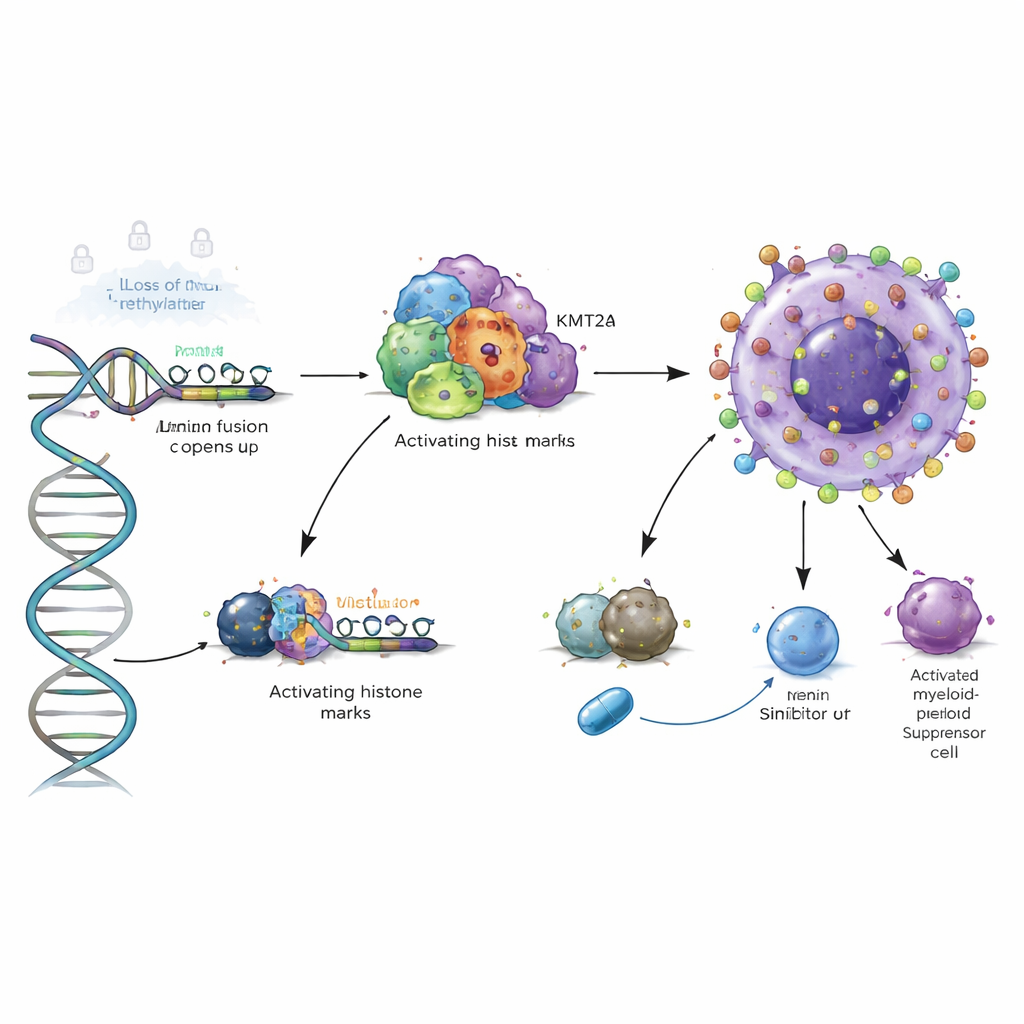
Um potente interruptor de cromatina em leucemias de alto risco
O estudo aprofundou-se examinando os andaimes proteicos 3D que se assentam no DNA. Em tipos de LMA de alto risco que carregam fusões no gene KMT2A ou mutações em NPM1, os autores mostraram que proteínas de fusão e seu cofator Menin se ligam diretamente à região de controle do VSIR, trazendo marcas de histonas “ativadoras” que abrem a cromatina local. Bloquear a Menin com drogas experimentais em modelos celulares reduziu essas marcas e baixou os níveis de VSIR, e degradar a NPM1 mutante teve efeito semelhante. Isso significa que o VSIR não está apenas incidentalmente ativo nessas leucemias perigosas; ele está diretamente integrado a um programa cromatínico oncogênico que potencialmente pode ser desligado com inibidores direcionados.
O que o VSIR significa para o entorno imune do tumor
Como a VISTA atua sobre células imunes, os autores estudaram como os níveis de VSIR se correlacionam com o microambiente tumoral. Usando dados em larga escala e de célula única de muitos cânceres do sangue, acharam que o VSIR se concentra em monócitos e macrófagos, e também está presente em alguns linfócitos T citotóxicos e células natural killer. Tumores com alto VSIR tendiam a mostrar assinaturas fortes de atividade imune e inflamação, mas o equilíbrio entre respostas úteis e prejudiciais variou conforme a doença. Na LMA, o VSIR esteve ligado a células e vias que suprimem o ataque de células T, consistente com um nicho leucêmico evasivo ao sistema imune. Em contraste, em alguns cânceres linfoides, alto VSIR apareceu ao lado de características de vigilância imune mais eficaz.
Prever quem se beneficia da imunoterapia
A equipe então perguntou se o VSIR poderia sinalizar quão bem um paciente poderia responder a drogas que bloqueiam pontos de checagem imune. Usando uma ferramenta computacional que prevê resposta à imunoterapia e dados do mundo real de pacientes com melanoma e câncer de pâncreas, eles descobriram que tumores com maior expressão de VSIR tinham maior probabilidade de responder e que esses pacientes viveram mais. Em cânceres do sangue, modelos previram que pacientes com alto VSIR com LMA, síndromes mielodisplásicas, mieloma e várias leucemias podem tirar benefício particular do bloqueio de pontos de checagem, embora isso ainda precise de testes clínicos diretos. Curiosamente, o impacto do VSIR na sobrevida foi específico por doença: na LMA, maior VSIR marcou piores desfechos mesmo após ajuste por outros fatores de risco, enquanto no linfoma difuso de grandes células B e no mieloma esteve associado a melhor sobrevida.
Como essas descobertas podem mudar o cuidado
Em conjunto, o trabalho pinta o VSIR como um freio imune finamente regulado que é sequestrado em certos cânceres do sangue por duas rotas principais: perda de metilação do DNA e ativação direta por complexos de cromatina contendo Menin. Na LMA agressiva, isso ajuda as células leucêmicas a se protegerem do ataque imune e marca pacientes de maior risco, mas ao mesmo tempo pode identificar aqueles cujos tumores estão prontos para responder à imunoterapia. O estudo sugere que combinar inibidores de Menin com drogas que bloqueiem a VISTA pode ser uma estratégia promissora, especialmente em LMA com rearranjos KMT2A e mutação em NPM1. De forma mais ampla, medir o VSIR pode ajudar médicos a ajustar tratamentos baseados no sistema imune à biologia específica de cada câncer hematológico.
Citação: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Palavras-chave: ponto de checagem imune VISTA, leucemia mieloide aguda, regulação epigenética, Menin KMT2A NPM1, imunoterapia do câncer