Clear Sky Science · de
Umfassende Charakterisierung von VSIR zeigt doppelte epigenetische Regulation und Immunlandschaft bei hämatologischen Malignomen
Warum das für Patientinnen und Patienten mit Blutkrebs wichtig ist
Bei vielen soliden Tumoren gibt es inzwischen wirkungsvolle Immuntherapien, doch ähnliche Durchbrüche bleiben bei Blutkrebserkrankungen wie Leukämie und Lymphom hinterher. Diese Studie konzentriert sich auf eine weniger bekannte Bremse des Immunsystems namens VISTA, gesteuert vom Gen VSIR. Indem die Forschenden kartieren, wo und wie VSIR in verschiedenen Blutkrebserkrankungen aktiviert wird und wie dies mit Patientenergebnissen und Therapieansprechen zusammenhängt, weisen sie auf neue Wege hin, Patientinnen und Patienten für Immuntherapien zuzuordnen und klügere Wirkstoffkombinationen zu entwerfen.
Wo diese Immunbremse im Körper vorkommt
Das Team stellte zunächst eine grundlegende Frage: Bei gesunden Menschen welche Zellen tragen normalerweise diese Immunbremse? Anhand großer öffentlicher Datensätze zur Genaktivität aus Tausenden Proben fanden sie, dass VSIR am stärksten in myeloiden weißen Blutzellen wie Neutrophilen und Monozyten aktiv ist und in vielen anderen Geweben deutlich weniger. Beim Vergleich über Dutzende von Krebsarten zeichnete sich ein auffälliges Muster ab: Unter allen Tumoren zeigte die akute myeloische Leukämie (AML) den stärksten Anstieg von VSIR, andere myeloide Blutkrebse lagen ebenfalls hoch, während die meisten soliden Tumoren niedrigere oder sogar reduzierte Werte aufwiesen. Das hebt AML als Erkrankung hervor, bei der die VISTA-Bremse besonders relevant sein könnte.
Wie Krebszellen das VSIR‑Gen umprogrammieren
Als Nächstes wollten die Forschenden wissen, was diesen abnormalen Anstieg tatsächlich antreibt. Sie stellten fest, dass klassische DNA‑Mutationen im VSIR selten sind und die Veränderung nicht erklären. Stattdessen sind epigenetische Veränderungen die Hauptverursacher — chemische Markierungen und Proteinkomplexe, die steuern, wie eng DNA verpackt ist und ob Gene zugänglich sind. Bei AML und verwandten Blutkrankheiten verlieren Schlüsselkontrollregionen nahe VSIR Methylgruppen, eine Art chemischer Markierung, die Gene normalerweise stumm hält. Dieser Verlust der Methylierung wurde in mehreren Patientenkohorten und in einer dedizierten Serie von 168 klinischen Proben bestätigt und zeigte einen stufenweisen Rückgang vom gesunden Knochenmark über myelodysplastische Syndrome bis zur manifesten AML. Mit fallender Methylierung stieg die VSIR‑Aktivität, was diese epigenetische Verschiebung direkt mit der Überaktivierung des Gens verbindet.
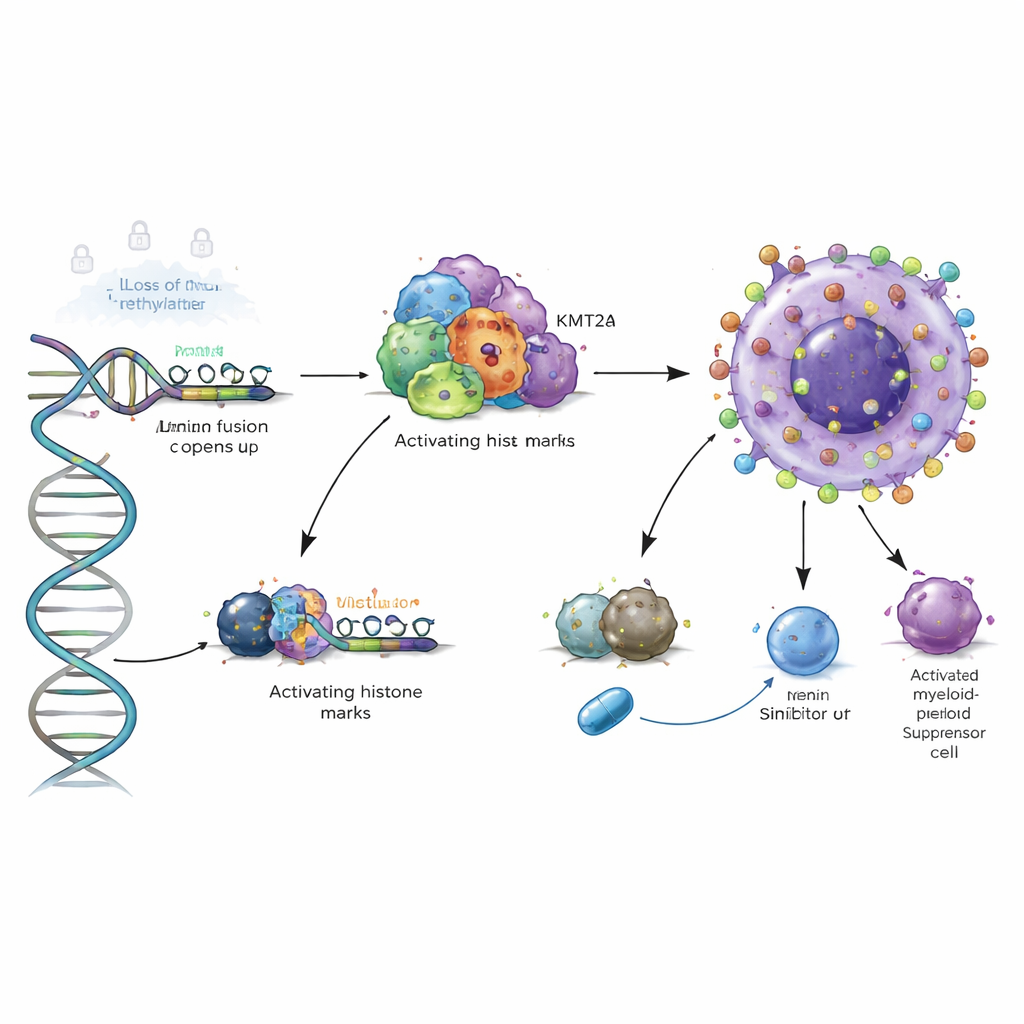
Ein kraftvoller Chromatin‑Schalter bei Hochrisiko‑Leukämien
Die Studie ging eine Ebene tiefer und untersuchte die dreidimensionalen Proteingerüste, die auf der DNA sitzen. In Hochrisiko‑AML‑Typen mit KMT2A‑Genfusionen oder NPM1‑Mutationen zeigten die Autorinnen und Autoren, dass Fusionsproteine und ihr Ko‑Faktor Menin direkt an der VSIR‑Regionskontrolle binden und „aktivierende“ Histonmarken einbringen, die das lokale Chromatin öffnen. Die Blockade von Menin mit experimentellen Wirkstoffen in Zellmodellen reduzierte diese Marken und senkte VSIR‑Spiegel; das gezielte Abbau mutantem NPM1 hatte einen ähnlichen Effekt. Das bedeutet, VSIR ist in diesen aggressiven Leukämien nicht nur beiläufig aktiv, sondern direkt in ein onkogenes Chromatinprogramm eingebunden, das sich potenziell mit zielgerichteten Inhibitoren abschalten lässt.
Was VSIR für das immunologische Umfeld des Tumors bedeutet
Da VISTA auf Immunzellen wirkt, untersuchten die Autorinnen und Autoren, wie VSIR‑Spiegel mit dem Tumormikromilieu korrelieren. Unter Verwendung von Bulk‑ und Einzelzell‑Daten aus zahlreichen Blutkrebserkrankungen fanden sie, dass VSIR auf Monozyten und Makrophagen konzentriert ist und auch auf einigen zytotoxischen T‑Zellen und natürlichen Killerzellen vorkommt. VSIR‑hohe Tumoren zeigten tendenziell starke Signaturen von Immunaktivität und Entzündung, aber das Gleichgewicht zwischen nützlichen und schädlichen Reaktionen variierte je nach Erkrankung. Bei AML war VSIR mit Zellen und Signalwegen verknüpft, die T‑Zell‑Angriffe unterdrücken — konsistent mit einer immunflüchtenden Leukämie‑Nische. Dagegen ging in einigen lymphoiden Krebserkrankungen hohes VSIR mit Merkmalen effektiverer Immunüberwachung einher.
Vorhersage, wer von Immuntherapie profitiert
Das Team prüfte dann, ob VSIR signalisieren könnte, wie gut ein Patient auf Immun-Checkpoint‑Medikamente ansprechen würde. Mithilfe eines rechnerischen Werkzeugs zur Vorhersage des Immuntherapieansprechens und realer Daten von Patientinnen und Patienten mit Melanom und Pankreaskarzinom fanden sie, dass Tumoren mit höherer VSIR‑Expression eher ansprachen und diese Patientinnen und Patienten länger lebten. Bei Blutkrebserkrankungen sagten Modelle voraus, dass VSIR‑hoch‑Patienten mit AML, myelodysplastischen Syndromen, Myelom und mehreren Leukämien möglicherweise besonderen Nutzen von Checkpoint‑Blockaden hätten, wobei dies noch direkte klinische Tests erfordert. Interessanterweise war der Effekt von VSIR auf das Überleben krankheitsspezifisch: In AML markierte höheres VSIR schlechtere Ergebnisse, selbst nach Berücksichtigung anderer Risikofaktoren, während es bei diffus großzelligem B‑Zell‑Lymphom und Myelom mit besserem Überleben assoziiert war.
Wie diese Befunde die Versorgung verändern könnten
Insgesamt zeichnen die Ergebnisse VSIR als fein abgestimmte Immunbremse, die in bestimmten Blutkrebserkrankungen auf zwei Hauptwegen missbraucht wird: Verlust der DNA‑Methylierung und direkte Aktivierung durch Menin‑enthaltende Chromatin‑komplexe. In aggressiver AML hilft dies den Leukämiezellen, sich vor Immunangriffen zu schützen, und kennzeichnet Patientinnen und Patienten mit höherem Risiko, kann aber gleichzeitig jene markieren, deren Tumoren für eine Immuntherapie empfänglich sein könnten. Die Studie legt nahe, dass die Kombination von Menin‑Inhibitoren mit VISTA‑blockierenden Wirkstoffen eine vielversprechende Strategie sein könnte, insbesondere bei KMT2A‑rearrangierter und NPM1‑mutierter AML. Allgemeiner könnte die Messung von VSIR Ärzten helfen, immunbasierte Behandlungen an die spezifische Biologie jeder Blutkrebserkrankung anzupassen.
Zitation: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Schlüsselwörter: VISTA-Immun-Checkpoint, akute myeloische Leukämie, epigenetische Regulation, Menin KMT2A NPM1, Krebsimmuntherapie