Clear Sky Science · es
Caracterización exhaustiva de VSIR revela doble regulación epigenética y paisaje inmunitario en malignidades hematológicas
Por qué esto importa para los pacientes con cáncer de la sangre
Los médicos disponen de poderosas nuevas terapias inmunitarias para muchos tumores sólidos, pero avances similares han tardado en llegar a los cánceres hematológicos como las leucemias y los linfomas. Este estudio se centra en un freno menos conocido del sistema inmune llamado VISTA, controlado por un gen denominado VSIR. Al mapear dónde y cómo se activa VSIR en distintos cánceres hematológicos, y cómo esto se relaciona con los resultados y la respuesta al tratamiento, los investigadores señalan nuevas formas de emparejar a los pacientes con la inmunoterapia y diseñar combinaciones de fármacos más inteligentes.
Dónde aparece este freno inmune en el organismo
El equipo planteó primero una pregunta básica: en personas sanas, ¿qué células llevan normalmente este freno inmune? Analizando grandes conjuntos públicos de datos de actividad génica de miles de muestras, encontraron que VSIR es más activo en los glóbulos blancos de la familia mieloide, como neutrófilos y monocitos, y mucho menos activo en muchos otros tejidos. Al observar docenas de tipos de cáncer, emergió un patrón llamativo: entre todos los cánceres, la leucemia mieloide aguda (LMA) mostró el aumento más marcado de VSIR, con otras neoplasias mieloides sanguíneas también elevadas, mientras que la mayoría de los tumores sólidos presentaron niveles más bajos o incluso reducidos. Esto distingue a la LMA como una enfermedad en la que el freno VISTA podría ser especialmente relevante.
Cómo las células cancerosas reajustan el gen VSIR
A continuación, los investigadores quisieron saber qué impulsa realmente este aumento anómalo. Hallaron que las mutaciones clásicas en el ADN de VSIR son raras y no pueden explicar el cambio. En su lugar, los culpables principales son cambios epigenéticos: etiquetas químicas y complejos proteicos que controlan cómo se empaqueta el ADN y si los genes son accesibles. En la LMA y los trastornos hematológicos relacionados, regiones de control clave próximas a VSIR pierden grupos metilo, un tipo de marca química que normalmente mantiene los genes silenciados. Esta pérdida de metilación se confirmó en varias cohortes de pacientes y en un conjunto dedicado de 168 muestras clínicas, mostrando una caída escalonada desde médula ósea sana, pasando por síndromes mielodisplásicos, hasta LMA franca. A medida que la metilación caía, la actividad de VSIR aumentaba, vinculando este cambio epigenético directamente con la sobreactivación del gen.
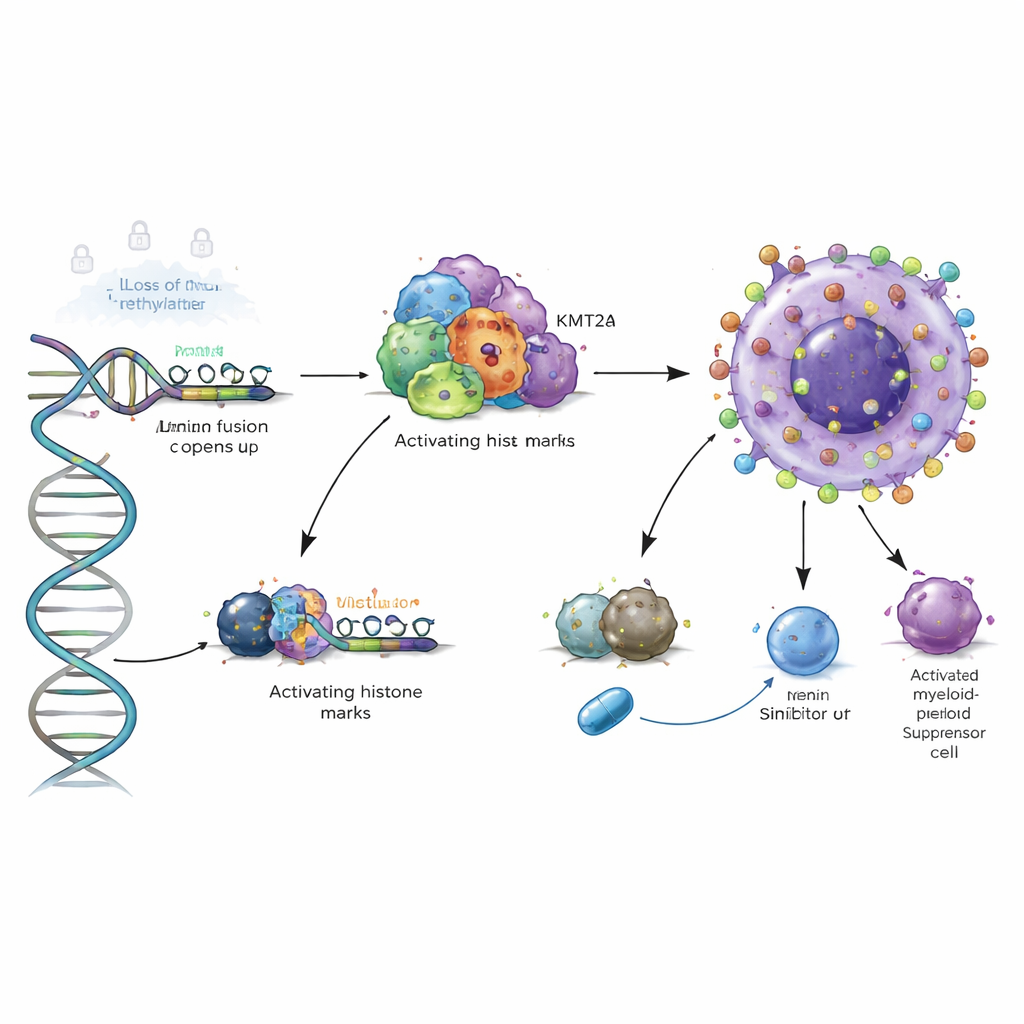
Un potente interruptor de cromatina en leucemias de alto riesgo
El estudio profundizó un nivel más al examinar los andamiajes proteicos 3D que se sitúan sobre el ADN. En los tipos de LMA de alto riesgo que portan reordenamientos del gen KMT2A o mutaciones en NPM1, los autores demostraron que las proteínas de fusión y su cofactor Menin se unen directamente a la región de control de VSIR, incorporando marcas de histonas “activadoras” que abren la cromatina local. Bloquear Menin con fármacos experimentales en modelos celulares redujo estas marcas y disminuyó los niveles de VSIR, y degradar la NPM1 mutante tuvo un efecto similar. Esto significa que VSIR no está activado de forma incidental en estas leucemias peligrosas; está integrado directamente en un programa cromatínico oncogénico que potencialmente puede apagarse con inhibidores dirigidos.
Qué significa VSIR para el vecindario inmunitario del tumor
Puesto que VISTA actúa sobre células inmunitarias, los autores estudiaron cómo los niveles de VSIR se correlacionan con el microambiente tumoral. Utilizando datos tanto bulk como de célula única de numerosos cánceres sanguíneos, encontraron que VSIR se concentra en monocitos y macrófagos, y también está presente en algunas células T citotóxicas y células NK. Los tumores con alta expresión de VSIR tendían a mostrar firmas fuertes de actividad inmune e inflamación, pero el equilibrio entre respuestas útiles y perjudiciales difería según la enfermedad. En la LMA, VSIR se vinculó a células y vías que suprimen el ataque de las células T, coherente con un nicho leucémico evasivo al sistema inmune. En contraste, en algunos cánceres linfoides, VSIR elevado apareció junto a rasgos de vigilancia inmune más efectiva.
Predecir quién se beneficia de la inmunoterapia
El equipo preguntó luego si VSIR podría indicar qué pacientes responderían mejor a los fármacos inhibidores de puntos de control inmunitario. Usando una herramienta computacional que predice la respuesta a la inmunoterapia y datos del mundo real de pacientes con melanoma y cáncer de páncreas, encontraron que los tumores con mayor expresión de VSIR tenían más probabilidades de responder y que esos pacientes vivieron más. En los cánceres sanguíneos, los modelos predijeron que los pacientes con VSIR alto en LMA, síndromes mielodisplásicos, mieloma y varias leucemias podrían beneficiarse de forma particular del bloqueo de puntos de control, aunque esto aún requiere pruebas clínicas directas. Curiosamente, el impacto de VSIR sobre la supervivencia fue específico de la enfermedad: en LMA, mayor VSIR marcó peores resultados incluso tras ajustar por otros factores de riesgo, mientras que en el linfoma difuso de células B grandes y en el mieloma se asoció con mejor supervivencia.
Cómo podrían cambiar la atención estos hallazgos
En conjunto, el trabajo presenta a VSIR como un freno inmune finamente regulado que es secuestrado en ciertos cánceres hematológicos mediante dos vías principales: pérdida de metilación del ADN y activación directa por complejos de cromatina que contienen Menin. En la LMA agresiva, esto ayuda a las células leucémicas a protegerse del ataque inmune y marca a pacientes con mayor riesgo, pero al mismo tiempo puede señalar a aquellos cuyos tumores están predispuestos a responder a la inmunoterapia. El estudio sugiere que combinar inhibidores de Menin con fármacos que bloqueen VISTA podría ser una estrategia prometedora, especialmente en LMA con reordenamientos de KMT2A y mutaciones de NPM1. Más ampliamente, medir VSIR podría ayudar a los médicos a adaptar los tratamientos basados en el sistema inmune a la biología específica de cada cáncer de la sangre.
Cita: Xu, Zj., Wu, Xm., Chang, R. et al. Comprehensive characterization of VSIR reveals dual epigenetic regulation and immune landscape across hematological malignancies. Sci Rep 16, 11556 (2026). https://doi.org/10.1038/s41598-026-41978-2
Palabras clave: Punto de control inmune VISTA, leucemia mieloide aguda, regulación epigenética, Menin KMT2A NPM1, inmunoterapia contra el cáncer