Clear Sky Science · tr
Acı tadı reseptörleri T2R14 ve T2R46'nın ligand bağlanma modları
Acılığın dilin ötesinde neden önemi var
Çoğumuz acı tatları yiyecek veya içeceklerden uzak durulması gereken şeyler olarak düşünürüz, fakat kahve ya da tonic suyun keskin tadını veren aynı sensörler, vücut genelinde dağılmış halde bulunur ve metabolizma, iltihaplanma ve hatta kanseri etkiler. Bu çalışma, T2R14 ve T2R46 adı verilen en geniş kapsamlı iki “acı algılayıcısı”na odaklanıyor ve çok farklı acı molekülleri atomik ayrıntıda nasıl tanıdıklarını gösteriyor. Bu bileşiklerin reseptörlerde nerelere yerleştiğini ve hücre içinde bir sinyali nasıl tetiklediklerini ortaya koyarak, şans eseri keşiflere bel bağlamadan vücudun acılık devresine yönelik yeni ilaçlar tasarlama olanağı açıyor.
Acı kimyasallar için iki çok yönlü nöbetçi
İnsanların bilinen 25 acı tat reseptörü vardır, ancak T2R14 ve T2R46 bitkisel bileşikler ve ilaçlar açısından özellikle geniş bir yelpazeye yanıt verdikleri için öne çıkar. Bu reseptörler yalnızca dilde bulunmaz; bağırsak, kan damarları, yağ dokusu ve hava yollarında da yer alırlar ve kolesterol, iltihap, obezite ve tümör büyümesini düzenlemeye yardımcı olurlar. Buna rağmen ilaç geliştiriciler bunları hedeflemek konusunda zorlandı çünkü doğal ligandları genellikle zayıf bağlanır ve seçicilikleri düşüktür. Bu sorunu ele almak için yazarlar, T2R14 ve T2R46'nın yedi üç boyutlu yüksek çözünürlüklü yapısını belirlemek üzere kriyo-elektron mikroskopisi kullandılar; yapılar ya boş ya da farklı acı moleküllere bağlı olarak, hücre içindeki bir G proteini aracılığıyla sinyal iletirken yakalandı.
Bir reseptör, acı moleküller için iki kapı
İlk sürpriz T2R14'ten geldi; bu reseptörün ligandları için iki ayrı demirleme bölgesi kullandığı ortaya çıktı. Önceki çalışmalar hücrenin iç kısmına daha yakın bir iç site olduğunu önermişti, ancak yeni yapılar birçok iyi bilinen bitkisel bileşiğinin—örneğin narenciye flavonu tangeretin ve antiseptik klorheksidin—aslında hücrenin dışına açık daha büyük bir cebe yerleştiğini gösteriyor. Bu dış cep hacimli, genellikle yüksüz veya pozitif yüklü, hacimli molekülleri barındırabilirken; daha küçük iç cep kompakt, negatif yüklü asitleri tercih ediyor. 385 bilinen T2R14 aktivatörünün bilgisayar destekli dokingi, yaklaşık %90'ının dış cebi tercih ettiğini, yalnızca belirli küçük asidik veya fenilpropanoid moleküllerin iç cep’i tercih ettiğini gösterdi. Bu çift girişli sistem, T2R14'ün yüzlerce çok farklı acı maddeyi tanıyabilmesini açıklamaya yardımcı oluyor.
İki reseptör, aynı ligand, çok farklı uyumlar
Çalışma daha sonra aynı bileşik olan tangeretinin T2R14 ve T2R46'ya nasıl bağlandığını karşılaştırdı. Her iki reseptör de bu narenciye molekülünü algılasa da yapıların gösterdiği üzere tangeretin T2R14 içinde dik dururken T2R46'da yaklaşık 90 derece döndürülmüş şekilde yatar. Bu dramatik yeniden yönlenme, dıştaki helikslerin özellikle VII. heliks adı verilen bir segmentinin konumunda ve bağlanma cebini döşeyen aminoasitlerdeki ince farklılıklardan kaynaklanıyor. T2R14, tangeretinin bir ucunu kavramak için cep girişinde hantal, yağlı bir residü kümesini kullanırken; T2R46 daha klasik, merkezde konumlanmış bir cebe dayanır; burada yüksek ölçüde korunmuş tek bir triptofan bir merkez görevi görür ve tangeretin yanı sıra striknin, artemisinin ve denatoniyum gibi alakasız birkaç ligandın çekirdeği ile istiflenir. Bu anahtar residülerin mutasyonu reseptör aktivasyonunu belirgin şekilde azalttı ve farklı düzenlemelerin her reseptörün ligandlarını nasıl seçtiği ve onlara nasıl yanıt verdiği için elzem olduğunu doğruladı.
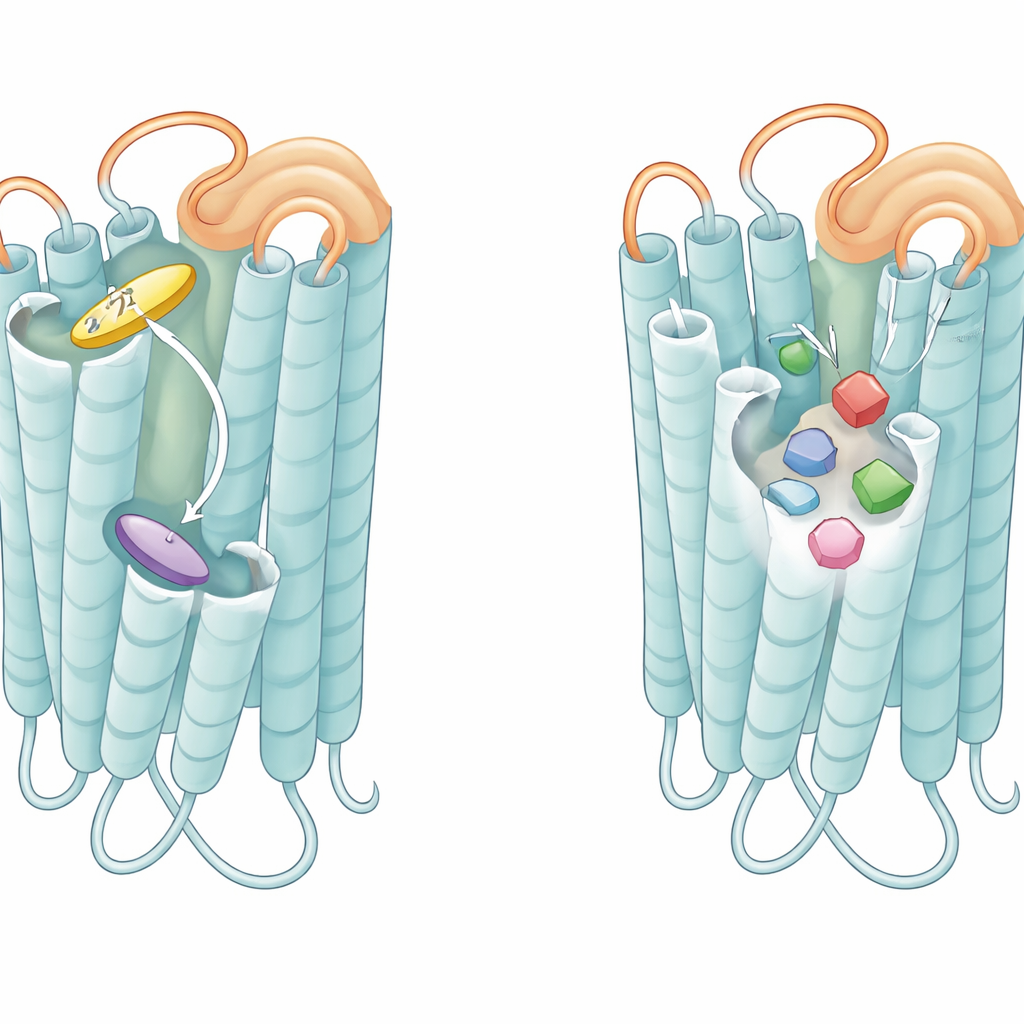
Döngüler ve cepler acı duyarlılığını nasıl ayarlıyor
Cebe ek olarak, her reseptörün dış yüzü üzerinde sarkan esnek döngü, yani ikinci ekstraselüler döngü, kritik bir oyuncu olarak ortaya çıktı. T2R46'da herhangi bir tatlandırıcı bağlanmadığında bu döngü cebe doğru katlanır ve bir ligandı taklit ederek gerçek acı moleküllerinin kullandığı aynı triptofana karşı istiflenir. Bu döngüden kopyalanan peptitler reseptörü tek başlarına aktive edebildi ve döngü residülerinin değiştirilmesi reseptörün arka plan aktivitesini ve zayıf agonistlere yanıtını azalttı. T2R14'ün döngüsünden türetilmiş benzer bir peptit T2R14'ü güçlü şekilde aktive etti ve daha az ölçüde T2R46'yı da aktive etti. Bu bulgular döngünün, reseptörü zayıf bağlanan acı bileşiklere bile hızla yanıt vermeye hazır, ön-uyarılmış bir durumda tutan dahili, bağlı bir mini-agonist gibi davrandığını öne sürüyor.
Gelecek ilaçlar için anlamı
Farklı acı bileşiklerin T2R14 ve T2R46 içinde tam olarak nasıl yerleştiğini ve zayıf bağlanmaya rağmen nasıl açıldıklarını haritalandırarak bu çalışma rasyonel ilaç tasarımı için bir kroki sunuyor. T2R14 için kimyagerler ya geniş dış cep’e ya da daha sıkı iç cep’e yönelebilir; böylece seçicilik ve yük tercihleri ayarlanabilir. T2R46 için ise korunan merkezi cep ve esnek döngüyle etkileşimi, geniş ve kaba acı ilaçlar yerine daha hassas araçlar gibi davranacak ligandlar tasarlamak için stabil bir çerçeve sunuyor. Bu reseptörler dilin çok ötesinde metabolizma, iltihap ve kanseri etkilediğinden, böyle hedeflenmiş moleküller bir gün yemeğin tadını zorunlu olarak değiştirmeden acı algılama mekanizmamızı hastalık tedavisinde kullanabilir.
Atıf: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Anahtar kelimeler: acı tat reseptörleri, T2R14, T2R46, ligand bağlanması, ilaç keşfi