Clear Sky Science · fr
Modes de liaison des ligands des récepteurs du goût amer T2R14 et T2R46
Pourquoi l'amertume importe au-delà de la langue
La plupart d'entre nous associent les saveurs amères à quelque chose à éviter dans la nourriture ou la boisson, mais les mêmes capteurs qui rendent le café ou le tonic âpre sont aussi disséminés dans l'organisme, où ils influencent le métabolisme, l'inflammation et même le cancer. Cette étude se concentre sur deux des détecteurs d'amertume les plus polyvalents, appelés T2R14 et T2R46, et montre en détail atomique comment ils reconnaissent des molécules amères très différentes. En révélant où ces composés se lient sur les récepteurs et comment cela déclenche un signal à l'intérieur des cellules, ce travail ouvre la voie à la conception de nouveaux médicaments qui exploitent le circuit de l'amertume de l'organisme sans dépendre de découvertes fortuites.
Deux sentinelles polyvalentes pour les composés amers
L'humain possède 25 récepteurs du goût amer connus, mais T2R14 et T2R46 se distinguent parce qu'ils répondent à une gamme particulièrement large de composés végétaux et de médicaments. Ces récepteurs ne se trouvent pas seulement sur la langue ; on les trouve aussi dans l'intestin, les vaisseaux sanguins, le tissu adipeux et les voies respiratoires, où ils contribuent à réguler le cholestérol, l'inflammation, l'obésité et la croissance tumorale. Pourtant, les développeurs de médicaments ont eu du mal à les cibler car leurs ligands naturels ont tendance à se lier faiblement et avec peu de sélectivité. Pour relever ce défi, les auteurs ont utilisé la cryo‑microscopie électronique à haute résolution pour déterminer sept structures tridimensionnelles de T2R14 et T2R46, soit vides, soit liées à différents molécules amères, toutes prises en action en train de signaler via une protéine G à l'intérieur de la cellule.
Un récepteur, deux portes pour les molécules amères
La première surprise est venue de T2R14, qui s'est avéré utiliser deux zones d'ancrage distinctes pour ses ligands. Des travaux antérieurs avaient suggéré un site interne plus proche de l'intérieur cellulaire, mais les nouvelles structures montrent que beaucoup de ses composés végétaux les plus connus, comme la flavone d'agrumes tangerétine et l'antiseptique chlorhexidine, se logent en réalité dans une poche plus large ouverte vers l'extérieur de la cellule. Cette poche externe peut accueillir des molécules volumineuses, souvent non chargées ou chargées positivement, tandis qu'une poche interne plus petite favorise les acides compacts et chargés négativement. Le docking informatique de 385 activateurs connus de T2R14 a montré qu'environ 90 % préfèrent la poche externe, tandis que seules certaines petites molécules acides ou des phénylpropanoïdes privilégient l'emplacement interne. Ce système à double entrée aide à expliquer pourquoi T2R14 peut reconnaître des centaines de substances amères très différentes.
Deux récepteurs, un ligand, des ajustements très différents
L'étude a ensuite comparé comment le même composé, la tangerétine, se lie à T2R14 et à T2R46. Bien que les deux récepteurs détectent cette molécule d'agrumes, les structures révèlent que la tangerétine est dressée dans T2R14 mais couchée dans T2R46, pivotée d'environ 90 degrés. Cette réorientation spectaculaire est due à des différences subtiles dans le positionnement des hélices les plus externes, en particulier un segment appelé hélice VII, et aux acides aminés qui bordent la poche de liaison. T2R14 utilise un groupe de résidus volumineux et apolaires à l'entrée de la poche pour agripper une extrémité de la tangerétine, tandis que T2R46 repose sur une poche centrale plus classique où un tryptophane fortement conservé joue le rôle de noyau, s'empilant contre le cœur de plusieurs ligands non apparentés, y compris la tangerétine, la strychnine, l'artémisinine et le dénatonium. La mutation de ces résidus clés réduit fortement l'activation du récepteur, confirmant que ces arrangements distincts sont essentiels à la manière dont chaque récepteur choisit et répond à ses ligands.
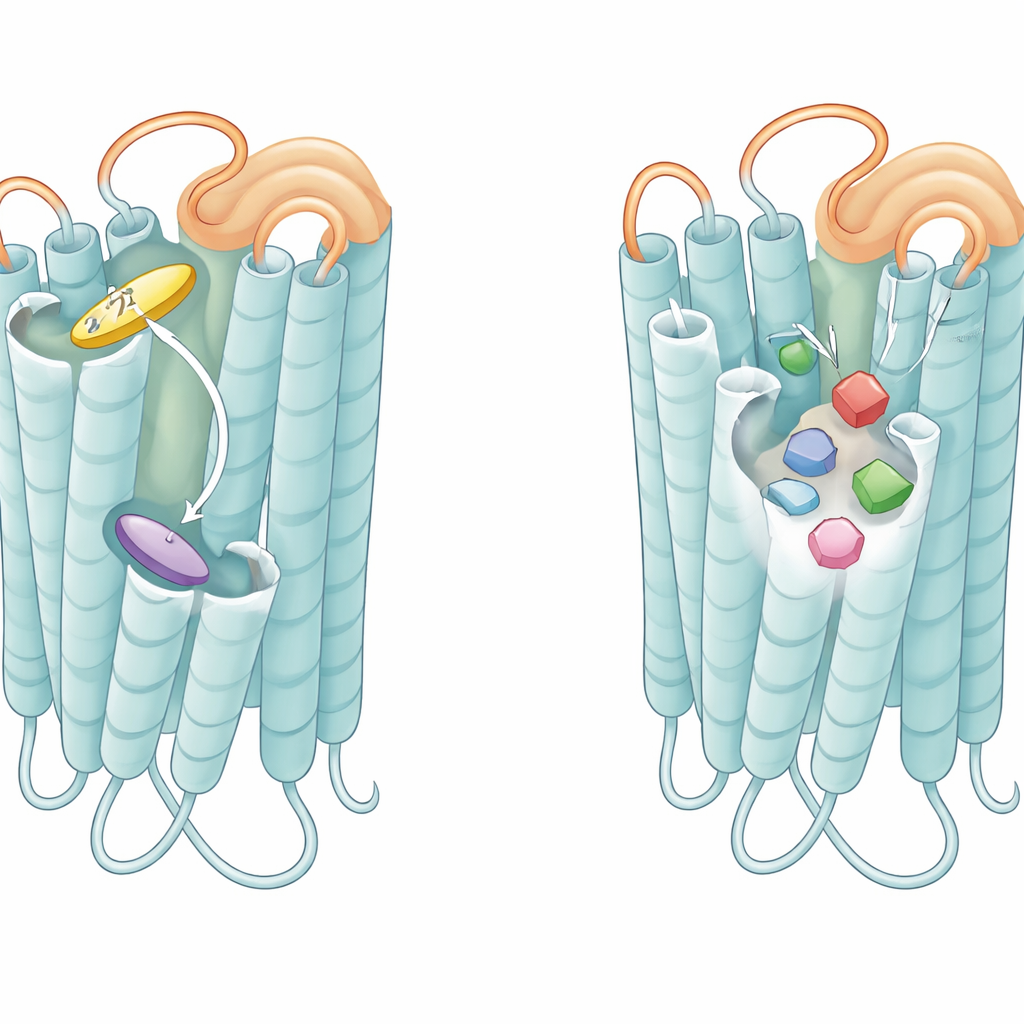
Comment les boucles et les poches ajustent la sensibilité à l'amertume
Au-delà des poches elles‑mêmes, la boucle flexible qui surplombe la face externe de chaque récepteur, connue sous le nom de deuxième boucle extracellulaire, s'est imposée comme un élément crucial. Dans T2R46, quand aucun tastant n'est lié, cette boucle se replie dans la poche et imite un ligand, s'empilant contre le même tryptophane que les vraies molécules amères utilisent. Des peptides copiés de cette boucle pouvaient activer le récepteur à eux seuls, et modifier les résidus de la boucle réduisait l'activité de fond du récepteur ainsi que sa réponse aux faibles agonistes. Un peptide similaire dérivé de la boucle de T2R14 activait fortement T2R14 et, dans une moindre mesure, T2R46. Ces résultats suggèrent que la boucle agit comme un mini‑agoniste intégré et ancré qui maintient le récepteur dans un état de pré‑alerte, prêt à répondre rapidement même à des composés amers de faible affinité.
Ce que cela signifie pour les médicaments à venir
En cartographiant précisément comment différents composés amers s'imbriquent dans T2R14 et T2R46, et comment une boucle intégrée les aide à s'activer malgré une liaison faible, ce travail fournit une feuille de route pour la conception rationnelle de médicaments. Pour T2R14, les chimistes peuvent viser soit la vaste poche externe, soit la poche interne plus étroite pour ajuster la sélectivité et les préférences de charge. Pour T2R46, la poche centrale conservée et son interaction avec la boucle flexible offrent un cadre stable pour concevoir des ligands qui agissent davantage comme des outils précis que comme des médicaments globalement amers. Parce que ces récepteurs influencent le métabolisme, l'inflammation et le cancer loin de la langue, de telles molécules ciblées pourraient un jour exploiter notre machinerie de détection de l'amertume pour traiter des maladies—sans nécessairement modifier le goût du repas.
Citation: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Mots-clés: récepteurs du goût amer, T2R14, T2R46, liaison des ligands, découverte de médicaments