Clear Sky Science · pl
Tryby wiązania ligandów receptorów smaku gorzkiego T2R14 i T2R46
Dlaczego gorzkość ma znaczenie poza językiem
Większość z nas myśli o gorzkich smakach jako o czymś, czego należy unikać w jedzeniu czy napojach, ale te same sensory, które sprawiają, że kawa czy tonik są ostre, są rozproszone w całym organizmie i wpływają na metabolizm, stany zapalne, a nawet nowotwory. Badanie koncentruje się na dwóch z najszerszych „detektorów gorzkości”, nazwanych T2R14 i T2R46, i pokazuje w skali atomowej, jak rozpoznają bardzo różne gorzkie cząsteczki. Odkrywając, gdzie te związki osiadają na receptorach i jak to wyzwala sygnał wewnątrz komórek, praca otwiera drogę do projektowania nowych leków wykorzystujących obwody gorzkiego smaku w organizmie bez polegania na przypadkowych odkryciach.
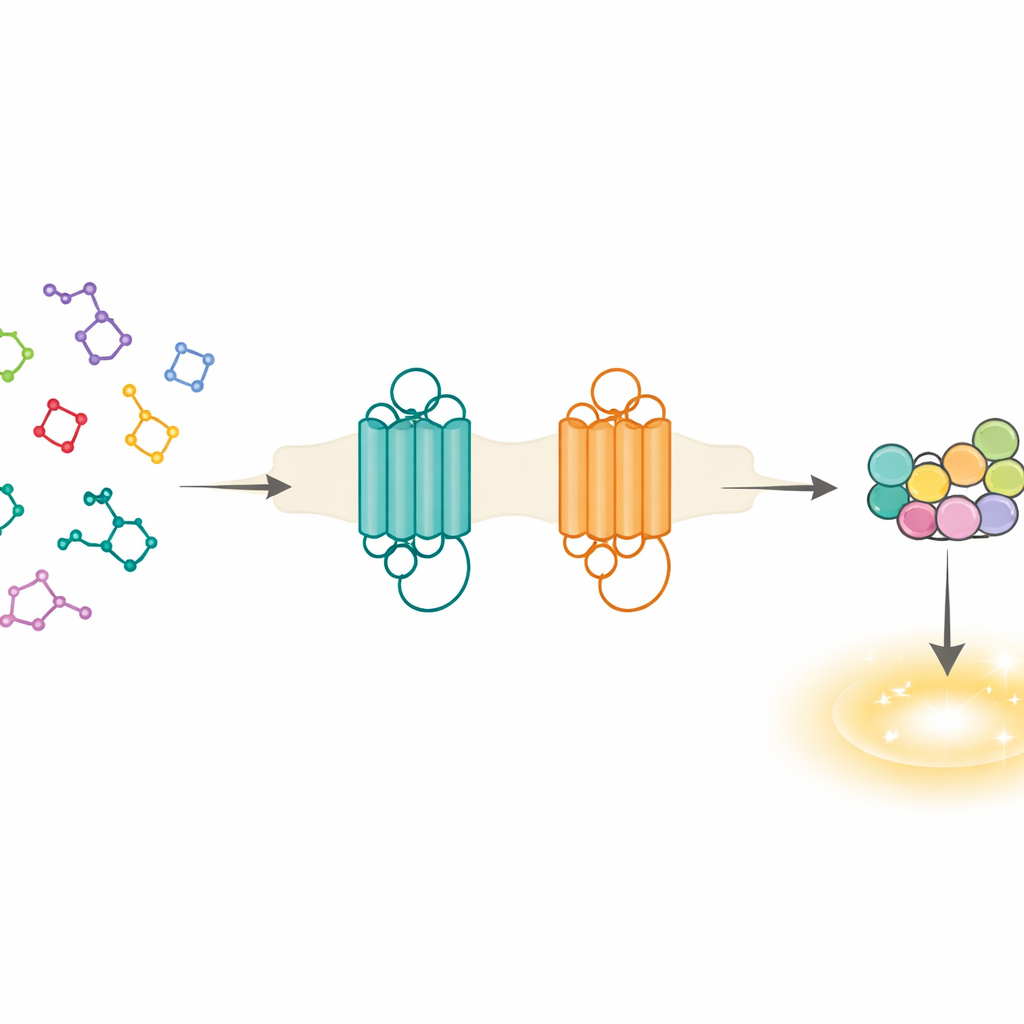
Dwaj wszechstronni strażnicy chemikaliów gorzkich
Ludzie mają 25 poznanych receptorów smaku gorzkiego, ale T2R14 i T2R46 wyróżniają się tym, że reagują na wyjątkowo szeroki zakres związków roślinnych i leków. Receptory te nie występują tylko na języku; znajdują się także w jelitach, naczyniach krwionośnych, tkance tłuszczowej i drogach oddechowych, gdzie pomagają regulować cholesterol, stany zapalne, otyłość i wzrost guzów. Jednak twórcy leków mieli trudności z ich ukierunkowaniem, ponieważ ich naturalne ligandów zwykle wiążą się słabo i z niską selektywnością. Aby sprostać temu problemowi, autorzy użyli wysokorozdzielczej krioelektronowej mikroskopii, by określić siedem struktur trójwymiarowych T2R14 i T2R46, zarówno pustych, jak i związanych z różnymi gorzkimi cząsteczkami, wszystkie w trakcie przekazywania sygnału przez białko G wewnątrz komórki.
Jeden receptor, dwa wejścia dla gorzkich cząsteczek
Pierwszym zaskoczeniem był T2R14, który okazał się używać dwóch oddzielnych miejsc dokujących dla swoich ligandów. Wcześniejsze prace sugerowały miejsce wewnętrzne bliżej wnętrza komórki, ale nowe struktury pokazują, że wiele z jego najlepiej poznanych związków roślinnych, takich jak cytrusowy flawon tangeretyna i środek antyseptyczny chlorheksydyna, osiada w większej kieszeni otwartej na zewnątrz komórki. Ta zewnętrzna kieszeń może mieścić masywne, często niejonowe lub dodatnio naładowane cząsteczki, podczas gdy mniejsza wewnętrzna preferuje zwarte, ujemnie naładowane kwasy. Obliczeniowe dokowanie 385 znanych aktywatorów T2R14 wykazało, że około 90% woli kieszeń zewnętrzną, podczas gdy tylko niektóre małe kwasowe lub fenylopropanoidowe cząsteczki wybierają wewnętrzną. Ten system z dwoma wejściami pomaga wyjaśnić, dlaczego T2R14 rozpoznaje setki bardzo różnych gorzkich substancji.
Dwa receptory, jeden ligand, bardzo odmienne dopasowania
Następnie badanie porównało, jak ta sama cząsteczka, tangeretyna, wiąże się z T2R14 i T2R46. Chociaż oba receptory wykrywają tę cytrusową cząsteczkę, struktury ujawniają, że tangeretyna siedzi pionowo w T2R14, lecz leży bokiem w T2R46, obrócona o około 90 stopni. Ta dramatyczna reorientacja jest spowodowana subtelnymi różnicami w położeniu najbardziej zewnętrznych helis, zwłaszcza segmentu zwanego helisą VII, oraz przez to, które aminokwasy wyściełają kieszeń wiążącą. T2R14 używa skupiska masywnych, lipofilowych reszt przy wejściu do kieszeni, by chwycić jeden koniec tangeretyny, podczas gdy T2R46 polega na bardziej klasycznej, centralnie umieszczonej kieszeni, w której pojedynczy wysoko konserwowany tryptofan działa jak oś, układając się w stos względem rdzenia kilku niespokrewnionych ligandów, w tym tangeretyny, strychniny, artemizyniny i denatonium. Zmiany (mutacje) tych kluczowych reszt znacznie zmniejszały aktywację receptora, potwierdzając, że różne układy są niezbędne dla tego, jak każdy receptor wybiera i reaguje na swoje ligandy.
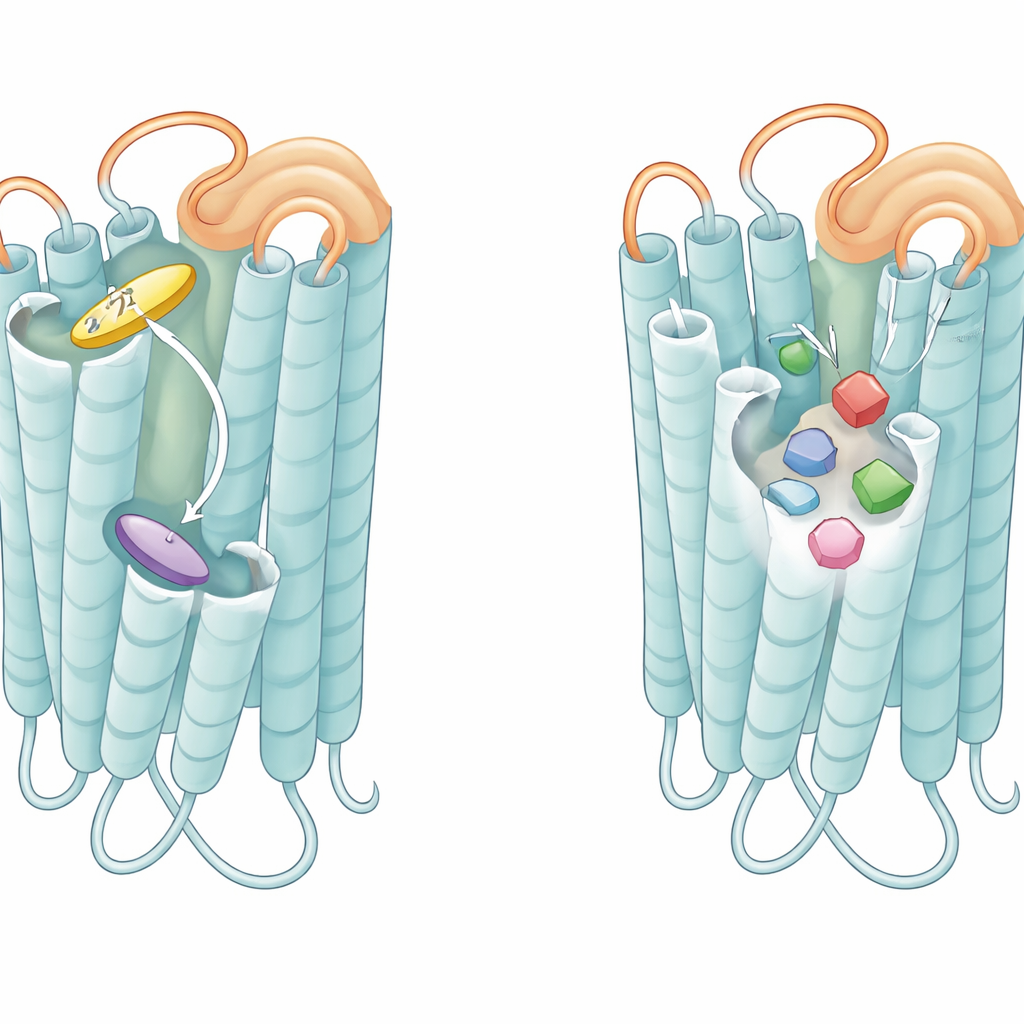
Jak pętle i kieszenie dostrajają czułość na gorzkość
Ponad same kieszenie, elastyczna pętla zwisająca nad zewnętrzną powierzchnią każdego receptora, znana jako druga pętla zewnątrzkomórkowa, okazała się kluczowym graczem. W T2R46, gdy żaden tastant nie jest związany, ta pętla składa się do wnętrza kieszeni i naśladuje ligand, układając się w stos względem tego samego tryptofanu, którego używają prawdziwe gorzkie cząsteczki. Peptydy skopiowane z tej pętli same mogły aktywować receptor, a zmiany reszt pętli zmniejszały aktywność tła receptora i jego odpowiedź na słabe agonisty. Podobny peptyd pochodzący z pętli T2R14 silnie aktywował T2R14 i, w mniejszym stopniu, T2R46. Te odkrycia sugerują, że pętla zachowuje się jak wbudowany, przytwierdzony mini-agonista, który utrzymuje receptor w stanie półgotowości, gotowym odpowiedzieć szybko nawet na niskodoaffinityjne gorzkie związki.
Co to oznacza dla przyszłych leków
Mapując dokładnie, jak różne gorzkie związki mieszczą się w T2R14 i T2R46 oraz jak wbudowana pętla pomaga im włączać receptor mimo słabego wiązania, ta praca dostarcza planu dla racjonalnego projektowania leków. Dla T2R14 chemicy mogą celować w przestronną zewnętrzną kieszeń lub węższą wewnętrzną, aby dostosować selektywność i preferencje ładunkowe. Dla T2R46 konserwowana kieszeń centralna i jej interakcja z elastyczną pętlą oferują stabilne ramy do projektowania ligandów, które działają bardziej jak precyzyjne narzędzia niż tępe, szeroko gorzkie związki. Ponieważ te receptory wpływają na metabolizm, stany zapalne i nowotwory daleko od języka, takie ukierunkowane molekuły mogłyby pewnego dnia wykorzystać nasz mechanizm wykrywania gorzkości do leczenia chorób — bez konieczności zmieniania smaku potraw.
Cytowanie: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Słowa kluczowe: receptory smaku gorzkiego, T2R14, T2R46, wiązanie ligandów, poszukiwanie leków