Clear Sky Science · it
Modalità di legame dei ligandi dei recettori del gusto amaro T2R14 e T2R46
Perché l’amarezza conta oltre la lingua
La maggior parte di noi pensa ai sapori amari come a qualcosa da evitare nel cibo o nelle bevande, ma gli stessi sensori che rendono il caffè o l’acqua tonica taglienti sono distribuiti in tutto il corpo, dove influenzano il metabolismo, l’infiammazione e persino il cancro. Questo studio si concentra su due dei “rilevatori di amarezza” più ampi, chiamati T2R14 e T2R46, e mostra in dettaglio atomico come riconoscano molecole amare molto diverse. Rivelando dove questi composti si posano sui recettori e come ciò innesca un segnale all’interno delle cellule, il lavoro apre la strada alla progettazione di nuovi farmaci che sfruttino i circuiti dell’amarezza del corpo senza fare affidamento su scoperte casuali.
Due sentinelle versatili per i composti amari
Gli esseri umani possiedono 25 recettori del gusto amaro noti, ma T2R14 e T2R46 si distinguono perché rispondono a una gamma particolarmente ampia di composti vegetali e farmaci. Questi recettori non si trovano solo sulla lingua; sono presenti anche nell’intestino, nei vasi sanguigni, nel tessuto adiposo e nelle vie aeree, dove aiutano a regolare colesterolo, infiammazione, obesità e crescita tumorale. Tuttavia, gli sviluppatori di farmaci hanno faticato a mirarli perché i loro ligandi naturali tendono a legarsi debolmente e con scarsa selettività. Per affrontare questo problema, gli autori hanno utilizzato la crio–microscopia elettronica ad alta risoluzione per determinare sette strutture tridimensionali di T2R14 e T2R46, sia vuote sia legate a diversi composti amari, tutte catturate nell’atto di segnalare attraverso una proteina G all’interno della cellula.
Un recettore, due porte per le molecole amare
La prima sorpresa è arrivata da T2R14, che si è rivelato usare due aree di ancoraggio separate per i suoi ligandi. Lavori precedenti avevano suggerito un sito interno più vicino all’interno cellulare, ma le nuove strutture mostrano che molti dei suoi composti vegetali più noti, come la flavone agrumaria tangeretina e l’antiseptico clorexidina, si sistemano in realtà in una tasca più ampia aperta verso l’esterno della cellula. Questa tasca esterna può accogliere molecole voluminose, spesso neutre o cariche positivamente, mentre una tasca interna più piccola favorisce acidi compatti e carichi negativamente. Il docking computazionale di 385 attivatori noti di T2R14 ha mostrato che circa il 90% preferisce la tasca esterna, mentre solo certe piccole molecole acide o fenilpropanoidi favoriscono quella interna. Questo sistema a doppio ingresso aiuta a spiegare perché T2R14 può riconoscere centinaia di sostanze amare molto diverse tra loro.
Due recettori, un ligando, adattamenti molto diversi
Lo studio ha quindi confrontato come lo stesso composto, la tangeretina, si lega a T2R14 e T2R46. Sebbene entrambi i recettori percepiscano questa molecola agrumaria, le strutture rivelano che la tangeretina sta in posizione verticale in T2R14 ma si dispone lateralmente in T2R46, ruotata di circa 90 gradi. Questa drammatica riorientazione è causata da differenze sottili nel posizionamento delle eliche più esterne, in particolare di un segmento chiamato elica VII, e dagli aminoacidi che rivestono la tasca di legame. T2R14 utilizza un ammasso di residui voluminosi e idrofobici all’ingresso della tasca per afferrare un’estremità della tangeretina, mentre T2R46 si affida a una tasca centrale più classica in cui un singolo triptofano altamente conservato funge da fulcro, impilando contro il nucleo di diversi ligandi non correlati, inclusi tangeretina, stricnina, artemisinina e denatonio. La mutazione di questi residui chiave ha ridotto drasticamente l’attivazione del recettore, confermando che i diversi arrangiamenti sono essenziali per il modo in cui ciascun recettore sceglie e risponde ai propri ligandi.
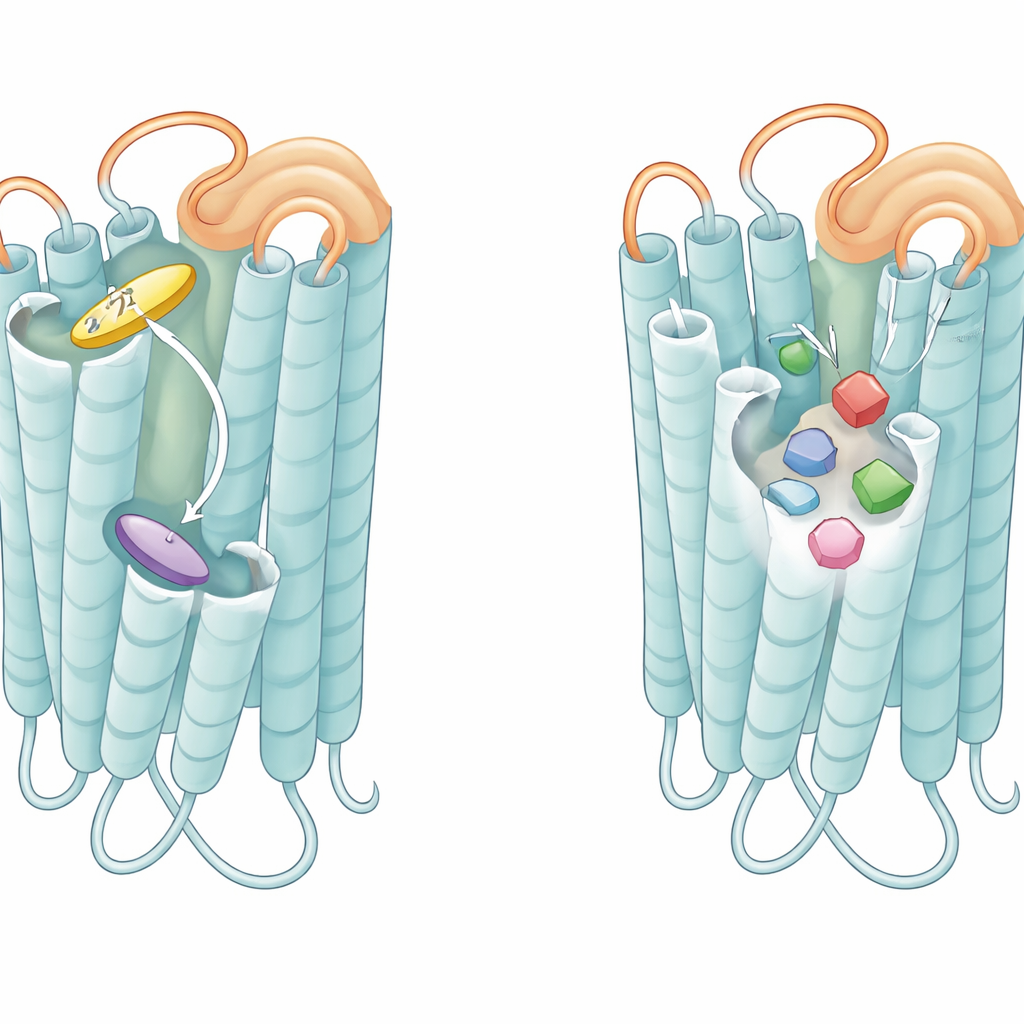
Come anse e tasche sintonizzano la sensibilità all’amaro
Oltre alle tasche stesse, il loop flessibile che pende sulla faccia esterna di ciascun recettore, noto come secondo loop extracellulare, è emerso come un attore cruciale. In T2R46, quando non è legato alcun gustante, questo loop si ripiega dentro la tasca e imita un ligando, impilandosi contro lo stesso triptofano che le vere molecole amare usano. Peptidi copiati da questo loop potevano attivare il recettore autonomamente, e l’alterazione dei residui del loop riduceva l’attività di fondo del recettore e la sua risposta ad agonisti deboli. Un peptide simile derivato dal loop di T2R14 ha fortemente attivato T2R14 e, in misura minore, anche T2R46. Questi risultati suggeriscono che il loop si comporta come un mini-agonista integrato e tetherato che mantiene il recettore in uno stato di pre-allerta, pronto a rispondere rapidamente anche a composti amari a bassa affinità.
Cosa significa per i farmaci del futuro
Mappando esattamente come diversi composti amari si sistemano in T2R14 e T2R46, e come un loop incorporato li aiuta a attivare il recettore nonostante un legame debole, questo lavoro fornisce un progetto per la progettazione razionale di farmaci. Per T2R14, i chimici possono mirare sia alla spaziosa tasca esterna sia a quella interna più stretta per modulare selettività e preferenze di carica. Per T2R46, la tasca centrale conservata e la sua interazione con il loop flessibile offrono una piattaforma stabile per progettare ligandi che agiscano più come strumenti precisi che come farmaci amari ampi e poco selettivi. Poiché questi recettori influenzano metabolismo, infiammazione e cancro lontano dalla lingua, tali molecole mirate potrebbero un giorno sfruttare la nostra macchina sensoriale dell’amaro per trattare le malattie—senza necessariamente cambiare il sapore della cena.
Citazione: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Parole chiave: recettori del gusto amaro, T2R14, T2R46, legame del ligando, scoperta di farmaci