Clear Sky Science · nl
Bindingsmodi van liganden voor de bittere smaakreceptoren T2R14 en T2R46
Waarom bitterheid verder reikt dan de tong
De meesten van ons zien bittere smaken als iets om in voedsel of drinken te vermijden, maar dezelfde sensoren die koffie of tonic scherp doen smaken zitten ook verspreid door het lichaam en beïnvloeden daar stofwisseling, ontsteking en zelfs kanker. Deze studie richt zich op twee van de meest veelzijdige "bittersensors", T2R14 en T2R46, en toont op atomaire schaal hoe ze zeer verschillende bittere moleculen herkennen. Door te laten zien waar deze verbindingen op de receptoren landen en hoe dat een signaal binnenin cellen activeert, opent het werk de deur naar het ontwerpen van nieuwe geneesmiddelen die het bitterheidscircuit van het lichaam benutten zonder afhankelijk te zijn van toevallige ontdekkingen.
Twee veelzijdige wachters voor bittere chemicaliën
Mensen hebben 25 bekende bittere smaakreceptoren, maar T2R14 en T2R46 vallen op omdat ze reageren op een bijzonder breed scala aan plantaardige verbindingen en geneesmiddelen. Deze receptoren zitten niet alleen op de tong; ze komen ook voor in de darm, bloedvaten, vetweefsel en luchtwegen, waar ze helpen bij het reguleren van cholesterol, ontsteking, obesitas en tumorgroei. Toch hebben geneesmiddelontwikkelaars moeite gehad ze te targeten omdat hun natuurlijke liganden vaak zwak en weinig selectief binden. Om dit probleem aan te pakken bepaalden de auteurs met hogeresolutie cryo-elektronenmicroscopie zeven driedimensionale structuren van T2R14 en T2R46, al dan niet gebonden aan verschillende bittere moleculen, allemaal vastgelegd in de act van signalering via een G-eiwit binnen de cel.
Één receptor, twee toegangen voor bittere moleculen
De eerste verrassing kwam van T2R14, dat bleek twee afzonderlijke aanlegplaatsen voor zijn liganden te gebruiken. Eerder werk wees op een interne site dichter bij het celinterieur, maar de nieuwe structuren laten zien dat veel van zijn bekendste plantaardige verbindingen, zoals de citrusflavon tangeretine en het antisepticum chloorhexidine, zich juist nestelen in een grotere pocket die naar de buitenkant van de cel openstaat. Deze buitenste pocket kan volumineuze, vaak ongeladen of positief geladen moleculen herbergen, terwijl een kleinere binnenste pocket compacte, negatief geladen zuren bevoordeelt. Computerdocking van 385 bekende T2R14-activatoren toonde aan dat ongeveer 90% de buitenste pocket verkiest, terwijl alleen bepaalde kleine zure of fenylpropanoïde moleculen de binnenste voorkeur hebben. Dit tweevoudige ingangssysteem helpt verklaren waarom T2R14 honderden zeer verschillende bittere stoffen kan herkennen.
Twee receptoren, één ligand, heel verschillende passen
De studie vergeleek vervolgens hoe dezelfde verbinding, tangeretine, bindt aan T2R14 en T2R46. Hoewel beide receptoren dit citrusmolecuul waarnemen, onthullen de structuren dat tangeretine rechtop staat in T2R14 maar zijwaarts ligt in T2R46, gedraaid met ongeveer 90 graden. Deze dramatische heroriëntatie wordt veroorzaakt door subtiele verschillen in de positie van de buitenste helices, met name een segment dat helix VII wordt genoemd, en door welke aminozuren de bindingspocket bekleden. T2R14 gebruikt een cluster van omvangrijke, hydrofobe residuen bij de ingang van de pocket om het ene uiteinde van tangeretine vast te houden, terwijl T2R46 vertrouwt op een meer klassieke, centraal geplaatste pocket waar een enkele sterk geconserveerde tryptofaan als centrum fungeert en stapelt tegen de kern van meerdere niet-verwante liganden, waaronder tangeretine, strychnine, artemisinine en denatonium. Het muteren van deze sleutelresiduen verminderde receptoractivatie sterk, wat bevestigt dat de verschillende ordeningen essentieel zijn voor hoe elke receptor zijn liganden kiest en erop reageert.
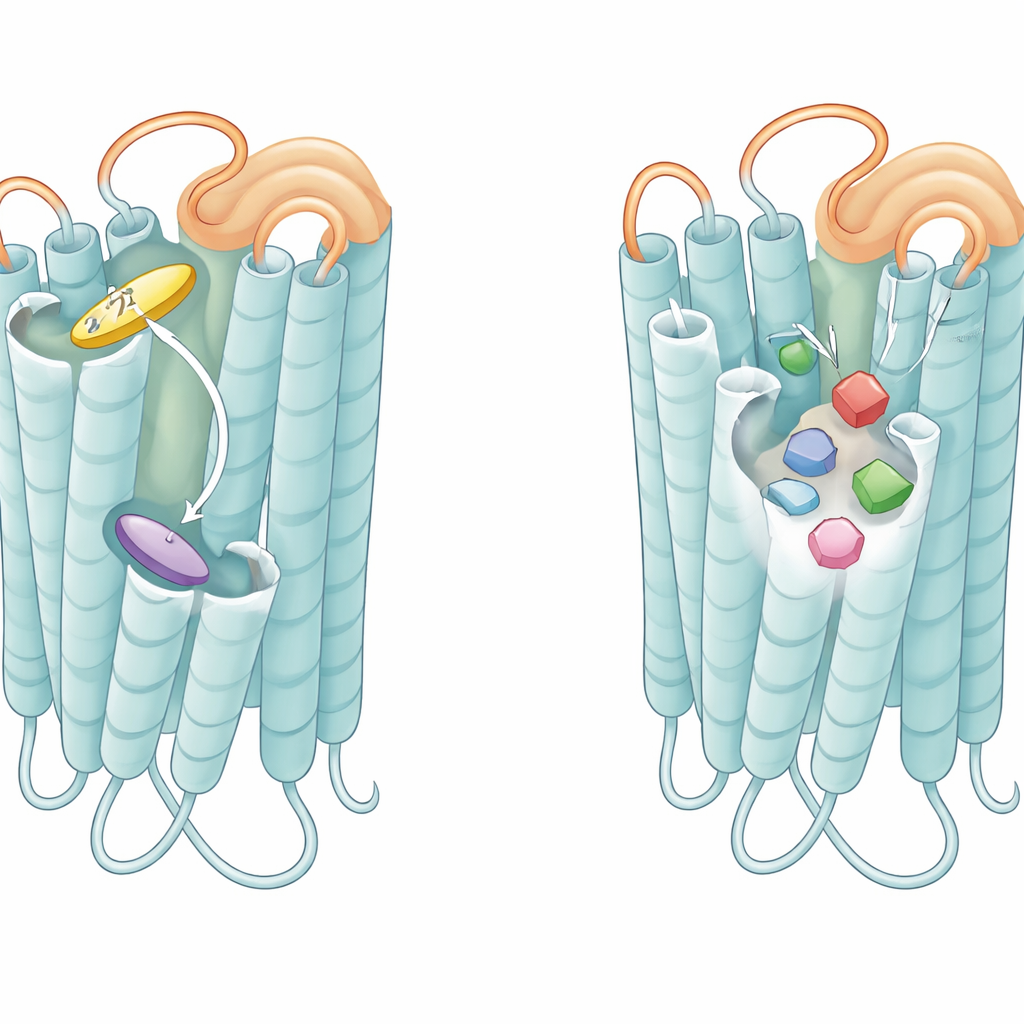
Hoe lussen en pockets de bittergevoeligheid afstemmen
Buiten de pockets zelf kwam de flexibele lus die over de buitenzijde van elke receptor hangt, bekend als de tweede extracellulaire lus, naar voren als een cruciale speler. In T2R46, wanneer geen smaakstof gebonden is, vouwt deze lus naar beneden in de pocket en bootst daarmee een ligand na, door te stapelen tegen dezelfde tryptofaan die echte bittere moleculen gebruiken. Peptiden gebaseerd op deze lus konden de receptor op zichzelf activeren, en het veranderen van lusresiduen verminderde de achtergrondactiviteit van de receptor en zijn respons op zwakke agonisten. Een vergelijkbaar peptide afgeleid van T2R14’s lus activeerde T2R14 sterk en in mindere mate ook T2R46. Deze bevindingen suggereren dat de lus zich gedraagt als een ingebouwde, vastgestelde mini-agonist die de receptor in een voorwaakzame staat houdt, klaar om snel te reageren zelfs op laagaffiniteits bittere verbindingen.
Betekenis voor toekomstige geneesmiddelen
Door precies in kaart te brengen hoe verschillende bittere verbindingen zich in T2R14 en T2R46 nestelen, en hoe een ingebouwde lus hen helpt inschakelen ondanks zwakke binding, levert dit werk een blauwdruk voor rationeel geneesmiddeldesign. Voor T2R14 kunnen chemici zich richten op de ruime buitenste pocket of op de strakkere binnenste om selectiviteit en ladingsvoorkeuren af te stemmen. Voor T2R46 bieden de geconserveerde centrale pocket en de interactie met de flexibele lus een stabiel kader om liganden te ontwerpen die meer als precieze instrumenten werken dan als botte, breed bittere stoffen. Omdat deze receptoren stofwisseling, ontsteking en kanker ver van de tong beïnvloeden, zouden dergelijke gerichte moleculen op termijn ons bitterheidsdetectiesysteem kunnen inzetten om ziekten te behandelen—zonder noodzakelijkerwijs te veranderen hoe het avondeten smaakt.
Bronvermelding: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Trefwoorden: bittersmaakreceptoren, T2R14, T2R46, ligandbinding, geneesmiddelontdekking