Clear Sky Science · sv
Ligandbindningssätt för de bittra smaksensorerna T2R14 och T2R46
Varför bitterhet spelar roll bortom tungan
De flesta av oss ser bittra smaker som något att undvika i mat eller dryck, men samma sensoriska mekanismer som får kaffe eller tonic att smaka skarpt finns också utspridda i kroppen, där de påverkar ämnesomsättning, inflammation och till och med cancer. Denna studie fokuserar på två av de mest mångsidiga ”bitternävarna”, kallade T2R14 och T2R46, och visar på atomnivå hur de känner igen mycket olika bittra molekyler. Genom att avslöja var dessa föreningar landar på receptorerna och hur det utlöser en signal inne i cellerna öppnar arbetet dörren för att designa nya läkemedel som utnyttjar kroppens bitterhetskretsar utan att förlita sig på slumpmässiga upptäckter.
Två mångsidiga väktare för bittra kemikalier
Människan har 25 kända bittra smaksensorer, men T2R14 och T2R46 sticker ut eftersom de svarar på ett särskilt brett spektrum av växtföreningar och läkemedel. Dessa receptorer finns inte bara på tungan; de återfinns också i tarmen, blodkärl, fettvävnad och luftvägar, där de hjälper till att reglera kolesterol, inflammation, fetma och tumörtillväxt. Trots det har läkemedelsutvecklare haft svårt att rikta in sig på dem eftersom deras naturliga ligander tenderar att binda svagt och med dålig selektivitet. För att tackla detta problem använde författarna högupplöst kryo-elektronmikroskopi för att bestämma sju tredimensionella strukturer av T2R14 och T2R46, antingen tomma eller bundna till olika bittra molekyler, alla fångade i stundens allvar då de signalerar genom ett G-protein inne i cellen.
En receptor, två ingångar för bittra molekyler
Den första överraskningen kom från T2R14, som visade sig använda två separata dockningsområden för sina ligander. Tidigare arbete hade föreslagit en intern plats närmare cellens insida, men de nya strukturerna visar att många av dess mest kända växtföreningar, såsom citrusflavonen tangeretin och antiseptikan klorhexidin, faktiskt sätter sig i en större ficka som är öppen mot cellens utsida. Denna yttre ficka kan omfamna stora, ofta oladdade eller positivt laddade molekyler, medan en mindre inre ficka gynnar kompakta, negativt laddade syror. Datorbaserad dockning av 385 kända T2R14-aktivatorer visade att omkring 90 % föredrar den yttre fickan, medan endast vissa små syror eller fenylpropanoidmolekyler favoriserar den inre. Detta dubbla inträdesystem bidrar till att förklara varför T2R14 kan känna igen hundratals mycket olika bittra ämnen.
Två receptorer, en ligand, mycket olika passformer
Studien jämförde sedan hur samma förening, tangeretin, binder till T2R14 respektive T2R46. Även om båda receptorer känner av denna citrusmolekyl visar strukturerna att tangeretin sitter upprätt i T2R14 men ligger på sidan i T2R46, vriden med cirka 90 grader. Denna dramatiska omorientering orsakas av subtila skillnader i hur de yttersta helixarna är positionerade, särskilt ett segment kallat helix VII, och av vilka aminosyror som klär bindningsfickan. T2R14 använder en klunga av stora, fettälskande rester vid fickans ingång för att greppa ena änden av tangeretin, medan T2R46 förlitar sig på en mer klassisk, centralt placerad ficka där en enda högkonserverad tryptofan fungerar som nav och staplar mot kärnan i flera orelaterade ligander, inklusive tangeretin, stryknin, artemisinin och denatonium. Mutationer i dessa nyckelrester minskade starkt receptoraktiveringen, vilket bekräftar att de olika arrangemangen är avgörande för hur varje receptor väljer och svarar på sina ligander.
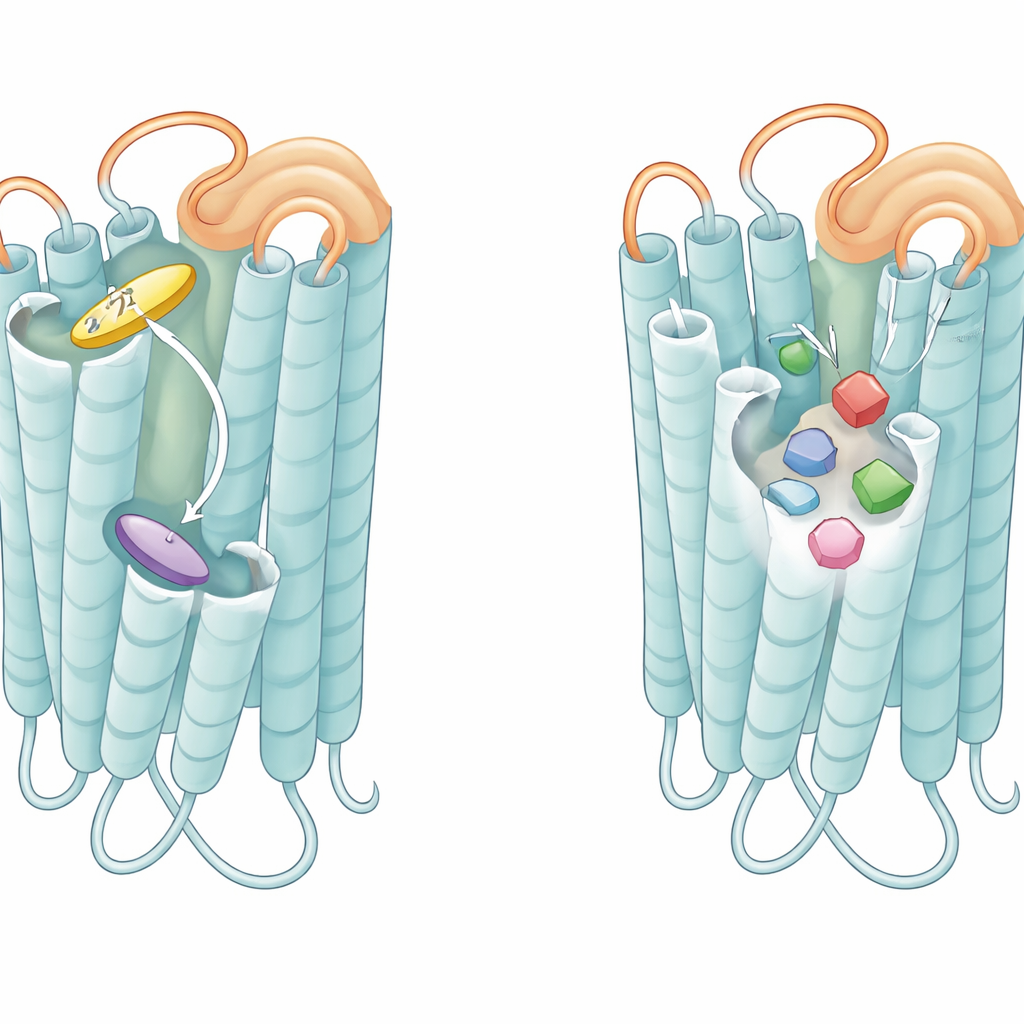
Hur slingor och fickor finjusterar bitterkänsligheten
Bortom själva fickorna framträdde den flexibla slinga som hänger över receptorernas yttre sida, känd som den andra extracellulära loopen, som en avgörande spelare. I T2R46, när ingen smakämne är bundet, viker denna slinga ner i fickan och efterliknar en ligand, staplandes mot samma tryptofan som verkliga bittra molekyler använder. Peptider hämtade från denna slinga kunde själva aktivera receptorn, och att förändra slingans rester minskade receptorernas bakgrundsaktivitet och dess svar på svaga agonister. En liknande peptid härledd från T2R14:s slinga aktiverade starkt T2R14 och, i mindre grad, även T2R46. Dessa fynd tyder på att slingan beter sig som en inbyggd, fäst mini-agonist som håller receptorn i ett förvarningstillstånd, redo att reagera snabbt även på lågaffinitets bittra föreningar.
Vad detta betyder för framtida läkemedel
Genom att kartlägga exakt hur olika bittra föreningar placerar sig i T2R14 och T2R46, och hur en inbyggd slinga hjälper dem att slå på trots svag bindning, ger detta arbete en ritning för rationell läkemedelsdesign. För T2R14 kan kemister sikta antingen på den rymliga yttre fickan eller den snävare inre för att justera selektivitet och laddningspreferenser. För T2R46 erbjuder den konserverade centrala fickan och dess interaktion med den flexibla slingans ett stabilt ramverk för att designa ligander som verkar mer som precisa verktyg än som trubbiga, brett bittra läkemedel. Eftersom dessa receptorer påverkar ämnesomsättning, inflammation och cancer långt från tungan, skulle sådana riktade molekyler en dag kunna utnyttja vårt bitterhetssinne för att behandla sjukdom — utan att nödvändigtvis förändra hur maten smakar.
Citering: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Nyckelord: bittra smaksensorer, T2R14, T2R46, ligandbindning, läkemedelsupptäckt