Clear Sky Science · pt
Modos de ligação de ligantes dos receptores do gosto amargo T2R14 e T2R46
Por que o amargor importa além da língua
A maioria de nós associa sabores amargos a algo a evitar em alimentos ou bebidas, mas os mesmos sensores que tornam o café ou a água tônica aguçados estão espalhados pelo corpo, onde influenciam o metabolismo, a inflamação e até o câncer. Este estudo concentra-se em dois dos “detetores de amargor” mais abrangentes, chamados T2R14 e T2R46, e mostra em detalhe atômico como eles reconhecem moléculas amargas muito diferentes. Ao revelar onde esses compostos se acomodam nos receptores e como isso desencadeia um sinal dentro das células, o trabalho abre caminho para projetar novos medicamentos que aproveitem o circuito do amargor do corpo sem depender de descobertas fortuitas.
Dois sentinelas versáteis para químicos amargos
Os humanos têm 25 receptores de gosto amargo conhecidos, mas T2R14 e T2R46 se destacam por responderem a uma gama especialmente ampla de compostos vegetais e fármacos. Esses receptores não estão apenas na língua; também ocorrem no intestino, nos vasos sanguíneos, no tecido adiposo e nas vias aéreas, onde ajudam a regular colesterol, inflamação, obesidade e crescimento tumoral. Ainda assim, desenvolvedores de fármacos têm dificuldade em direcioná-los porque seus ligantes naturais tendem a se ligar fracamente e com baixa seletividade. Para enfrentar esse problema, os autores usaram criomicroscopia eletrônica de alta resolução para determinar sete estruturas tridimensionais de T2R14 e T2R46, vazias ou ligadas a diferentes moléculas amargas, todas capturadas no momento de sinalização através de uma proteína G dentro da célula.
Um receptor, duas portas para moléculas amargas
A primeira surpresa veio de T2R14, que revelou usar duas áreas de acoplamento separadas para seus ligantes. Trabalhos anteriores haviam sugerido um sítio interno mais próximo do interior celular, mas as novas estruturas mostram que muitos de seus compostos vegetais mais conhecidos, como a flavona cítrica tangeretina e o antisséptico clorexidina, na verdade se alojam em um bolso maior aberto para o exterior da célula. Esse bolso externo pode acomodar moléculas volumosas, frequentemente neutras ou positivamente carregadas, enquanto um bolso interno menor favorece ácidos compactos e negativamente carregados. Acoplamentos computacionais de 385 ativadores conhecidos de T2R14 mostraram que cerca de 90% preferem o bolso externo, enquanto apenas certos pequenos ácidos ou fenilpropanoides favorecem o interno. Esse sistema de entrada dupla ajuda a explicar por que T2R14 consegue reconhecer centenas de substâncias amargas muito diferentes.
Dois receptores, um ligante, encaixes bem diferentes
O estudo comparou então como o mesmo composto, a tangeretina, se liga a T2R14 e T2R46. Embora ambos os receptores percebam essa molécula cítrica, as estruturas revelam que a tangeretina fica ereta em T2R14, mas deitada em T2R46, girada cerca de 90 graus. Essa reorientação dramática é causada por diferenças sutis no posicionamento das hélices mais externas, especialmente um segmento chamado hélice VII, e pelos aminoácidos que revestem o bolso de ligação. T2R14 usa um aglomerado de resíduos volumosos e hidrofóbicos na entrada do bolso para prender uma extremidade da tangeretina, enquanto T2R46 conta com um bolso central mais clássico onde um único triptofano altamente conservado atua como núcleo, empilhando-se contra o núcleo de vários ligantes não relacionados, incluindo tangeretina, estricnina, artemisinina e denatônio. Mutar esses resíduos-chave reduziu fortemente a ativação do receptor, confirmando que os arranjos distintos são essenciais para como cada receptor escolhe e responde aos seus ligantes.
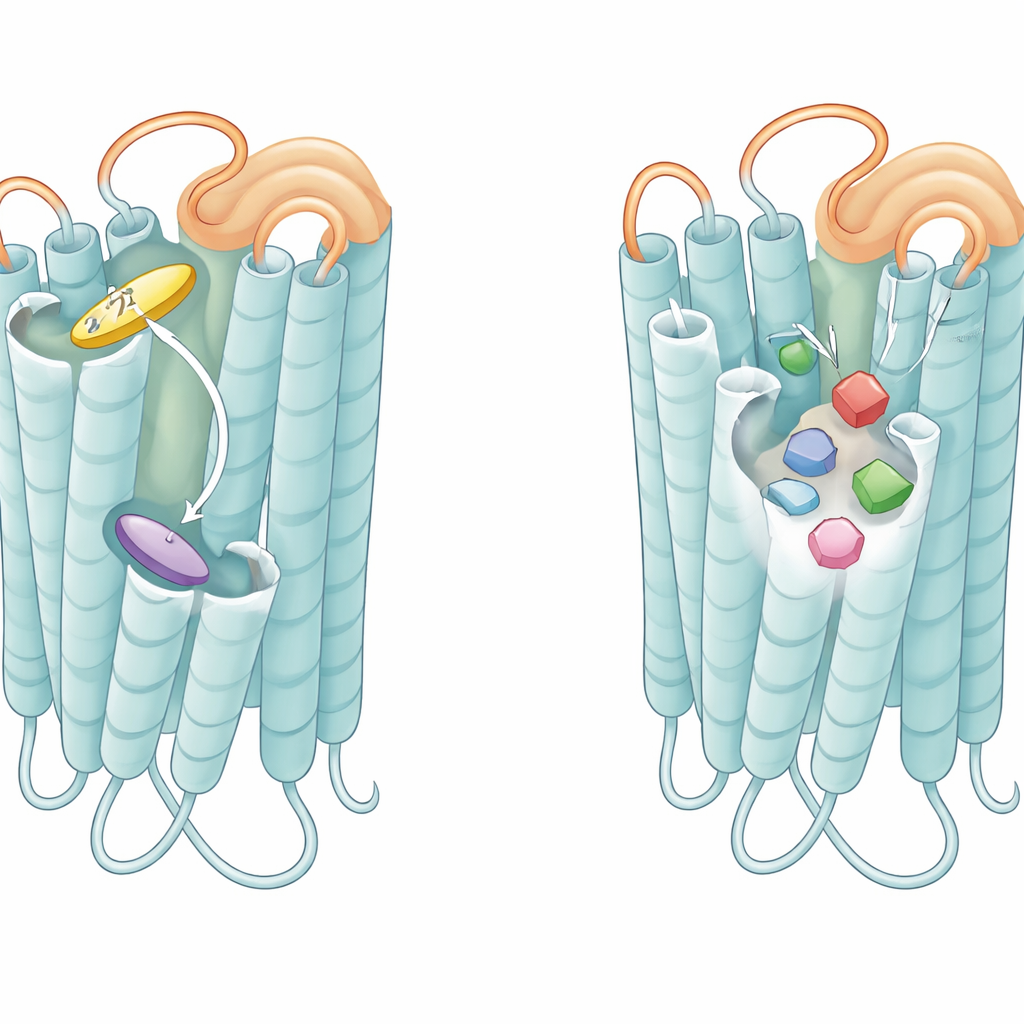
Como alças e bolsos ajustam a sensibilidade ao amargor
Além dos próprios bolsos, a alça flexível que se projeta sobre a face externa de cada receptor, conhecida como segunda alça extracelular, emergiu como um componente crucial. Em T2R46, quando nenhum tastante está ligado, essa alça dobra-se para dentro do bolso e imita um ligante, empilhando-se contra o mesmo triptofano que moléculas amargas reais usam. Pequenos peptídeos copiados dessa alça conseguiram ativar o receptor por si só, e alterar resíduos da alça reduziu a atividade basal do receptor e sua resposta a agonistas fracos. Um peptídeo semelhante derivado da alça de T2R14 ativou fortemente o T2R14 e, em menor grau, o T2R46. Esses achados sugerem que a alça age como um mini-agonista embutido e preso, que mantém o receptor em um estado de pré-alerta, pronto para responder rapidamente mesmo a compostos amargos de baixa afinidade.
O que isso significa para futuros medicamentos
Ao mapear exatamente como diferentes compostos amargos se alojam em T2R14 e T2R46, e como uma alça embutida os ajuda a ativar apesar da ligação fraca, este trabalho fornece um roteiro para o desenho racional de fármacos. Para T2R14, químicos podem mirar tanto no espaçoso bolso externo quanto no interno mais apertado para ajustar seletividade e preferências de carga. Para T2R46, o bolso central conservado e sua interação com a alça flexível oferecem uma estrutura estável para projetar ligantes que atuem mais como ferramentas precisas do que como fármacos amplamente amargos e pouco seletivos. Como esses receptores influenciam metabolismo, inflamação e câncer longe da língua, tais moléculas direcionadas poderiam um dia aproveitar nossa maquinaria de detecção do amargor para tratar doenças — sem necessariamente alterar o sabor das refeições.
Citação: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Palavras-chave: receptores do gosto amargo, T2R14, T2R46, ligação de ligantes, descoberta de fármacos