Clear Sky Science · ru
Режимы связывания лигандов горького рецептора T2R14 и T2R46
Почему горечь важна не только для языка
Большинство из нас воспринимает горький вкус как то, чего следует избегать в пище и напитках, но одни и те же сенсоры, из‑за которых кофе или тоник кажутся резкими, распределены по всему организму и влияют на метаболизм, воспаление и даже рак. В этом исследовании рассматриваются два из самых универсальных «детекторов горечи» — T2R14 и T2R46 — и показано на атомном уровне, как они распознают принципиально разные горькие молекулы. Установив, где именно эти соединения располагаются на рецепторах и как это запускает внутриклеточный сигнал, работа открывает путь к разработке новых лекарств, которые будут использовать схемы горечи организма без опоры на случайные открытия.
Два универсальных стража горьких веществ
У человека известно 25 рецепторов горького вкуса, но T2R14 и T2R46 выделяются тем, что реагируют на особенно широкий спектр растительных веществ и лекарств. Эти рецепторы находятся не только на языке; их обнаруживают также в кишечнике, кровеносных сосудах, жировой ткани и дыхательных путях, где они помогают регулировать холестерин, воспаление, ожирение и рост опухолей. При этом разработчикам лекарств трудно нацеливаться на них, потому что их природные лиганды обычно связываются с низкой аффинностью и плохой селективностью. Чтобы решить эту проблему, авторы использовали крио‑электронную микроскопию высокого разрешения и определили семь трёхмерных структур T2R14 и T2R46 — пустых или связанных с разными горькими молекулами, — все в состоянии активации через G‑белок внутри клетки.
Один рецептор — две двери для горьких молекул
Первым сюрпризом стал T2R14, который оказался использующим две отдельные области стыковки для своих лигандов. Ранние работы предполагали внутренний сайт ближе к цитоплазме, но новые структуры показывают, что многие из его наиболее известных растительных соединений, такие как цитрусовый флавон танжеретин и антисептик хлоргексидин, фактически помещаются в более крупную полость, открытую к внешней стороне клетки. Эта внешняя полость может вмещать громоздкие, часто незаряженные или положительно заряженные молекулы, тогда как меньшая внутренняя полость предпочитает компактные, отрицательно заряженные кислоты. Компьютерное докирование 385 известных активаторов T2R14 показало, что примерно 90% из них отдают предпочтение внешней полости, в то время как в внутреннюю чаще попадают только определённые небольшие кислые или фенилпропаноидные молекулы. Такая система с двумя входами помогает понять, почему T2R14 распознаёт сотни очень разных горьких веществ.
Два рецептора, один лиганд — очень разные посадки
Далее в работе сравнили, как один и тот же компаунд, танжеретин, связывается с T2R14 и T2R46. Хотя оба рецептора чувствуют эту цитрусовую молекулу, структуры показывают, что в T2R14 танжеретин располагается «вправо» вертикально, а в T2R46 ложится боком, повернутый примерно на 90 градусов. Эта драматическая переориентация обусловлена тонкими различиями в расположении наружных спиралей, особенно сегмента, называемого спираль VII, и составом аминокислот, выстилающих связывающую полость. T2R14 использует кластер объёмных гидрофобных остатков у входа в карман, чтобы зафиксировать один конец танжеретина, тогда как T2R46 опирается на более классическую центральную полость, где одна сильно консервативная триптофановая аминокислота выступает в роли центра — осуществляя стэкинг с ядром нескольких несвязанных лигандов, включая танжеретин, стрихнин, артемизинин и денатоний. Мутации в этих ключевых остатках резко снижали активацию рецепторов, что подтверждает: различные организации карманов критически важны для того, как каждый рецептор выбирает и отвечает на свои лиганды.
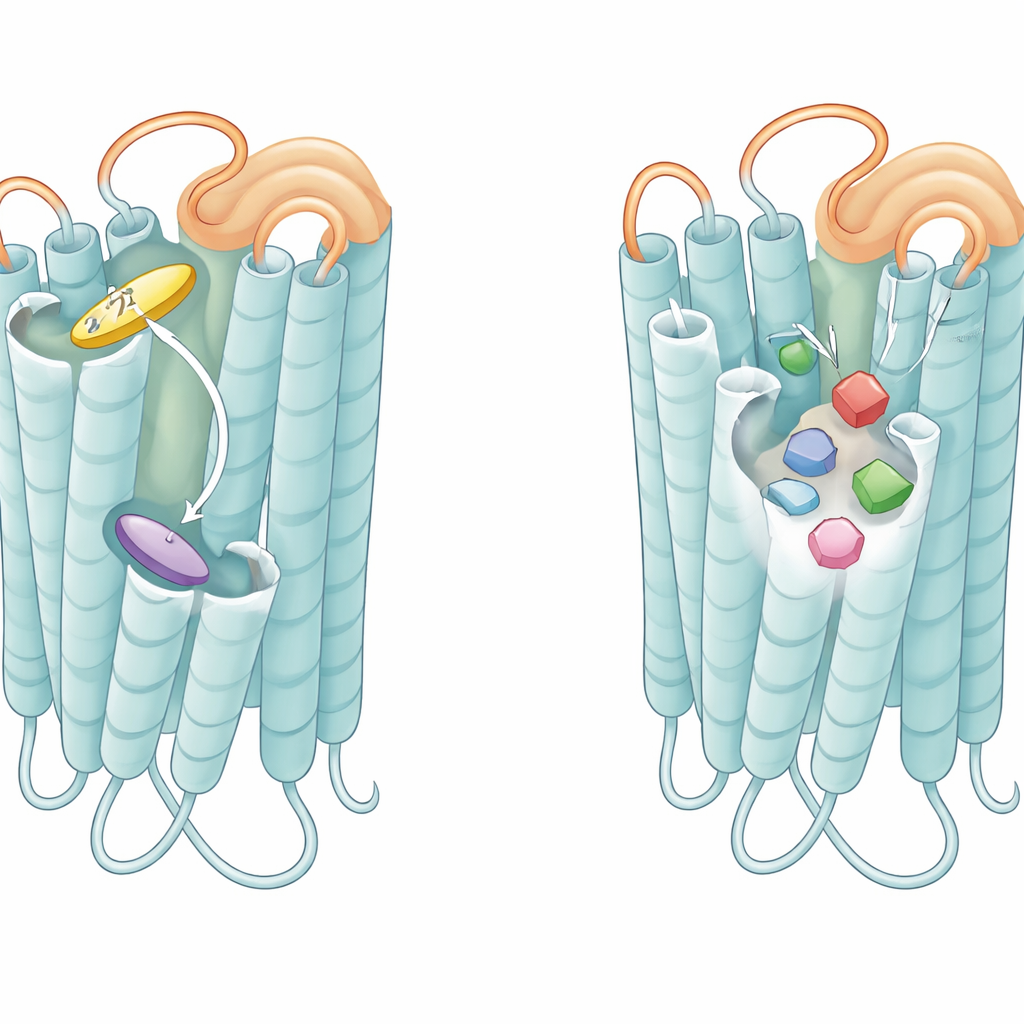
Как петли и карманы настраивают чувствительность к горечи
Помимо самих полостей, гибкая петля, свисающая над внешней стороной каждого рецептора и известная как вторая внеклеточная петля, оказалась ключевым элементом. В T2R46, когда никакой вкусообразующий лиганд не связан, эта петля складывается внутрь кармана и имитирует лиганд, стэкуясь с тем же триптофаном, которого используют настоящие горькие молекулы. Пептиды, скопированные с этой петли, могли сами по себе активировать рецептор, а изменение остатков в петле снижало фоновую активность рецептора и его ответ на слабые агонисты. Аналогичный пептид, полученный из петли T2R14, сильно активировал T2R14 и, в меньшей степени, T2R46. Эти наблюдения указывают на то, что петля действует как встроенный, прикреплённый мини‑агонист, поддерживающий рецептор в предвключённом состоянии и позволяющий быстро реагировать даже на низкоаффинные горькие соединения.
Что это значит для будущих лекарств
Отобразив, как различные горькие соединения размещаются в T2R14 и T2R46 и как встроенная петля помогает им включать рецептор несмотря на слабое связывание, эта работа даёт чертёж для рационального дизайна лекарств. Для T2R14 химики могут нацеливаться как на просторную внешнюю полость, так и на более узкую внутреннюю, чтобы настраивать селективность и предпочтения по заряду. Для T2R46 консервативная центральная полость и её взаимодействие с гибкой петлёй предлагают стабильную основу для создания лигандов, действующих как точные инструменты, а не грубые широко горькие молекулы. Поскольку эти рецепторы влияют на метаболизм, воспаление и рак далеко от языка, такие таргетные молекулы однажды могли бы использовать нашу систему восприятия горечи для лечения заболеваний — без необходимости менять вкус пищи.
Цитирование: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Ключевые слова: рецепторы горького вкуса, T2R14, T2R46, связывание лигандов, поиск лекарств