Clear Sky Science · de
Bindungsmodi von Liganden an den bitteren Geschmacksrezeptoren T2R14 und T2R46
Warum Bitterkeit über die Zunge hinaus wichtig ist
Die meisten von uns betrachten bittere Aromen als etwas, das man in Speisen oder Getränken meiden sollte, doch dieselben Sensoren, die Kaffee oder Tonic Water scharf schmecken lassen, sind im ganzen Körper verstreut und beeinflussen Stoffwechsel, Entzündungen und sogar Krebs. Diese Studie konzentriert sich auf zwei der vielseitigsten „Bitterdetektoren“, genannt T2R14 und T2R46, und zeigt im atomaren Detail, wie sie sehr unterschiedliche bittere Moleküle erkennen. Indem sie offenlegt, wo diese Verbindungen an den Rezeptoren andocken und wie das innerhalb der Zelle ein Signal auslöst, schafft die Arbeit die Grundlage dafür, neue Medikamente zu entwerfen, die die Bitterkeitsvorrichtungen des Körpers gezielt nutzen, ohne auf Zufallsfunde angewiesen zu sein.
Zwei vielseitige Wächter für bittere Substanzen
Beim Menschen sind 25 bittere Geschmacksrezeptoren bekannt, doch T2R14 und T2R46 fallen auf, weil sie auf ein besonders breites Spektrum pflanzlicher Verbindungen und Arzneistoffe reagieren. Diese Rezeptoren sitzen nicht nur auf der Zunge; man findet sie auch im Darm, in Blutgefäßen, im Fettgewebe und in den Atemwegen, wo sie Cholesterin, Entzündungen, Fettleibigkeit und Tumorwachstum mitregulieren. Arzneimittelentwicklern fiel es jedoch schwer, sie gezielt anzusprechen, weil ihre natürlichen Liganden oft schwach und wenig selektiv binden. Um dieses Problem anzugehen, bestimmten die Autoren mit hochauflösender Kryo-Elektronenmikroskopie sieben dreidimensionale Strukturen von T2R14 und T2R46, entweder unbesetzt oder gebunden an verschiedene bittere Moleküle, jeweils in dem Moment, in dem sie über ein G-Protein innerhalb der Zelle Signale übermitteln.
Ein Rezeptor, zwei Zugänge für bittere Moleküle
Die erste Überraschung betraf T2R14, das offenbar zwei getrennte Andockbereiche für seine Liganden nutzt. Frühere Arbeiten hatten eine interne Stelle näher zum Zellinneren vermutet, doch die neuen Strukturen zeigen, dass viele seiner bekanntesten Pflanzenverbindungen, wie die Zitrusflavon-Tangeretin und das Antiseptikum Chlorhexidin, tatsächlich in eine größere Tasche nach außen hin einliegen. Diese äußere Tasche kann sperrige, oft ungeladene oder positiv geladene Moleküle aufnehmen, während eine kleinere innere Tasche kompakte, negativ geladene Säuren bevorzugt. Computersimulierte Andockberechnungen für 385 bekannte T2R14-Aktivatoren ergaben, dass etwa 90 % die äußere Tasche bevorzugen, während nur bestimmte kleine saure oder Phenylpropanoid-Moleküle die innere bevorzugen. Dieses Doppel-Zugangssystem erklärt, warum T2R14 hunderte sehr unterschiedlicher bitterer Substanzen erkennen kann.
Zwei Rezeptoren, ein Ligand, sehr unterschiedliche Passformen
Die Studie verglich dann, wie dieselbe Verbindung, Tangeretin, an T2R14 und T2R46 bindet. Obwohl beide Rezeptoren dieses Zitrusmolekül wahrnehmen, zeigen die Strukturen, dass Tangeretin in T2R14 aufrecht sitzt, in T2R46 dagegen seitlich liegt und um etwa 90 Grad gedreht ist. Diese dramatische Umorientierung entsteht durch subtile Unterschiede in der Positionierung der äußersten Helices, besonders eines Abschnitts namens Helix VII, und durch die unterschiedlichen Aminosäuren, die die Bindungstasche auskleiden. T2R14 verwendet einen Cluster aus sperrigen, fettliebenden Resten am Tascheneingang, um ein Ende von Tangeretin zu umgreifen, wohingegen T2R46 auf eine klassischere, zentral platzierte Tasche setzt, in der ein einzelnes hochkonserviertes Tryptophan als Zentrum fungiert und sich gegen den Kern mehrerer unzusammenhängender Liganden wie Tangeretin, Strychnin, Artemisinin und Denatonium stapelt. Mutationen dieser Schlüsselreste verringerten die Rezeptoraktivierung deutlich und bestätigten, dass die unterschiedlichen Anordnungen entscheidend dafür sind, wie jeder Rezeptor seine Liganden auswählt und darauf reagiert.
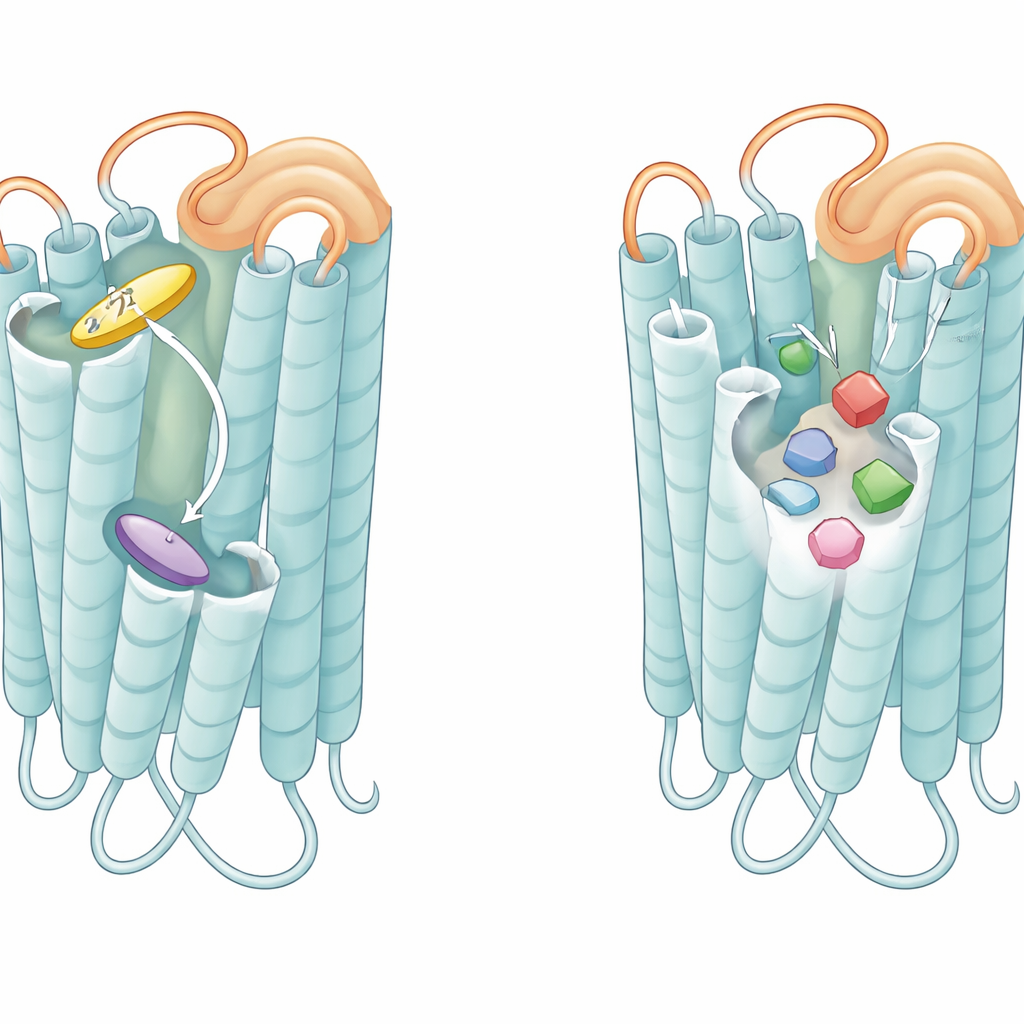
Wie Schleifen und Taschen die Bitterempfindlichkeit abstimmen
Über die Taschen selbst hinaus erwies sich die flexible Schleife, die die äußere Fläche jedes Rezeptors überragt und als zweite extrazelluläre Schleife bekannt ist, als entscheidender Faktor. Bei T2R46 klappt diese Schleife in Abwesenheit eines Tastants in die Tasche hinein und imitiert ein Ligand, indem sie gegen dasselbe Tryptophan stapelt, das echte bittere Moleküle nutzen. Peptide, die von dieser Schleife abgeschrieben wurden, konnten den Rezeptor eigenständig aktivieren, und Veränderungen der Schleifreste verringerten die Hintergrundaktivität des Rezeptors und seine Reaktion auf schwache Agonisten. Ein ähnliches Peptid aus der Schleife von T2R14 aktivierte T2R14 stark und T2R46 in geringerem Maße. Diese Befunde deuten darauf hin, dass die Schleife wie ein eingebauter, angehefteter Mini-Agonist funktioniert, der den Rezeptor in einem vorgewarnten Zustand hält und ihn befähigt, schnell selbst auf schwach bindende bittere Verbindungen zu reagieren.
Was das für künftige Medikamente bedeutet
Indem genau kartiert wird, wie verschiedene bittere Verbindungen in T2R14 und T2R46 gebettet sind und wie eine eingebaute Schleife ihnen hilft, trotz schwacher Bindung zu aktivieren, liefert diese Arbeit eine Blaupause für rationales Wirkstoffdesign. Bei T2R14 können Chemiker gezielt die geräumige äußere Tasche oder die engere innere Tasche anvisieren, um Selektivität und Ladungsvorlieben zu steuern. Bei T2R46 bieten die konservierte zentrale Tasche und ihre Wechselwirkung mit der flexiblen Schleife ein stabiles Gerüst, um Liganden zu entwerfen, die eher präzise Werkzeuge als grobe, breit wirkende bittere Substanzen sind. Da diese Rezeptoren weit entfernt von der Zunge Stoffwechsel, Entzündungen und Krebs beeinflussen, könnten derartige zielgerichtete Moleküle eines Tages unsere bitteren Sensoren nutzen, um Krankheiten zu behandeln—ohne unbedingt den Geschmack des Essens zu verändern.
Zitation: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Schlüsselwörter: bittere Geschmacksrezeptoren, T2R14, T2R46, Ligandenbindung, Arzneimittelentdeckung