Clear Sky Science · es
Modos de unión de ligandos de los receptores del gusto amargo T2R14 y T2R46
Por qué la amargura importa más allá de la lengua
La mayoría de nosotros pensamos en los sabores amargos como algo a evitar en la comida o la bebida, pero los mismos sensores que hacen que el café o el agua tónica sepan intensos también están repartidos por todo el cuerpo, donde influyen en el metabolismo, la inflamación e incluso en el cáncer. Este estudio se centra en dos de los detectores de amargor más generales, llamados T2R14 y T2R46, y muestra en detalle atómico cómo reconocen moléculas amargas muy distintas. Al revelar dónde se sitúan estos compuestos en los receptores y cómo eso desencadena una señal dentro de las células, el trabajo abre la puerta al diseño de nuevos medicamentos que aprovechen el circuito de la amargura del cuerpo sin depender de hallazgos fortuitos.
Dos centinelas versátiles para químicos amargos
Los humanos tienen 25 receptores del gusto amargo conocidos, pero T2R14 y T2R46 destacan porque responden a una gama especialmente amplia de compuestos vegetales y fármacos. Estos receptores no solo están en la lengua; también se encuentran en el intestino, los vasos sanguíneos, el tejido adiposo y las vías respiratorias, donde ayudan a regular el colesterol, la inflamación, la obesidad y el crecimiento tumoral. Sin embargo, los desarrolladores de fármacos han tenido dificultades para dirigirse a ellos porque sus ligandos naturales tienden a unirse débilmente y con poca selectividad. Para abordar este problema, los autores utilizaron criomicroscopía electrónica de alta resolución para determinar siete estructuras tridimensionales de T2R14 y T2R46, ya sea vacías o unidas a diferentes moléculas amargas, todas capturadas en el acto de señalizar a través de una proteína G dentro de la célula.
Un receptor, dos puertas para moléculas amargas
La primera sorpresa vino de T2R14, que resultó usar dos áreas de acoplamiento separadas para sus ligandos. Trabajos anteriores habían sugerido un sitio interno más cercano al interior celular, pero las nuevas estructuras muestran que muchos de sus compuestos vegetales más conocidos, como la flavona cítrica tangeretina y el antiséptico clorhexidina, en realidad se alojan en un bolsillo más grande abierto hacia el exterior de la célula. Este bolsillo externo puede acomodar moléculas voluminosas, a menudo no cargadas o con carga positiva, mientras que un bolsillo interior más pequeño favorece ácidos compactos y cargados negativamente. El acoplamiento por ordenador de 385 activadores conocidos de T2R14 mostró que aproximadamente el 90 % prefieren el bolsillo externo, mientras que solo ciertos pequeños ácidos o moléculas fenilpropanoides favorecen el interno. Este sistema de doble entrada ayuda a explicar por qué T2R14 puede reconocer cientos de sustancias amargas muy distintas.
Dos receptores, un ligando, ajustes muy diferentes
El estudio comparó luego cómo se une el mismo compuesto, la tangeretina, a T2R14 y a T2R46. Aunque ambos receptores detectan esta molécula cítrica, las estructuras revelan que la tangeretina se sitúa en posición vertical en T2R14 pero se tumba de lado en T2R46, girada aproximadamente 90 grados. Esta reorientación dramática se debe a diferencias sutiles en la posición de las hélices más externas, en especial un segmento llamado hélice VII, y a qué aminoácidos recubren el bolsillo de unión. T2R14 usa un grupo de residuos voluminosos y apolares en la entrada del bolsillo para sujetar un extremo de la tangeretina, mientras que T2R46 se apoya en un bolsillo más clásico y central donde un único triptófano altamente conservado actúa como un núcleo, apilándose contra el núcleo de varios ligandos no relacionados, incluida la tangeretina, la estricnina, la artemisinina y la denatonio. Mutar estos residuos clave redujo drásticamente la activación del receptor, confirmando que las diferentes disposiciones son esenciales para cómo cada receptor elige y responde a sus ligandos.
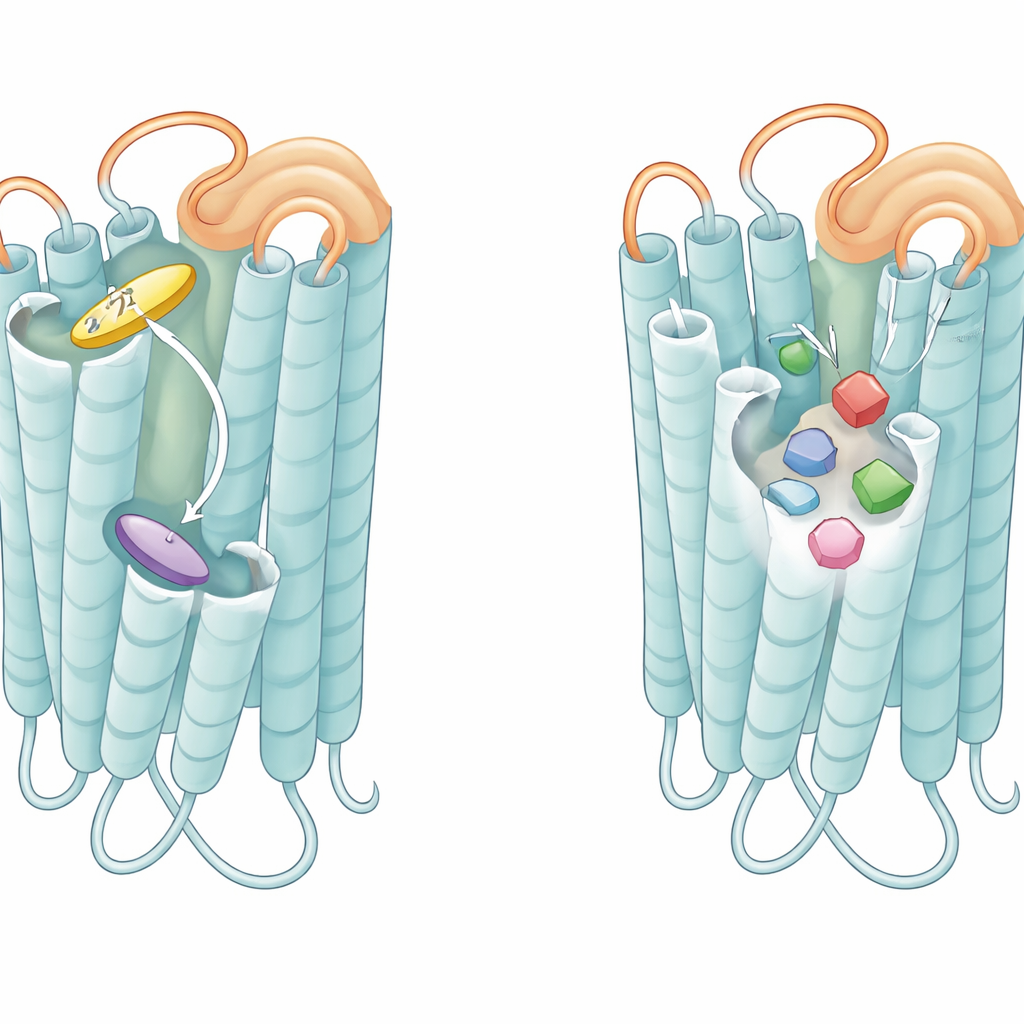
Cómo los bucles y los bolsillos afinan la sensibilidad al amargor
Más allá de los propios bolsillos, el bucle flexible que cuelga sobre la cara externa de cada receptor, conocido como el segundo bucle extracelular, emergió como un jugador crucial. En T2R46, cuando no hay tastante unido, este bucle se pliega dentro del bolsillo e imita a un ligando, apilándose contra el mismo triptófano que usan las verdaderas moléculas amargas. Péptidos copiadas de este bucle pudieron activar el receptor por sí solos, y alterar residuos del bucle redujo la actividad basal del receptor y su respuesta a agonistas débiles. Un péptido similar derivado del bucle de T2R14 activó fuertemente T2R14 y, en menor medida, T2R46. Estos hallazgos sugieren que el bucle se comporta como un miniagonista integrado y atado que mantiene al receptor en un estado de alerta previa, listo para responder rápidamente incluso a compuestos amargos de baja afinidad.
Qué significa esto para futuros medicamentos
Al mapear exactamente cómo diferentes compuestos amargos encajan en T2R14 y T2R46, y cómo un bucle incorporado les ayuda a activarse pese a una unión débil, este trabajo ofrece un plano para el diseño racional de fármacos. Para T2R14, los químicos pueden dirigirse tanto al espacioso bolsillo externo como al más estrecho interno para ajustar la selectividad y las preferencias de carga. Para T2R46, el bolsillo central conservado y su interacción con el bucle flexible ofrecen un marco estable para diseñar ligandos que actúen más como herramientas precisas que como fármacos amargos de amplio espectro. Dado que estos receptores influyen en el metabolismo, la inflamación y el cáncer lejos de la lengua, tales moléculas dirigidas podrían algún día aprovechar nuestra maquinaria de detección del amargor para tratar enfermedades, sin necesariamente cambiar cómo sabe la cena.
Cita: Tan, Q., Yu, Y., Han, X. et al. Ligand binding modes of the bitter taste receptor T2R14 and T2R46. Nat Struct Mol Biol 33, 691–700 (2026). https://doi.org/10.1038/s41594-026-01786-8
Palabras clave: receptores del gusto amargo, T2R14, T2R46, unión de ligandos, descubrimiento de fármacos