Clear Sky Science · tr
In vitro ve in vivo ortamda nörogelişimsel bozukluk risk genlerinin transkriptomik ve fenotipik yakınsaması
Neden farklı genler benzer beyin sorunlarına yol açabilir
Otizm veya gelişimsel gecikme tanısı alan birçok çocukta genetik mutasyonlar birbirinden çok farklıdır, ancak çoğu zaman öğrenme, davranış veya duyusal sorunlar benzer biçimde görülür. Bu çalışma, basit görünen ama sonuçları büyük olan bir soruyu soruyor: onlarca farklı risk geni değiştirildiğinde, beyin hücrelerinde aynı temel süreçleri bozuyorlar mı ve bu ortak zayıf noktalar gelecekteki tedavilere yol gösterebilir mi?
Beyin hücrelerinde aynı anda birçok gene bakmak
Araştırmacılar, çoğunlukla DNA’nın nasıl paketlendiğini ve okunmasını kontrol etmeye yardımcı olan, yüksek etkili 23 nörogelişimsel bozukluk ilişkili gene ve sinir hücreleri arasındaki iletişim için hayati birkaç gene odaklandı. İnsan kök hücreleri kullanarak gelişmekte olan kortekste bulunan üç temel hücre tipini büyüttüler: bölünen nöral progenitör hücreler, beyin aktivitesini uyaran eksitatör (glutamaterjik) nöronlar ve aktiviteyi baskılayan inhibitör (GABAerjik) nöronlar. Havuzlanmış bir CRISPR yaklaşımıyla her risk genini binlerce tek hücrede kapattılar ve sonra bu hücrelerde hangi diğer genlerin yukarı veya aşağı yönde değiştiğini ölçtüler. Bu, birçok farklı mutasyon arasında, daha sonra hangi gen setleri veya yollar üzerinde etkilerinin “yakınsadığını” görmelerini sağladı.
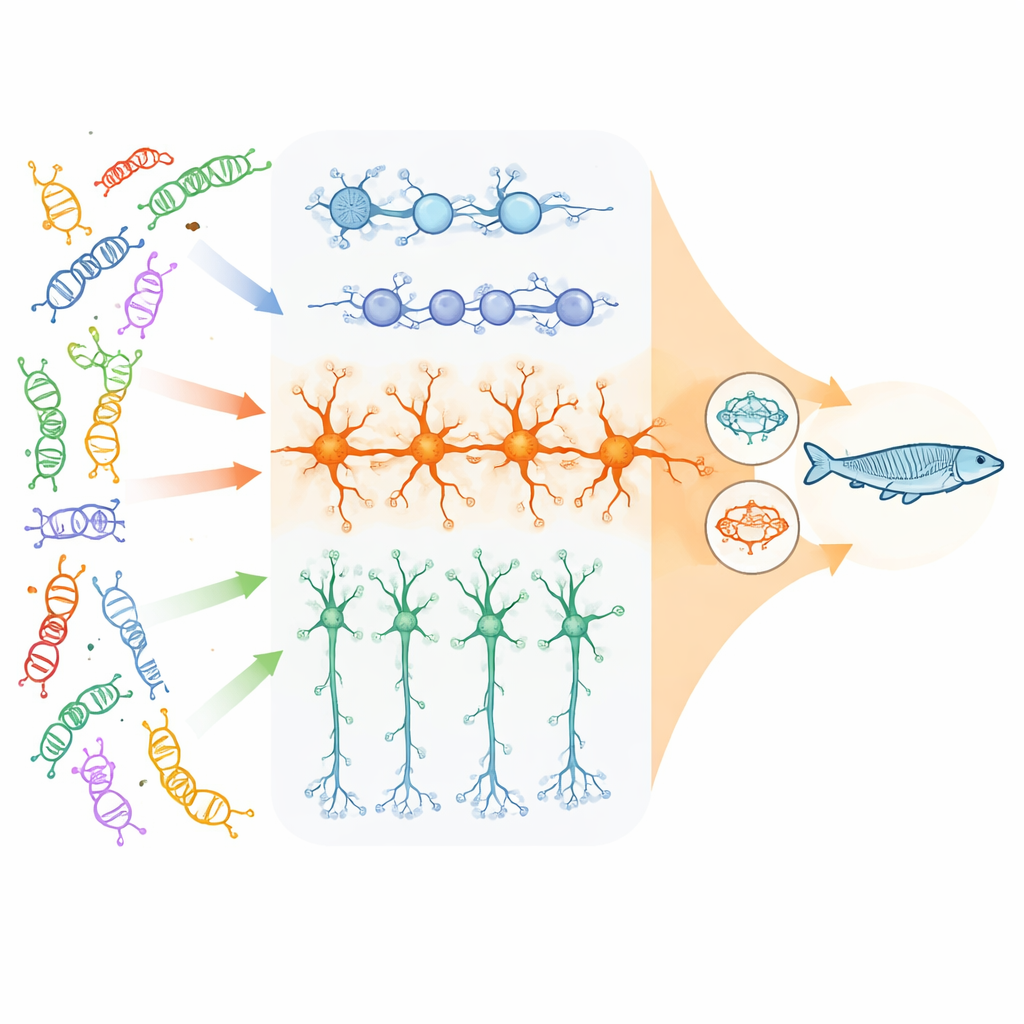
Yakınsama en güçlü şekilde eksitatör nöronlarda
Ekip, yakınsamanın hücre tipi ve gelişim aşamasına güçlü biçimde bağlı olduğunu buldu. Her genin yokluğunun kendine özgü bir parmak izi varken, en kapsamlı ve sıkı bağlantılı ortak değişiklikler olgun eksitatör nöronlarda ortaya çıktı. Burada, binlerce gen birçok farklı risk geninde benzer şekillerde değişmişti. Etkilenen ağlar üç temaya odaklandı: nöronların iletişim kurduğu sinapslar, hangi genlerin açık veya kapalı olacağını kontrol eden hücresel mekanizma ve beklenmedik bir şekilde hücrenin enerji fabrikaları olan mitokondriler. Buna karşılık, nöral progenitörler ağırlıklı olarak hücre bölünmesi ve erken beyin büyümesi yollarında ortak değişiklikler gösterirken, inhibitör nöronlar daha ılımlı ve farklı yakınsama desenleri sergiledi.
Gen ağlarından beyin işlevi ve davranışa
Bu yakınsayan değişikliklerin hastalık için önemli olup olmadığını test etmek için yazarlar ortak gen imzalarını psikiyatrik durumlara ilişkin büyük genetik çalışmalarla karşılaştırdı. Eksitatör nöronlardaki yakınsayan genler ve ağlar, otizm, şizofreni ve zihinsel yetersizlikle ilişkili risk varyantları ile ve ayrıca Fragile X proteininin bilinen hedefleri ile zenginleşmişti. Bu verilere eğitilmiş makine öğrenimi modelleri, 100’den fazla bilinen nörogelişimsel risk geni arasında, esas olarak otizme bağlı olanların eksitatör nöronlarda yakınsadığını, global gelişimsel gecikmeyle daha ilişkili olanların ise inhibitör nöronlarda yakınsadığını öngördü. Ekip ayrıca deneysel olarak birkaç temsilci risk geninin tek tek bozulmasının, nöronların yeni hücre üretme biçimleri ve mitokondrilerinin yapısı ile oksijen tüketimi üzerinde farklı ama ilişkili sorunlar ürettiğini gösterdi—havuzlanmış ekranlarda görülen yakınsama desenleriyle uyumlu şekilde.
Canlı hayvanlarda ve ilaçlarda yakınsamayı test etmek
Hücre kültürleri bütün beyin devrelerini veya davranışı yakalayamadığından, araştırmacılar aynı genlerden oluşan bir alt kümede mutasyon taşıyan zebra balıklarına yöneldi. Uyku, uyanıklık ve irkilme tepkilerinin otomatik izlenmesi, bu balıkları uyku değişiklikleri veya ışık değişimlerine artmış hassasiyet gibi benzer desenlere sahip dört davranışsal “küme”ye ayırdı. Yazarlar bu davranışsal gruplaşmaları insan hücre verileriyle üst üste koyduklarında, her kümenin kendi yakınsayan gen desenine sahip olduğunu ve bunun yine en güçlü şekilde eksitatör nöronlarda görüldüğünü buldular. Ardından ilaç-etki veritabanlarını ve önceki zebra balığı ilaç taramalarını kullanarak yakınsayan imzaları tersine çevirebilecek ve mutant davranışlara karşı koyabilecek ilaçları tahmin ettiler. Takip testlerinde seçilen 11 ilacın 10’u zebra balığı mutantlarında en az bir anormal davranışı iyileştirdi ve bazıları uyku veya duyusal tepkilerde çarpıcı bir düzelme sağladı.
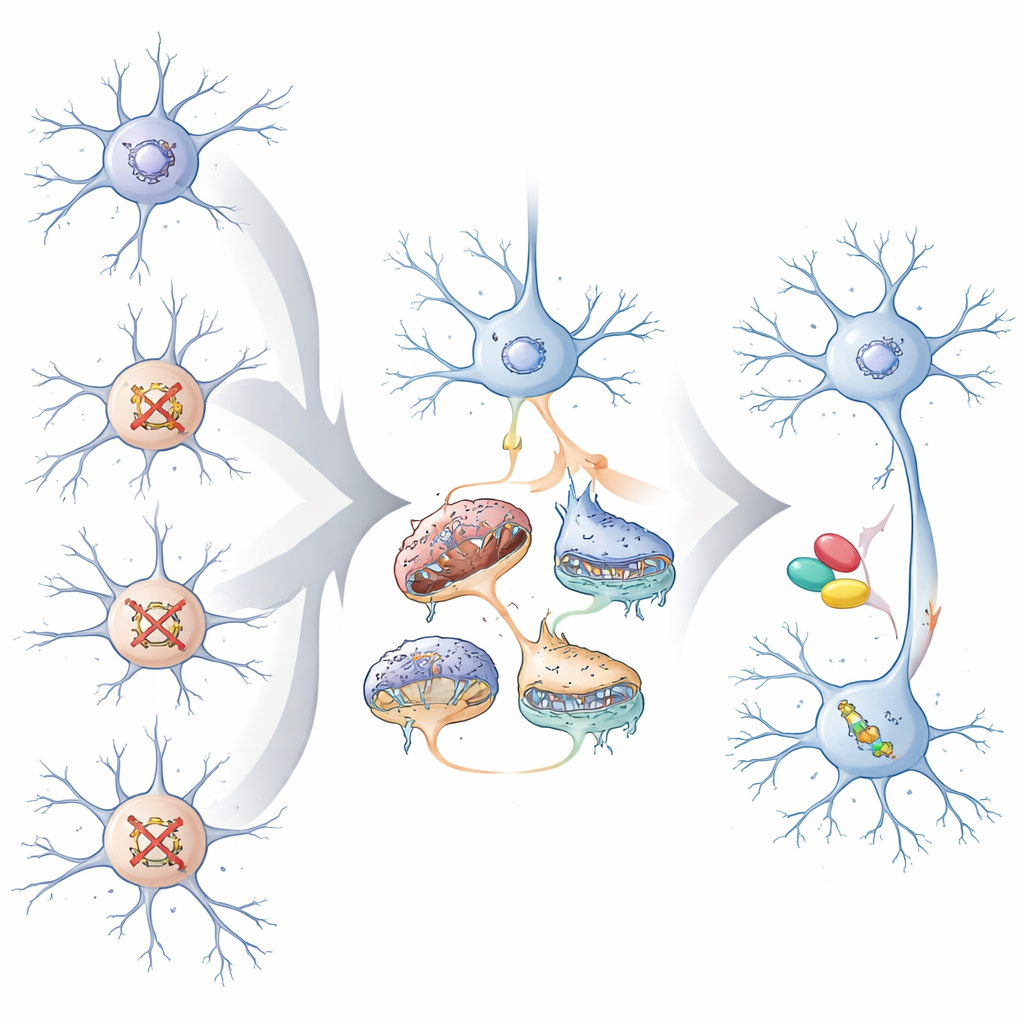
Gelecekteki tedaviler için bunun önemi
Uzman olmayan bir kişi için ana mesaj şudur: çok çeşitli otizm ve gelişimsel gecikme ile ilişkili genler, özellikle kortikal devreleri süren eksitatör nöronlarda, beyin hücrelerini daha küçük bir ortak sorun grubuna itebilir. Bu ortak problemler arasında sinapsların işlevi, gen etkinliğinin nasıl kontrol edildiği ve mitokondrilerin enerji sağlaması yer alır. Bu yakınsayan yolları haritalayarak çalışma, tedavilerin bir kişinin spesifik mutasyonuna göre değil, o mutasyonun harekete geçirdiği ortak hücresel “kırılma hatlarına” göre eşleştirilebileceğini öne sürüyor. Zebra balığı deneyleri, beyin geliştikten sonra bile bu ortak yolları hedeflemenin davranışı kısmen normalleştirebileceğini göstererek, yakınsayan biyolojinin daha kesin ve geniş kapsamlı terapilere yol gösterebileceği umudunu artırıyor.
Atıf: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Anahtar kelimeler: otizm genetiği, nörogelişimsel bozukluklar, eksitatör nöronlar, mitokondriyal işlev, zeberk balığı davranışı