Clear Sky Science · sv
Transkriptomisk och fenotypisk konvergens hos riskgener för neurodevelopmentala störningar in vitro och in vivo
Varför olika gener kan ge liknande hjärnproblem
Många barn som diagnostiserats med autism eller utvecklingsförsening har mycket olika genetiska mutationer, men delar ofta liknande svårigheter med inlärning, beteende eller sinnesupplevelser. Denna studie ställer en till synes enkel fråga med stora konsekvenser: när dussintals olika riskgener påverkas, rubbar de då samma grundläggande processer i hjärnceller, och skulle dessa gemensamma svaga punkter kunna användas för att leda framtida behandlingar?
Att undersöka många gener i hjärnceller samtidigt
Forskarna fokuserade på 23 högpåverkande gener kopplade till neurodevelopmentala störningar som främst hjälper till att styra hur DNA packas och läses, plus några som är viktiga för kommunikationen mellan nervceller. Med hjälp av humana stamceller odlade de tre nyckelcelltyper som finns i den utvecklande cortex: delande neurala progenitorceller, excitatoriska (glutamaterga) neuroner som stimulerar hjärnaktivitet, och inhibitoriska (GABAerga) neuroner som dämpar den. Med en poolad CRISPR-metod stängde de av varje riskgen i tusentals enskilda celler och mätte sedan vilka andra gener i dessa celler som ökade eller minskade i uttryck. Detta gjorde det möjligt att se, över många olika mutationer, var deras nedströms effekter "konvergerade" på samma uppsättningar gener eller signalvägar.
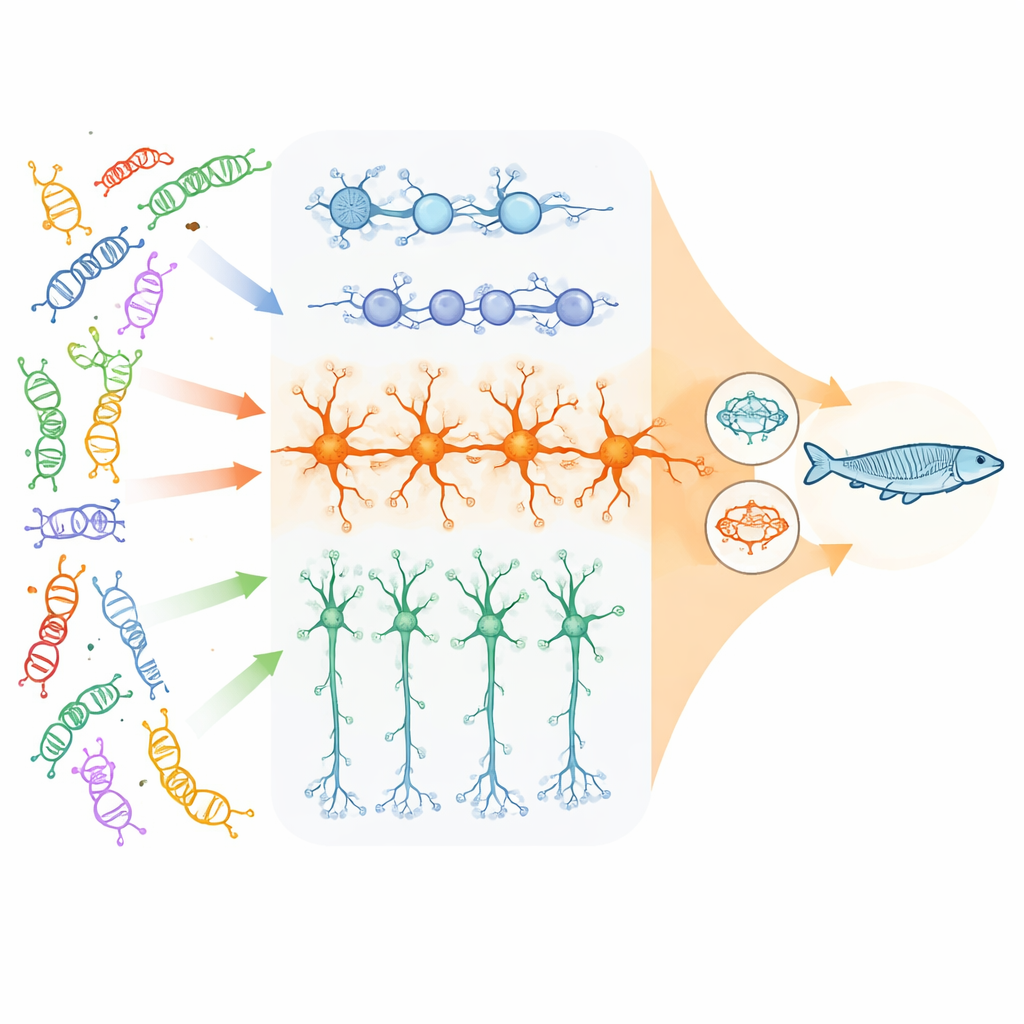
Konvergensen är starkast i excitatoriska neuroner
Teamet fann att konvergensen är starkt beroende av celltyp och utvecklingsstadium. Medan varje genknockout lämnade sitt eget fingeravtryck, uppstod de mest omfattande och tätt sammankopplade delade förändringarna i mogna excitatoriska neuroner. Här förändrades tusentals gener på liknande sätt över många olika riskgener. De påverkade nätverken kretsade kring tre teman: synapserna (kopplingarna där neuroner kommunicerar), den cellulära maskineriet som kontrollerar vilka gener som är aktiva eller inaktiva, och oväntat nog mitokondrierna — cellens energifabriker. I kontrast visade neurala progenitorer främst delade förändringar i celldelning och vägar för tidig hjärntillväxt, och inhibitoriska neuroner uppvisade mer blygsamma och distinkta konvergensmönster.
Från gen nätverk till hjärnfunktion och beteende
För att testa om dessa konvergerande förändringar har betydelse för sjukdom jämförde författarna de delade gensignaturerna med stora genetiska studier av psykiatriska tillstånd. De konvergenta generna och nätverken i excitatoriska neuroner var berikade för riskvarianter kopplade till autism, schizofreni och intellektuell funktionsnedsättning, liksom kända mål för Fragile X-proteinet. Maskininlärningsmodeller tränade på dessa data förutsade att, över mer än 100 kända riskgener för neurodevelopmentala störningar, tenderar de som huvudsakligen är kopplade till autism att konvergera i excitatoriska neuroner, medan de som mer är kopplade till generell utvecklingsförsening konvergerar i inhibitoriska neuroner. Teamet visade också experimentellt att flera representativa riskgener, när de störs individuellt, gav upphov till distinkta men relaterade problem i hur neuroner bildar nya celler och i hur deras mitokondrier är strukturerade och konsumerar syre — vilket matchar de konvergenta mönstren som observerades i de poolade skärmarna.
Testa konvergens i levande djur och med läkemedel
Eftersom cellodlingar inte fångar helhjärnkretsar eller beteende, vände forskarna sig till zebrafisk som bär mutationer i en delmängd av samma gener. Automatisk spårning av sömn, vakenhet och rädslorespons delade in dessa fiskar i fyra beteendemässiga "set" med liknande mönster, såsom förändrad sömn eller ökad känslighet för ljusförändringar. När författarna lade över dessa beteendemässiga grupper med sina humana celldata fann de att varje set var associerat med sitt eget mönster av konvergenta gener, återigen starkast i excitatoriska neuroner. De använde sedan läkemedelsresponser från databaser och tidigare zebrafiskscreeningar för att förutsäga läkemedel som kunde vända de konvergenta signaturerna och motverka mutantbeteendena. I uppföljande tester förbättrade 10 av 11 utvalda läkemedel åtminstone ett onormalt beteende hos zebrafiskmutanterna, och några gav påtagliga räddningar av sömn eller sensoriska responser.
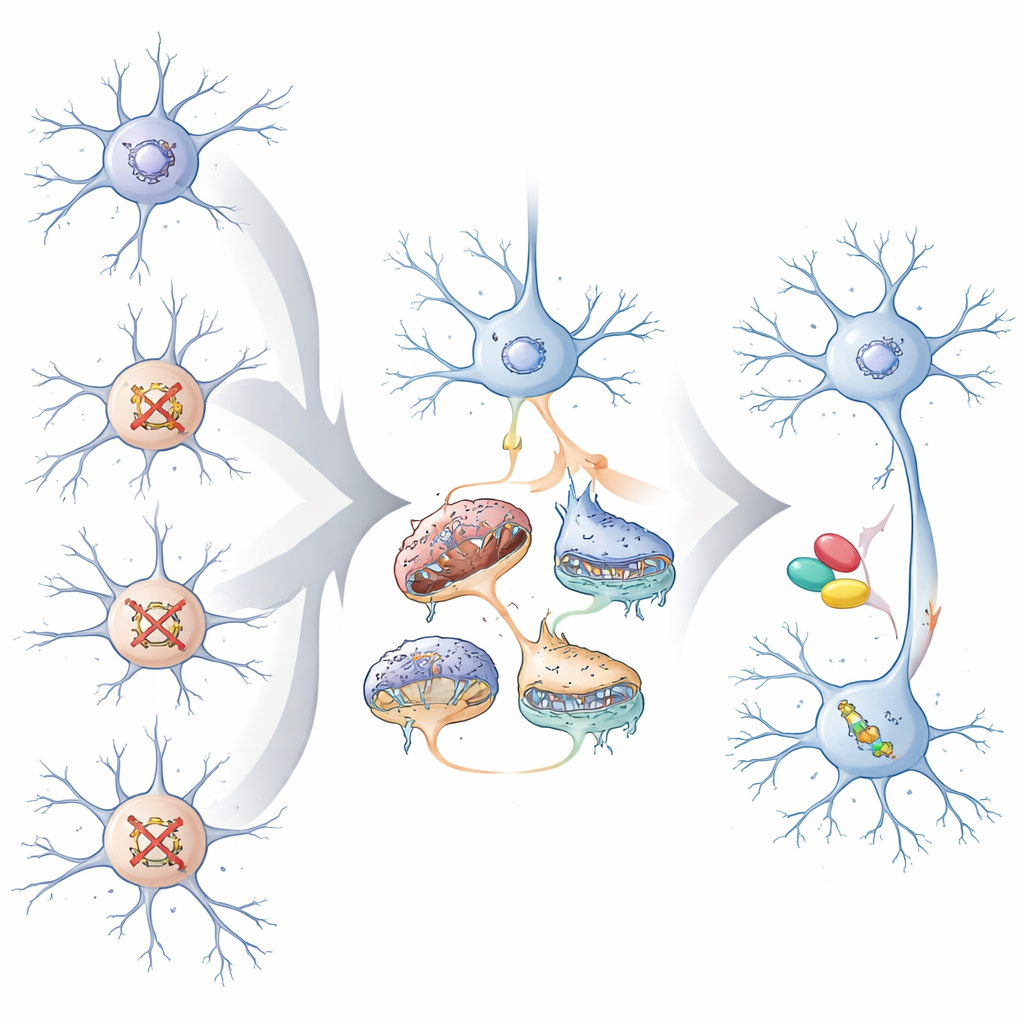
Varför detta betyder något för framtida behandlingar
För en icke-specialist är huvudbudskapet att mycket olika gener kopplade till autism och utvecklingsförsening kan driva hjärnceller mot en mindre uppsättning gemensamma problem, särskilt i de excitatoriska neuroner som driver kortikala kretsar. Dessa gemensamma problem inkluderar hur synapser fungerar, hur genaktivitet regleras och hur mitokondrier levererar energi. Genom att kartlägga dessa konvergenta vägar antyder studien att behandlingar en dag kanske kan matchas inte bara till en persons specifika mutation, utan till de delade cellulära "felsprickor" som mutationen aktiverar. Zebrafiskexperimenten antyder att riktade insatser mot dessa gemensamma vägar, även efter att hjärnan utvecklats, delvis kan normalisera beteende, vilket ger hopp om att konvergerande biologi kan vägleda mer precisa och brett användbara terapier.
Citering: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Nyckelord: autismgenetik, neurodevelopmentala störningar, excitatoriska neuroner, mitokondriell funktion, zebrafiskbeteende