Clear Sky Science · pt
Convergência transcriptômica e fenotípica de genes de risco para transtornos do neurodesenvolvimento in vitro e in vivo
Por que genes diferentes podem causar desafios cerebrais semelhantes
Muitas crianças diagnosticadas com autismo ou atraso no desenvolvimento carregam mutações genéticas bem distintas, mas frequentemente apresentam problemas semelhantes de aprendizagem, comportamento ou sensibilidade sensorial. Este estudo parte de uma pergunta aparentemente simples, com implicações amplas: quando dezenas de genes de risco distintos são alterados, eles acabam perturbando os mesmos processos centrais nas células cerebrais, e esses pontos frágeis compartilhados poderiam orientar tratamentos futuros?
Analisando muitos genes em células cerebrais ao mesmo tempo
Os pesquisadores focaram em 23 genes de alto impacto ligados a transtornos do neurodesenvolvimento que, em sua maioria, regulam como o DNA é empacotado e lido, além de alguns essenciais para a comunicação entre neurônios. Usando células-tronco humanas, eles cultivaram três tipos celulares-chave do córtex em desenvolvimento: células progenitoras neurais em divisão, neurônios excitatórios (glutamatérgicos) que estimulam a atividade cerebral, e neurônios inibitórios (GABAérgicos) que a moderam. Com uma abordagem CRISPR em pool, desligaram cada gene de risco em milhares de células individuais e mediram quais outros genes nessas células aumentaram ou diminuíram sua expressão. Isso permitiu ver, através de muitas mutações diferentes, onde seus efeitos downstream "convergiam" sobre os mesmos conjuntos de genes ou vias.
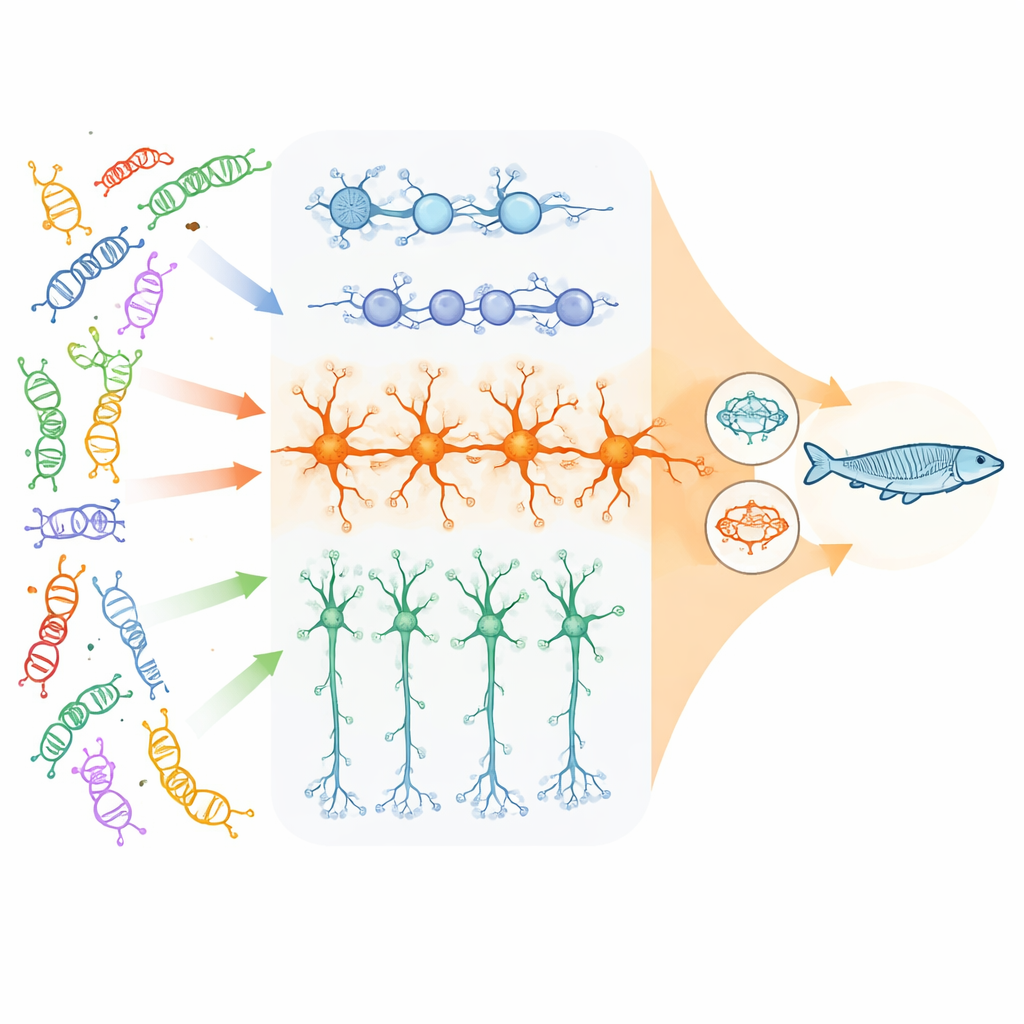
A convergência é mais forte em neurônios excitatórios
A equipe constatou que a convergência depende fortemente do tipo celular e do estágio de desenvolvimento. Embora cada knockout deixasse sua própria assinatura, as alterações compartilhadas mais extensas e fortemente conectadas apareceram em neurônios excitatórios maduros. Ali, milhares de genes foram alterados de maneira similar em muitos genes de risco distintos. As redes afetadas giravam em torno de três temas: sinapses (as junções onde os neurônios se comunicam), a maquinaria celular que controla quais genes são ativados ou silenciados, e, de forma inesperada, as mitocôndrias — as usinas de energia da célula. Em contraste, progenitores neurais mostraram principalmente mudanças compartilhadas em divisão celular e vias de crescimento inicial do cérebro, e neurônios inibitórios exibiram padrões de convergência mais modestos e distintos.
Das redes genéticas à função cerebral e ao comportamento
Para testar se essas mudanças convergentes importam para a doença, os autores compararam as assinaturas gênicas compartilhadas com grandes estudos genéticos de condições psiquiátricas. Os genes e redes convergentes em neurônios excitatórios estavam enriquecidos para variantes de risco associadas ao autismo, esquizofrenia e deficiência intelectual, além de alvos conhecidos da proteína Fragile X. Modelos de aprendizado de máquina treinados com esses dados previram que, entre mais de 100 genes de risco para o neurodesenvolvimento, aqueles mais ligados ao autismo tendem a convergir em neurônios excitatórios, enquanto os mais associados ao atraso global do desenvolvimento convergem em neurônios inibitórios. A equipe também mostrou experimentalmente que vários genes de risco representativos, quando perturbados individualmente, produziram problemas distintos porém relacionados na geração de novos neurônios e na estrutura e consumo de oxigênio das mitocôndrias — correspondendo aos padrões convergentes observados nas telas em pool.
Testando a convergência em animais vivos e com fármacos
Como culturas celulares não capturam circuitos cerebrais completos ou comportamento, os pesquisadores recorreram a zebrafish com mutações em um subconjunto dos mesmos genes. O rastreamento automatizado do sono, excitação e respostas de sobressalto agrupou esses peixes em quatro “conjuntos” comportamentais com padrões semelhantes, como sono alterado ou sensibilidade aumentada a mudanças de luz. Ao sobrepor esses agrupamentos comportamentais com os dados de células humanas, os autores encontraram que cada conjunto estava associado a seu próprio padrão de genes convergentes, novamente mais forte em neurônios excitatórios. Em seguida, usaram bancos de dados de resposta a medicamentos e triagens prévias em zebrafish para prever compostos que pudessem reverter as assinaturas convergentes e antagonizar os comportamentos mutantes. Em testes subsequentes, 10 dos 11 fármacos selecionados melhoraram ao menos um comportamento anômalo nos zebrafish mutantes, e alguns produziram resgates marcantes do sono ou das respostas sensoriais.
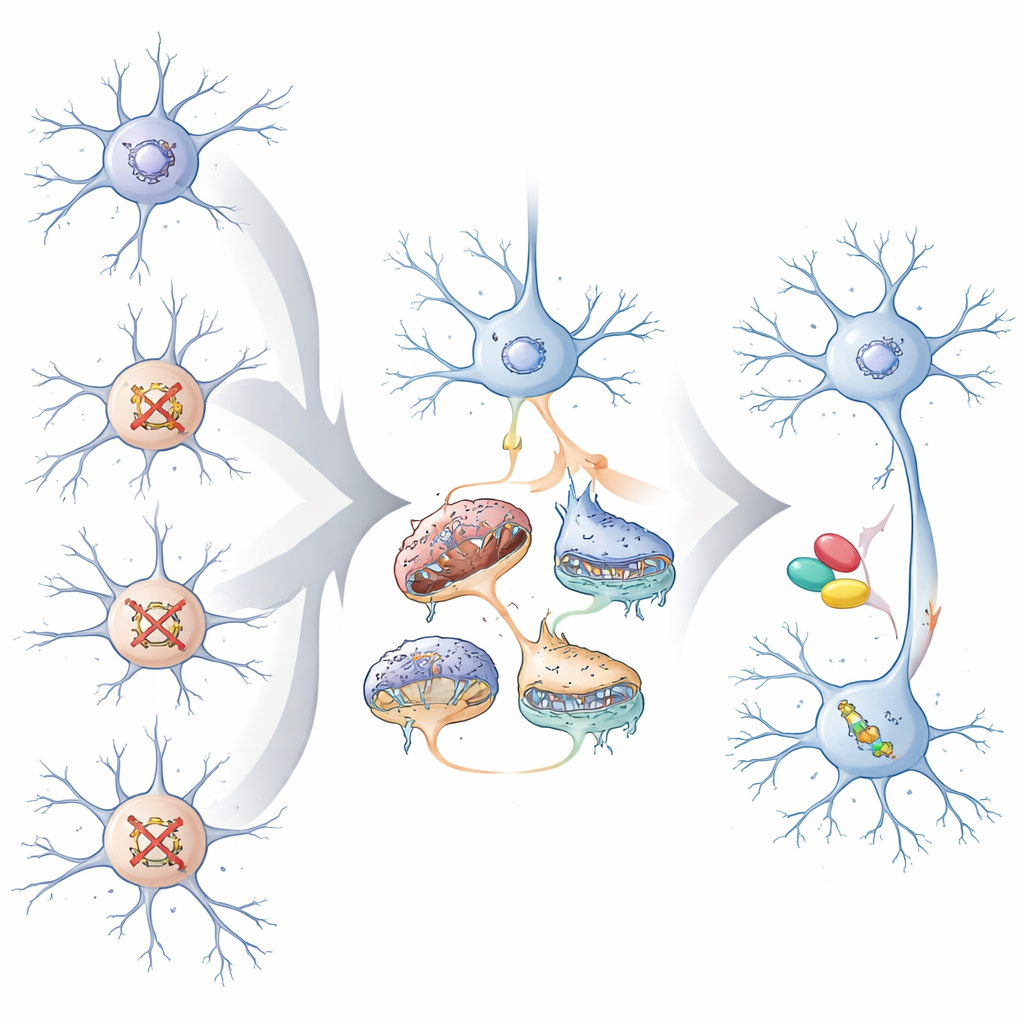
Por que isso importa para tratamentos futuros
Para um não-especialista, a mensagem principal é que genes muito diferentes relacionados ao autismo e a atrasos no desenvolvimento podem empurrar as células cerebrais para um conjunto menor de problemas compartilhados, especialmente nos neurônios excitatórios que impulsionam os circuitos corticais. Esses problemas comuns incluem o funcionamento das sinapses, o controle da atividade gênica e o fornecimento de energia pelas mitocôndrias. Ao mapear essas vias convergentes, o estudo sugere que tratamentos, no futuro, poderiam ser ajustados não apenas à mutação específica de uma pessoa, mas às “falhas” celulares compartilhadas que essa mutação ativa. Os experimentos em zebrafish indicam que mirar essas vias comuns, mesmo após o desenvolvimento cerebral, pode normalizar parcialmente o comportamento, levantando a esperança de que a biologia convergente possa orientar terapias mais precisas e amplamente úteis.
Citação: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Palavras-chave: genética do autismo, transtornos do neurodesenvolvimento, neurônios excitatórios, função mitocondrial, comportamento de zebrafish