Clear Sky Science · nl
Transcriptomische en fenotypische convergentie van risicogenen voor neuro-ontwikkelingsstoornissen in vitro en in vivo
Waarom verschillende genen vergelijkbare hersenproblemen kunnen veroorzaken
Veel kinderen met een diagnose autisme of ontwikkelingsachterstand hebben heel verschillende genetische mutaties, maar vertonen vaak vergelijkbare problemen op het gebied van leren, gedrag of zintuigelijke verwerking. Deze studie stelt een schijnbaar eenvoudige maar ingrijpende vraag: wanneer tientallen verschillende risicogenen worden aangepast, verstoren ze dan uiteindelijk dezelfde kernprocessen in hersencellen, en zouden die gedeelde kwetsbare plekken kunnen worden gebruikt om toekomstige behandelingen te sturen?
Veel genen tegelijk bestuderen in hersencellen
De onderzoekers concentreerden zich op 23 hoog-impact genen die gelinkt zijn aan neuro-ontwikkelingsstoornissen en die grotendeels helpen bepalen hoe DNA wordt verpakt en afgelezen, plus een paar genen die essentieel zijn voor communicatie tussen zenuwcellen. Met menselijke stamcellen kweekten ze drie belangrijke celtypen uit de zich ontwikkelende cortex: delende neurale progenitorcellen, exciterende (glutamaterge) neuronen die hersenactiviteit stimuleren, en inhibitorische (GABAerge) neuronen die die activiteit dempen. Met een pooled CRISPR-benadering schakelden ze elk risicogen uit in duizenden individuele cellen en maten vervolgens welke andere genen in die cellen omhoog- of omlaagreguleerden. Zo konden ze zien, over veel verschillende mutaties heen, waar hun downstream-effecten ‘convergeren’ op dezelfde sets genen of paden.
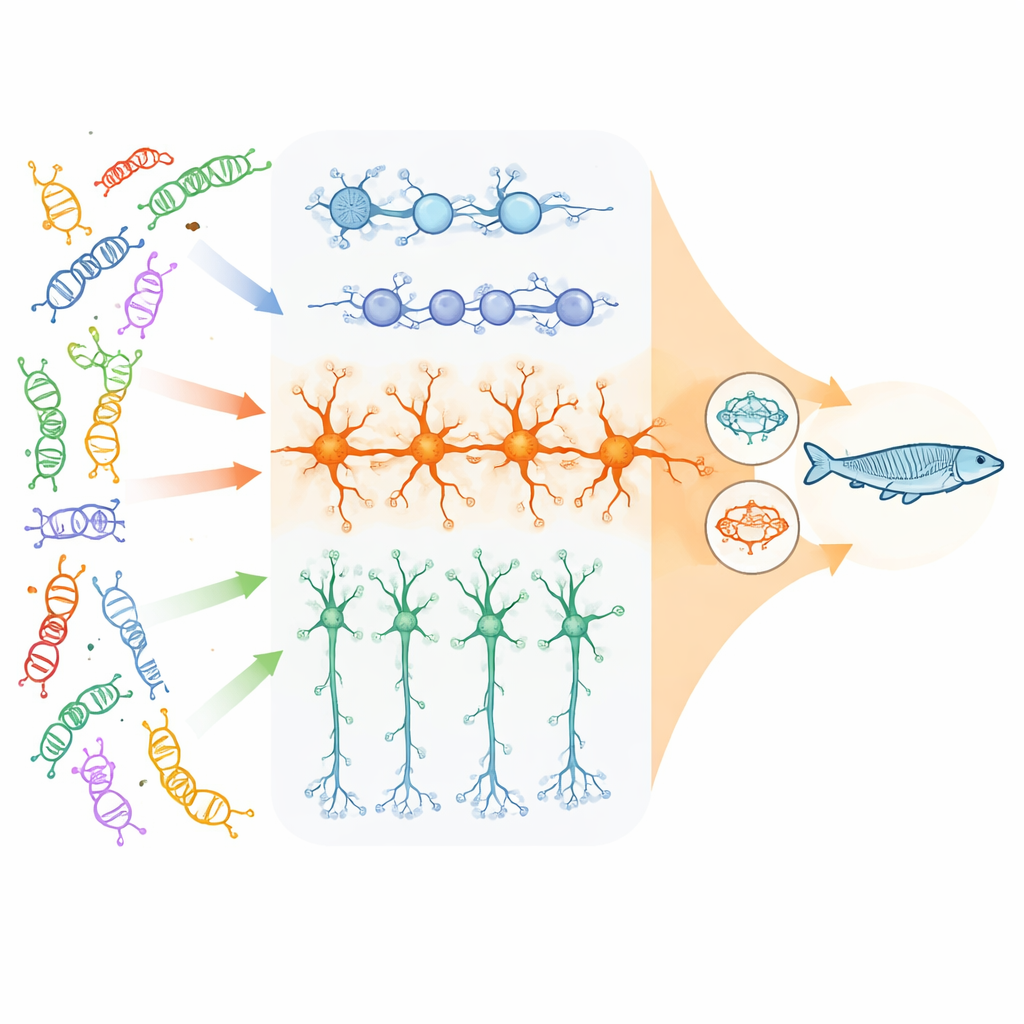
Convergentie is het sterkst in exciterende neuronen
Het team vond dat convergentie sterk afhankelijk is van celtype en ontwikkelingsstadium. Hoewel elke genknockout zijn eigen vingerafdruk achterliet, verschenen de meest uitgebreide en nauw verbonden gedeelde veranderingen in rijpe exciterende neuronen. Hier werden duizenden genen op vergelijkbare manieren veranderd over veel verschillende risicogenen heen. De aangetaste netwerken concentreerden zich rond drie thema’s: synapsen (de verbindingen waarlangs neuronen communiceren), de cellulaire machinerie die regelt welke genen aan- of uitgezet worden, en – verrassend genoeg – mitochondriën, de energiecentrales van de cel. Ter vergelijking lieten neurale progenitoren vooral gedeelde veranderingen zien in celdeling en vroege groeipaden van de hersenen, en inhibitorische neuronen toonden meer bescheiden en onderscheiden convergentiepatronen.
Van gen-netwerken naar hersenfunctie en gedrag
Om te testen of deze convergerende veranderingen van belang zijn voor ziekte, vergeleken de auteurs de gedeelde genesignaturen met grote genetische studies van psychiatrische omstandigheden. De convergerende genen en netwerken in exciterende neuronen waren verrijkt voor risicovarianten die geassocieerd zijn met autisme, schizofrenie en verstandelijke beperking, evenals bekende doelwitten van het Fragiele X-eiwit. Machine-learningmodellen getraind op deze gegevens voorspelden dat, over meer dan 100 bekende risicogenen voor neuro-ontwikkelingsstoornissen, die voornamelijk aan autisme gekoppeld zijn de neiging hebben te convergeren in exciterende neuronen, terwijl genen die meer verband houden met algemene ontwikkelingsachterstand convergeren in inhibitorische neuronen. Het team toonde experimenteel ook aan dat meerdere representatieve risicogenen, wanneer afzonderlijk verstoord, onderscheidende maar verwante problemen veroorzaakten in hoe neuronen nieuwe cellen genereren en in hoe hun mitochondriën zijn gestructureerd en zuurstof verbruiken — wat overeenkomt met de convergente patronen gezien in de pooled screens.
Convergentie testen in levende dieren en met geneesmiddelen
Aangezien kweekcellen geen hele-hersen-circuits of gedrag kunnen vastleggen, gebruikten de onderzoekers zebravissen met mutaties in een subgroep van dezelfde genen. Geautomatiseerde registratie van slaap, arousal en schrikresponsen groepeerde deze vissen in vier gedragsmatige “sets” met vergelijkbare patronen, zoals veranderde slaap of verhoogde gevoeligheid voor lichtveranderingen. Toen de auteurs deze gedragsgroepen overlayden met hun humane celgegevens, vonden ze dat elke set geassocieerd was met zijn eigen patroon van convergerende genen, opnieuw het sterkst in exciterende neuronen. Vervolgens gebruikten ze geneesmiddelresponsdatabases en eerdere zebravis-geneesmidddelen-screens om medicijnen te voorspellen die de convergerende signaturen zouden kunnen omkeren en de mutantgedragingen zouden kunnen tegenwerken. In vervolgtests verbeterden 10 van de 11 geselecteerde geneesmiddelen ten minste één abnormaal gedrag bij de zebravismutanten, en sommige leverden opvallend herstel van slaap- of zintuiglijke responsen.
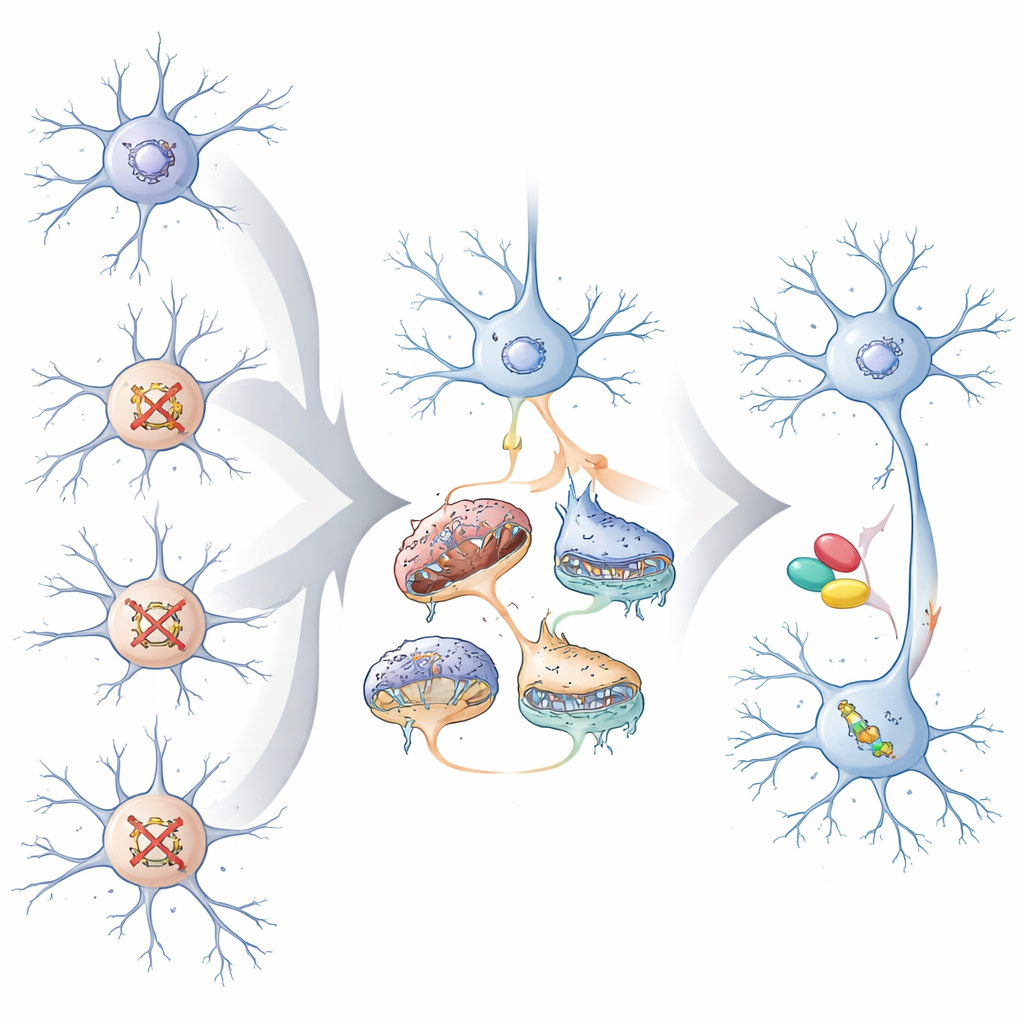
Waarom dit belangrijk is voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat heel verschillende aan autisme en ontwikkelingsachterstand gerelateerde genen hersencellen naar een kleiner aantal gedeelde problemen kunnen duwen, vooral in de exciterende neuronen die corticale circuits aansturen. Deze gemeenschappelijke problemen omvatten hoe synapsen functioneren, hoe genactiviteit wordt gecontroleerd en hoe mitochondriën energie leveren. Door deze convergerende paden in kaart te brengen, suggereert de studie dat behandelingen zich in de toekomst mogelijk niet alleen op iemands specifieke mutatie hoeven te richten, maar op de gedeelde cellulaire “breuklijnen” die die mutatie activeert. De zebravisexperimenten wijzen erop dat het richten op deze gedeelde paden, zelfs nadat de hersenen ontwikkeld zijn, gedrag deels kan normaliseren, wat hoop biedt dat convergente biologie kan leiden tot preciezere en breder toepasbare therapieën.
Bronvermelding: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Trefwoorden: autismegenetica, neuro-ontwikkelingsstoornissen, exciterende neuronen, mitochondriale functie, zebravisgedrag