Clear Sky Science · ja
in vitro と in vivo における神経発達障害リスク遺伝子のトランスクリプトームおよび表現型の収斂
異なる遺伝子がなぜ似た脳の問題を引き起こすのか
自閉症や発達遅滞と診断される多くの子どもは、非常に異なる遺伝子変異を持っていますが、学習、行動、感覚に関する似たような問題を共有することがよくあります。本研究は一見単純だが重要な問いを投げかけます:数十種類の異なるリスク遺伝子が変化したとき、それらは最終的に脳細胞の同じ核心的過程を乱すのか。そして、そうした共有された弱点は将来の治療の指針になり得るのか?
多数の遺伝子を同時に脳細胞で観察する
研究者らは、主にDNAのパッケージングと読み取りを制御する23の高影響リスク遺伝子と、神経細胞間の通信に不可欠な数遺伝子に注目しました。ヒト幹細胞を用い、発達中の大脳皮質に存在する主要な3種類の細胞を作り出しました:分裂する神経前駆細胞、脳活動を促進する興奮性(グルタミン酸作動性)ニューロン、そしてそれを抑制する抑制性(GABA作動性)ニューロンです。プール型CRISPRアプローチを用いて、数千の単一細胞で各リスク遺伝子をノックアウトし、その細胞内でどの遺伝子が上方または下方に変動するかを測定しました。これにより、多数の異なる変異にわたって、その下流効果がどの遺伝子群や経路に「収斂」するかを横断的に見ることができました。
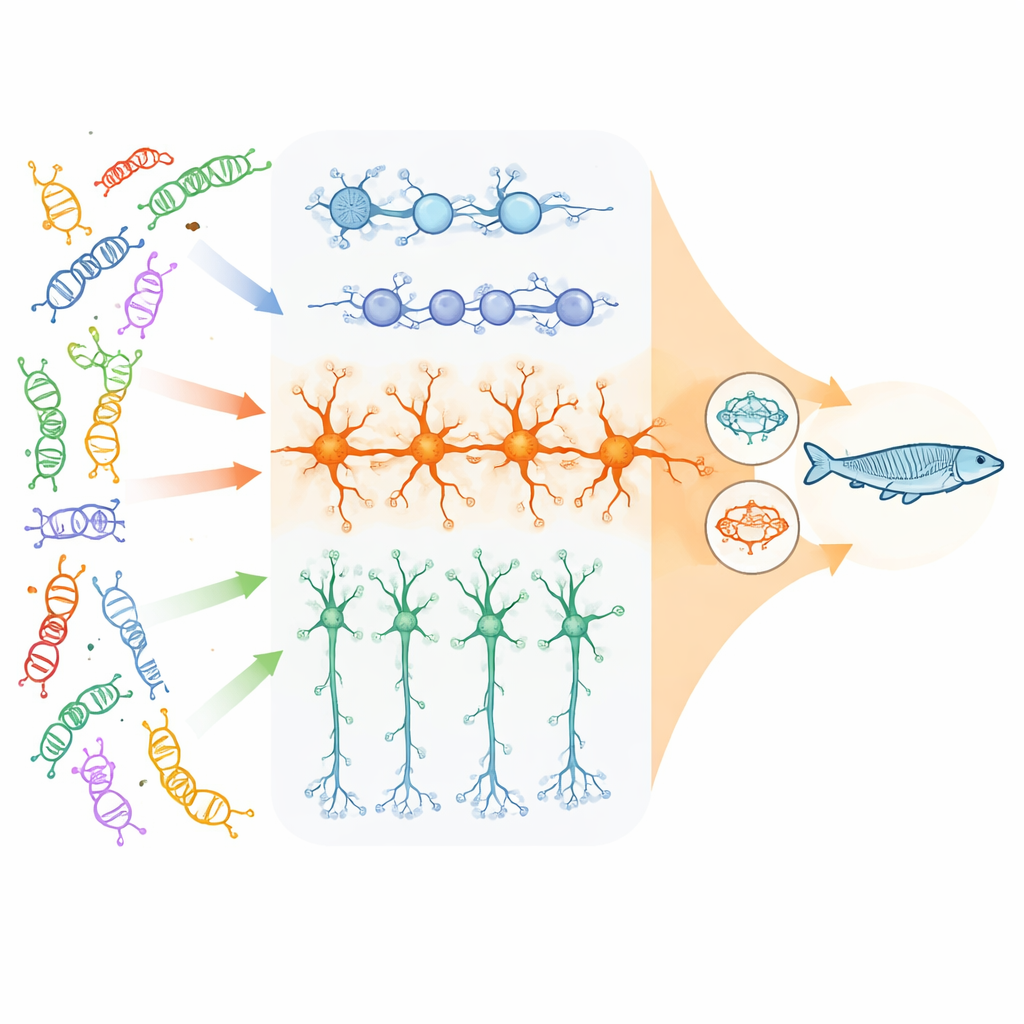
収斂は興奮性ニューロンで最も顕著
チームは、収斂が細胞型と発達段階に強く依存することを見出しました。各遺伝子ノックアウトは固有のフィンガープリントを残しましたが、最も広範で緊密に結びついた共有変化は成熟した興奮性ニューロンで現れました。ここでは、多数のリスク遺伝子に共通して数千の遺伝子が類似した変動を示しました。影響を受けたネットワークは三つの主題に集中していました:シナプス(ニューロンがやり取りする接合部)、どの遺伝子がオン/オフされるかを制御する細胞内装置、そして予想外にミトコンドリア—細胞のエネルギー工場です。対照的に、神経前駆細胞では主に細胞分裂や初期脳成長経路の共有変化が見られ、抑制性ニューロンではより控えめで特徴の異なる収斂パターンが観察されました。
遺伝子ネットワークから脳機能と行動へ
これらの収斂する変化が疾患にとって重要かどうかを検証するため、著者らは共有遺伝子署名を精神疾患に関する大規模な遺伝学研究と比較しました。興奮性ニューロンにおける収斂遺伝子およびネットワークは、自閉症、統合失調症、知的障害に関連するリスク変異と富化しており、Fragile Xタンパク質の既知の標的とも一致していました。これらのデータで学習した機械学習モデルは、100以上の既知の神経発達リスク遺伝子全体にわたり、自閉症に主に結びつく遺伝子は興奮性ニューロンで収斂する傾向があり、全般的な発達遅滞に結びつくものは抑制性ニューロンで収斂する傾向があると予測しました。さらに、代表的な複数のリスク遺伝子を個別に破壊すると、ニューロンの新生やミトコンドリアの構造と酸素消費に関して、異なるが関連した問題が生じることを実験的に示し—これらはプールスクリーンで観察された収斂パターンと一致しました。
生体内と薬物で収斂を検証する
細胞培養では全脳回路や行動を再現できないため、研究者らは同じ遺伝子のサブセットに変異を持つゼブラフィッシュに注目しました。睡眠、覚醒、驚愕反応の自動追跡により、これらの魚は睡眠の変化や光変化への過敏性などの類似パターンを示す4つの行動「セット」に分類されました。著者らがこれらの行動群をヒト細胞データに重ね合わせると、それぞれのセットが再び興奮性ニューロンで最も強い独自の収斂遺伝子パターンと関連していることが分かりました。続いて、薬物応答データベースと既往のゼブラフィッシュ薬物スクリーニングを用いて、収斂署名を逆転させ変異行動に対抗する可能性のある薬を予測しました。追試では、選択した11薬のうち10薬が少なくとも1つの異常行動を改善し、一部は睡眠や感覚応答の顕著な回復を示しました。
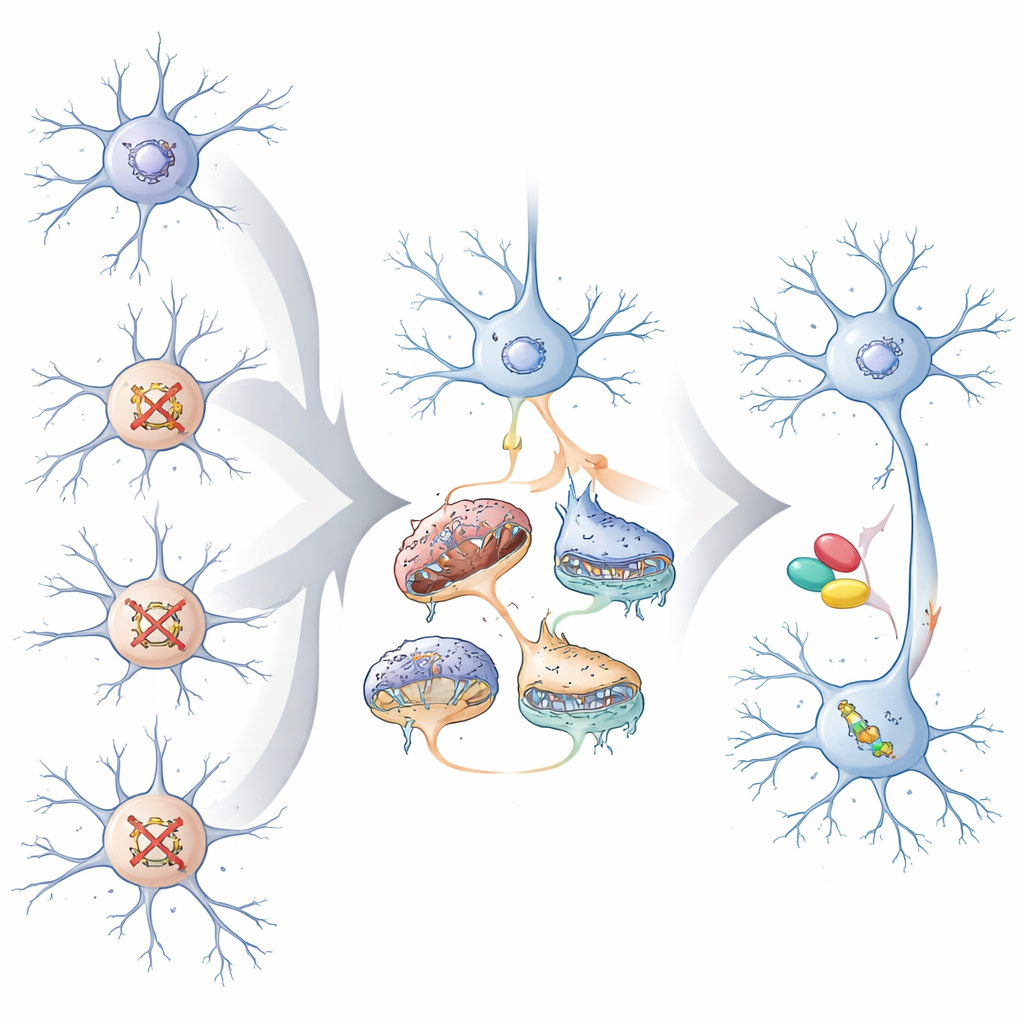
将来の治療への意義
専門外の人にとっての要点は、非常に異なる自閉症や発達遅滞関連遺伝子が、特に皮質回路を駆動する興奮性ニューロンにおいて、より小さな共通の問題へと脳細胞を傾ける可能性があるということです。これらの共通問題には、シナプスの機能、遺伝子活動の制御のあり方、ミトコンドリアによるエネルギー供給が含まれます。これらの収斂経路を描き出すことで、治療は将来的に個々の変異にだけ合わせるのではなく、その変異が引き起こす共有された細胞レベルの「断層線」に合わせて選ばれる可能性が示唆されます。ゼブラフィッシュの実験は、脳が発達した後でもこれらの共有経路を標的にすることで行動を部分的に正常化できることを示唆しており、収斂する生物学がより精密で幅広く有用な治療を導く可能性に希望を与えます。
引用: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
キーワード: 自閉症遺伝学, 神経発達障害, 興奮性ニューロン, ミトコンドリア機能, ゼブラフィッシュの行動