Clear Sky Science · de
Transkriptomische und phänotypische Konvergenz von Risiko-Genen für neuroentwicklungsstörungen in vitro und in vivo
Warum verschiedene Gene ähnliche Probleme im Gehirn hervorrufen können
Viele Kinder mit einer Diagnose von Autismus oder Entwicklungsverzögerung tragen sehr unterschiedliche genetische Veränderungen, zeigen aber oft ähnliche Lern-, Verhaltens- oder Sinnesauffälligkeiten. Diese Studie stellt eine auf den ersten Blick einfache, aber weitreichende Frage: Wenn Dutzende verschiedener Risikogene verändert werden, stören sie dann schließlich dieselben Kernprozesse in Gehirnzellen, und könnten diese gemeinsamen Schwachstellen für künftige Behandlungen nutzbar sein?
Viele Gene gleichzeitig in Gehirnzellen untersuchen
Die Forschenden konzentrierten sich auf 23 hochwirksame Gene, die mit neuroentwicklungsstörungen verknüpft sind und größtenteils die Verpackung und Ablesung von DNA steuern, sowie einige wenige, die für die Kommunikation zwischen Nervenzellen essenziell sind. Mit menschlichen Stammzellen züchteten sie drei Schlüsselzelltypen des sich entwickelnden Kortex: teilende neuronale Vorläuferzellen, exzitatorische (glutamaterge) Neuronen, die die Hirnaktivität anregen, und inhibitorische (GABAerge) Neuronen, die sie dämpfen. Mit einem gepoolten CRISPR-Ansatz schalteten sie jedes Risikogen in Tausenden einzelner Zellen aus und maßen anschließend, welche anderen Gene in diesen Zellen hoch- oder herunterreguliert wurden. So konnten sie über viele verschiedene Mutationen hinweg erkennen, wo deren nachgeschaltete Effekte in denselben Gen- oder Signalwegen „konvergierten“.
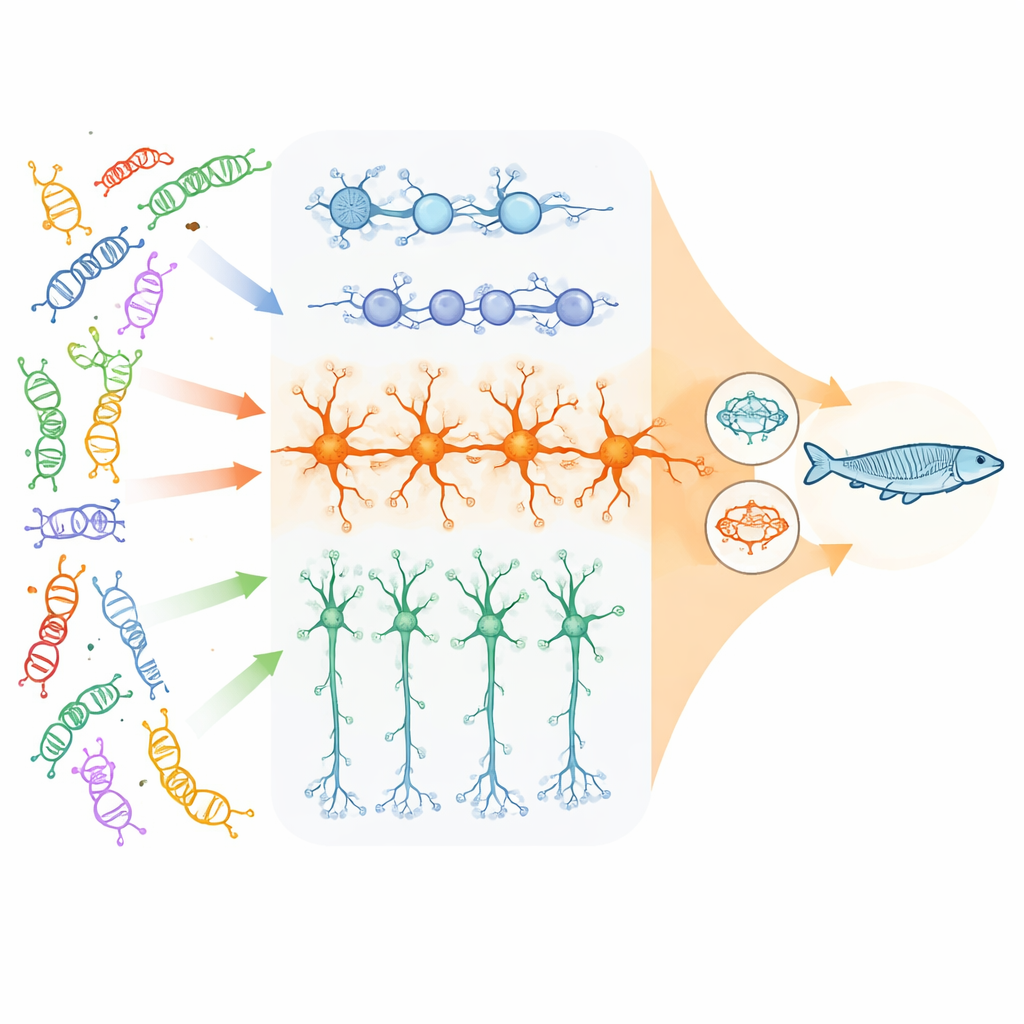
Konvergenz ist am stärksten in exzitatorischen Neuronen
Das Team fand heraus, dass die Konvergenz stark vom Zelltyp und dem Entwicklungsstadium abhängt. Während jedes Gen-Knockout seine eigene Signatur hinterließ, traten die umfangreichsten und eng vernetzten gemeinsamen Veränderungen in ausgereiften exzitatorischen Neuronen auf. Hier wurden tausende Gene über viele verschiedene Risikogene auf ähnliche Weise verändert. Die betroffenen Netzwerke konzentrierten sich auf drei Themen: Synapsen (die Kontaktstellen, an denen Neuronen kommunizieren), die zelluläre Maschinerie, die steuert, welche Gene an- oder ausgeschaltet werden, und unerwartet die Mitochondrien — die Energiefabriken der Zelle. Im Gegensatz dazu zeigten neuronale Vorläufer vor allem gemeinsame Änderungen in Zellteilungs- und frühen Wachstumswegen des Gehirns, und inhibitorische Neuronen wiesen bescheidenere und unterschiedliche Konvergenzmuster auf.
Von Gen-Netzwerken zu Gehirnfunktion und Verhalten
Um zu prüfen, ob diese konvergierenden Veränderungen für die Krankheit relevant sind, verglichen die Autorinnen und Autoren die gemeinsamen Gen-Signaturen mit großen genetischen Studien zu psychiatrischen Erkrankungen. Die konvergenten Gene und Netzwerke in exzitatorischen Neuronen waren angereichert für Risikovarianten, die mit Autismus, Schizophrenie und geistiger Behinderung verknüpft sind, sowie für bekannte Ziele des Fragilen-X-Proteins. Auf maschinellem Lernen basierende Modelle, die mit diesen Daten trainiert wurden, sagten voraus, dass sich — über mehr als 100 bekannte Risiko-Gene für Neuroentwicklung — solche, die vorrangig mit Autismus verbunden sind, tendenziell in exzitatorischen Neuronen konvergieren, während Gene, die stärker mit globaler Entwicklungsverzögerung assoziiert sind, in inhibitorischen Neuronen konvergieren. Experimentell zeigten die Forschenden außerdem, dass mehrere repräsentative Risikogene, einzeln gestört, unterschiedliche, aber verwandte Probleme in der Zellneubildung von Neuronen sowie in der Struktur und dem Sauerstoffverbrauch ihrer Mitochondrien hervorriefen — übereinstimmend mit den in den gepoolten Screens beobachteten konvergenten Mustern.
Konvergenz in lebenden Tieren und durch Medikamente testen
Da Zellkulturen keine kompletten Gehirnschaltkreise oder Verhalten abbilden können, wandten sich die Forschenden Zebrafischen zu, die Mutationen in einer Teilmenge derselben Gene tragen. Automatisierte Erfassung von Schlaf, Erregbarkeit und Schreckreaktionen gruppierte diese Fische in vier Verhaltens"sets" mit ähnlichen Mustern, etwa verändertem Schlaf oder erhöhter Lichtempfindlichkeit. Als die Autorinnen und Autoren diese Verhaltensgruppierungen mit ihren menschlichen Zell-Daten überlagerten, stellten sie fest, dass jedes Set mit seinem eigenen Muster konvergenter Gene assoziiert war, wiederum am stärksten in exzitatorischen Neuronen. Anschließend nutzten sie Datenbanken zu Wirkstoffantworten und frühere Zebrafisch-Drugscreens, um Medikamente vorherzusagen, die die konvergenten Signaturen umkehren und die mutanten Verhaltensweisen entgegenwirken könnten. In Folgetests verbesserten 10 von 11 ausgewählten Wirkstoffen mindestens ein abnormes Verhalten der Zebrafischmutanten, und einige bewirkten eine auffällige Normalisierung von Schlaf- oder Sensorik-Antworten.
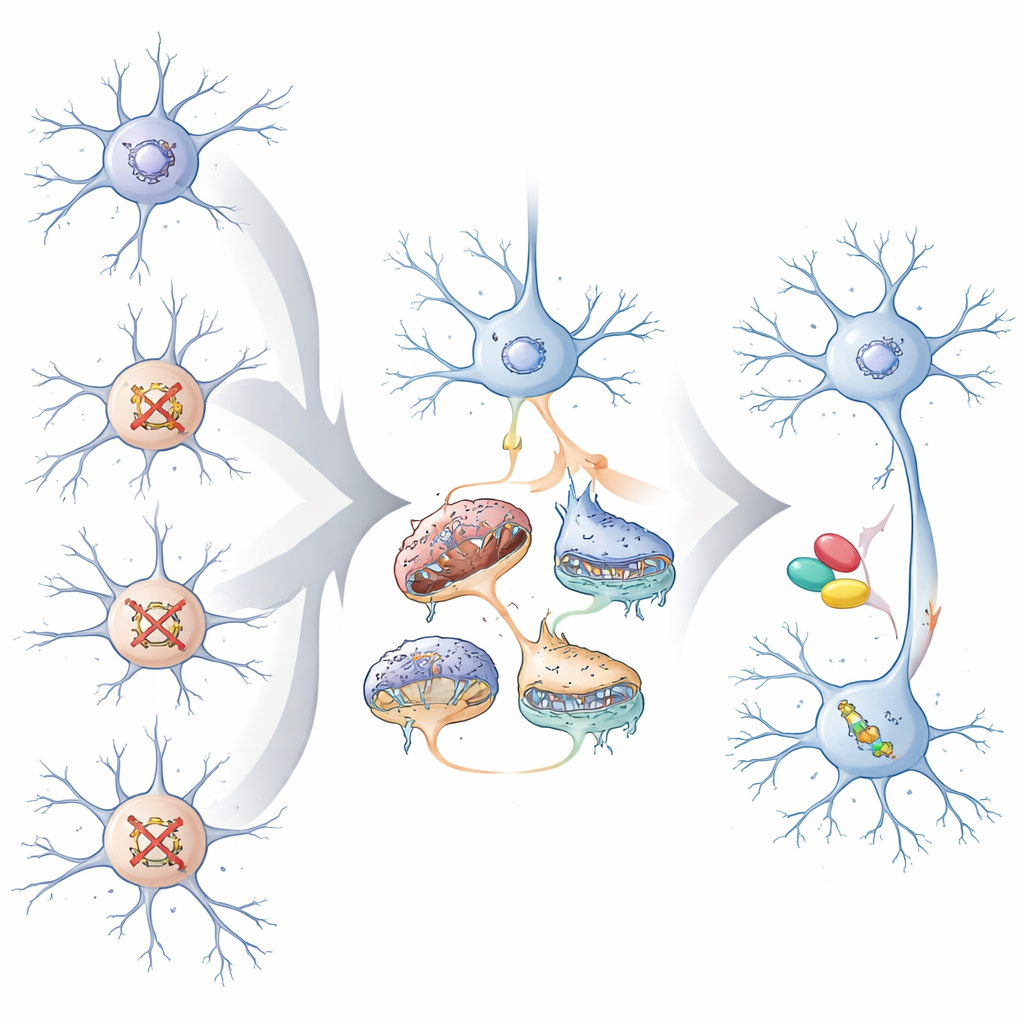
Warum das für künftige Behandlungen wichtig ist
Für Nicht-Fachleute lautet die Kernbotschaft: Sehr unterschiedliche mit Autismus und Entwicklungsverzögerung verbundene Gene können Gehirnzellen auf eine kleinere Menge gemeinsamer Probleme zusteuern, besonders in den exzitatorischen Neuronen, die kortikale Schaltkreise antreiben. Zu diesen gemeinsamen Problemen zählen die Funktionsweise von Synapsen, die Kontrolle der Genaktivität und die Energieversorgung durch Mitochondrien. Indem diese konvergenten Wege kartiert werden, legt die Studie nahe, dass Therapien eines Tages nicht nur auf eine bestimmte Mutation einer Person zugeschnitten sein könnten, sondern auf die gemeinsamen zellulären „Bruchlinien“, die diese Mutation aktiviert. Die Zebrafisch-Experimente deuten darauf hin, dass die gezielte Beeinflussung dieser gemeinsamen Wege, selbst nachdem das Gehirn sich entwickelt hat, Verhalten teilweise normalisieren kann — was die Hoffnung nährt, dass konvergente Biologie präzisere und breit anwendbare Therapien leiten könnte.
Zitation: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Schlüsselwörter: Autismus-Genetik, neuroentwicklungsstörungen, exzitatorische Neuronen, mitochondriale Funktion, Verhalten von Zebrafischen