Clear Sky Science · ru
Транскриптомная и фенотипическая конвергенция генов риска нейроразвития in vitro и in vivo
Почему разные гены могут вызывать похожие проблемы мозга
У многих детей с диагнозом аутизм или задержка развития встречаются очень разные генетические нарушения, но при этом часто проявляются схожие трудности в обучении, поведении или восприятии. В этом исследовании поставлен на первый взгляд простой, но важный вопрос: когда десятки различных генов риска изменены, не нарушают ли они одни и те же ключевые процессы в нейронах, и можно ли использовать эти общие уязвимости для разработки будущих методов лечения?
Изучение многих генов одновременно в клетках мозга
Авторы сосредоточились на 23 генах с высоким вкладом в риск нейроразвитных расстройств, большинство из которых участвует в контроле упаковки и считывания ДНК, а также на нескольких генах, важнейших для передачи сигналов между нейронами. Используя человеческие стволовые клетки, они получили три ключевых типа клеток, присутствующие в развивающейся коре: делящиеся нейральные прогениторные клетки, возбуждающие (глутаматергические) нейроны, которые стимулируют активность мозга, и тормозные (ГАМКергические) нейроны, которые её подавляют. С помощью объединённого (pooled) подхода CRISPR они инактивировали каждый ген риска в тысячах отдельных клеток и затем измеряли, какие другие гены в этих клетках повышали или понижали экспрессию. Это позволило увидеть, при разных мутациях, где их последействия «сходятся» на одних и тех же наборах генов или путях.
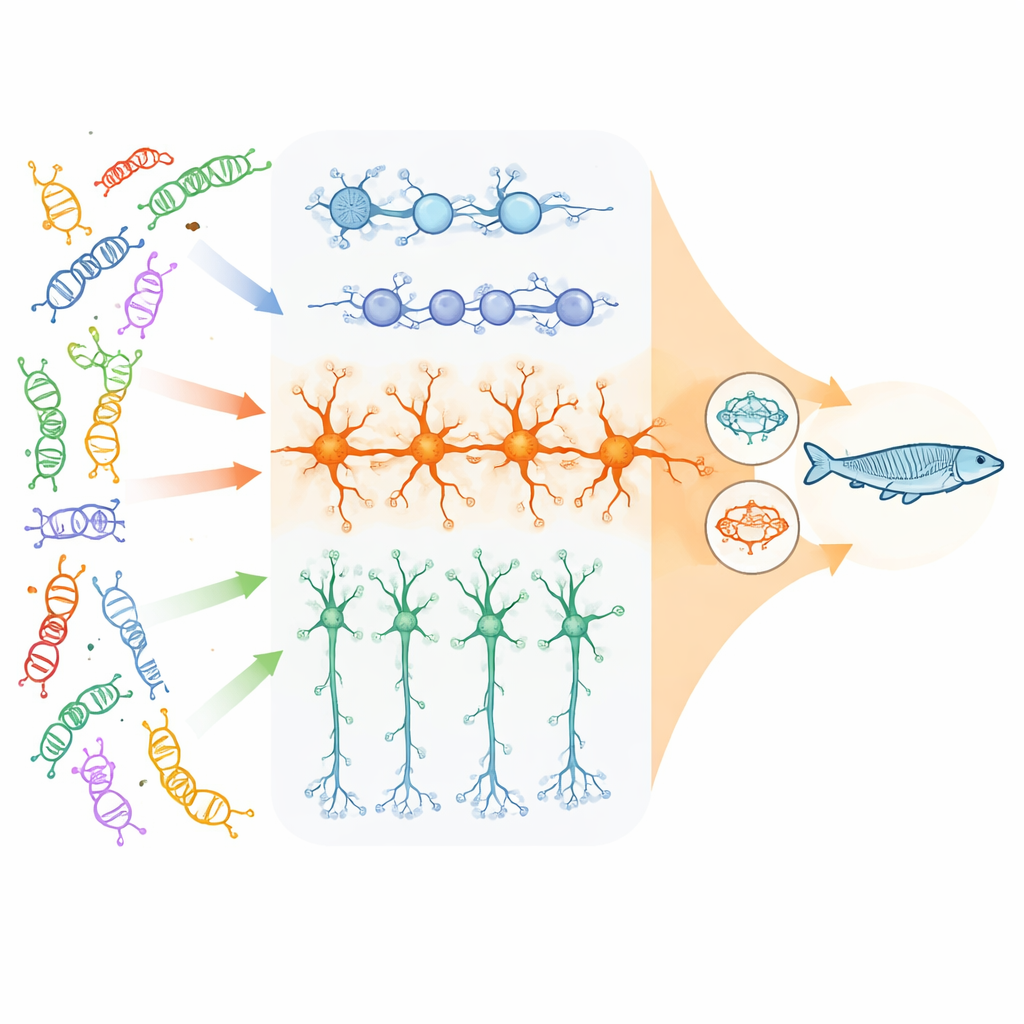
Конвергенция наиболее выражена в возбуждающих нейронах
Исследователи обнаружили, что степень конвергенции сильно зависит от типа клетки и стадии развития. Хотя каждая утрата гена оставляла свою подпись, наиболее широкие и тесно связанные общие изменения проявлялись в зрелых возбуждающих нейронах. Здесь тысячи генов изменяли экспрессию похожим образом при многих различных генетических нарушениях. Затронутые сети объединялись вокруг трёх тем: синапсы (точки контакта и передачи между нейронами), клеточные механизмы, контролирующие, какие гены включены или выключены, и, неожиданно, митохондрии — «энергетические станции» клетки. В то же время прогениторы в основном показывали общие изменения в путях, связанных с делением клеток и ранним ростом мозга, а в тормозных нейронах конвергенция была более скромной и отличалась по паттерну.
От генетических сетей к функции мозга и поведению
Чтобы проверить, имеют ли эти сходящиеся изменения отношение к болезни, авторы сопоставили общие генетические подписи с крупными генетическими исследованиями психических расстройств. Конвергентные гены и сети в возбуждающих нейронах были обогащены вариантами риска, связанными с аутизмом, шизофренией и умственной отсталостью, а также содержали известные мишени белка Fragile X. Модели машинного обучения, обученные на этих данных, предсказали, что среди более чем 100 известных генов риска нейроразвитных расстройств те, которые в основном связаны с аутизмом, склонны конвергировать в возбуждающих нейронах, тогда как гены, больше связанные с глобальной задержкой развития, сходятся в тормозных нейронах. Команда также экспериментально показала, что несколько репрезентативных генов риска, при индивидуальном нарушении, вызывают разные, но связанные проблемы в том, как нейроны образуют новые клетки и как устроены их митохондрии и потребляют кислород — что соответствует наблюдаемым конвергентным паттернам в объединённых скринингах.
Проверка конвергенции в живых животных и подбор лекарств
Поскольку культуры клеток не отражают целые мозговые цепи и поведение, исследователи обратились к данио-рерио (zebrafish) с мутациями в подмножестве тех же генов. Автоматическое отслеживание сна, бодрствования и реакций испуга сгруппировало этих рыб в четыре поведенческих «набора» с похожими паттернами, например изменённым сном или повышенной чувствительностью к изменениям света. Наложив эти поведенческие группы на данные по человеческим клеткам, авторы обнаружили, что каждому набору соответствует свой собственный паттерн конвергентных генов, снова наиболее выраженный в возбуждающих нейронах. Затем они использовали базы данных ответов на лекарства и предыдущие зебрафиш-скрининги, чтобы предсказать препараты, которые могли бы обратить конвергентные подписи и ослабить мутантное поведение. В последующих тестах 10 из 11 отобранных препаратов улучшили по крайней мере одно аномальное поведение у мутантных рыб, причём некоторые давали впечатляющее восстановление сна или сенсорных реакций.
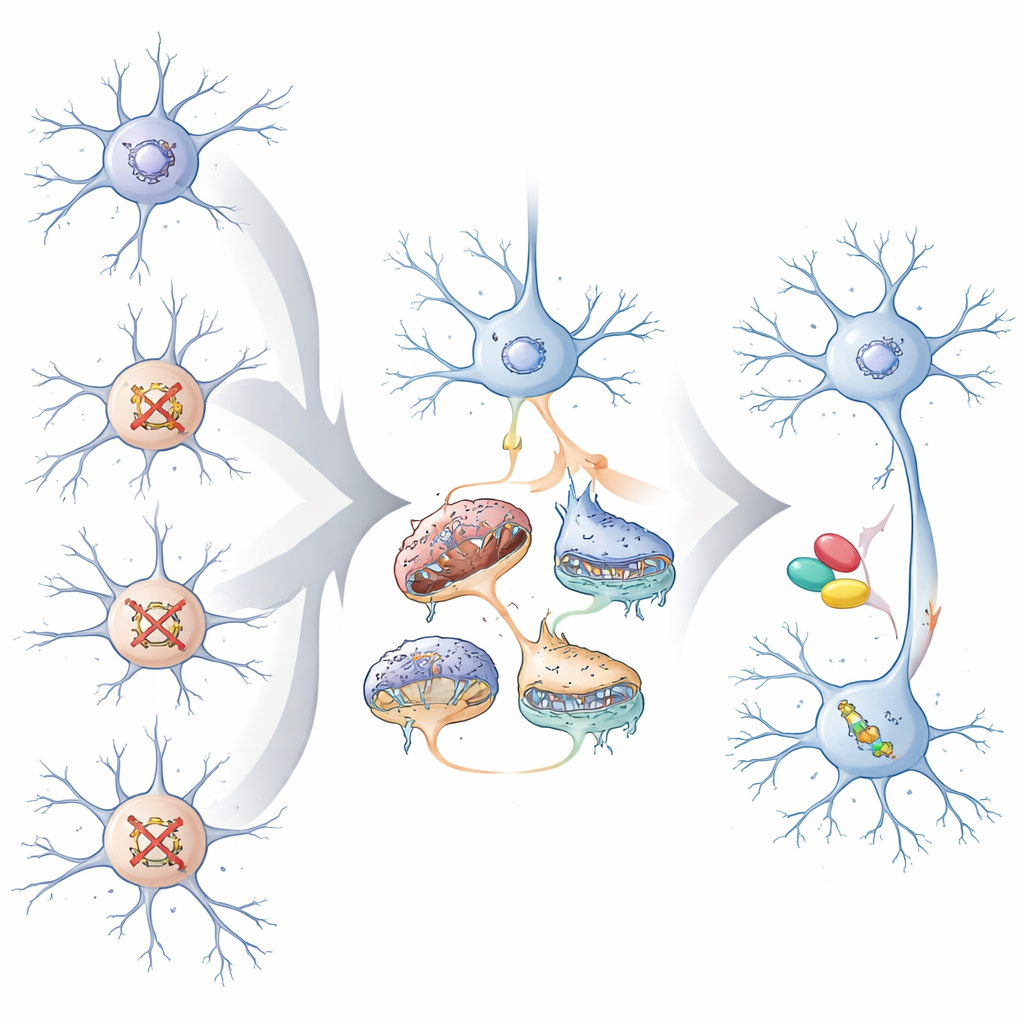
Почему это важно для будущих методов лечения
Ключевой вывод для неспециалиста состоит в том, что очень разные гены, связанные с аутизмом и задержкой развития, могут смещать нейроны в сторону сравнительно небольшого набора общих проблем, особенно в возбуждающих нейронах, которые управляют корковыми цепями. Эти общие проблемы включают работу синапсов, регулирование активности генов и обеспечение энергии митохондриями. Карта таких конвергентных путей даёт надежду, что в будущем лечение можно будет подбирать не только по конкретной мутации пациента, но и по общим клеточным «разломам», которые она вызывает. Эксперименты на зебрафиш показывают, что нацеливание на эти общие пути даже после формирования мозга частично нормализует поведение, что вселяет надежду на то, что конвергентная биология может направлять более точные и широкоприменимые терапевтические подходы.
Цитирование: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Ключевые слова: генетика аутизма, нейроразвитные расстройства, возбуждающие нейроны, митохондриальная функция, поведение цыплянок-данио (zebrafish)