Clear Sky Science · fr
Convergence transcriptomique et phénotypique des gènes de risque des troubles du développement neuronal in vitro et in vivo
Pourquoi des gènes différents peuvent provoquer des difficultés cérébrales similaires
De nombreux enfants diagnostiqués avec l'autisme ou un retard du développement portent des mutations génétiques très différentes, mais présentent souvent des problèmes d'apprentissage, de comportement ou de perception semblables. Cette étude pose une question apparemment simple aux implications importantes : lorsque des dizaines de gènes de risque différents sont altérés, perturbent-ils finalement les mêmes processus fondamentaux dans les cellules cérébrales, et ces points faibles partagés pourraient-ils orienter de futurs traitements ?
Examiner de nombreux gènes en même temps dans des cellules cérébrales
Les chercheurs se sont concentrés sur 23 gènes à fort impact liés aux troubles du développement neuronal, qui contrôlent principalement la façon dont l'ADN est emballé et lu, ainsi que quelques gènes essentiels à la communication entre cellules nerveuses. À partir de cellules souches humaines, ils ont cultivé trois types cellulaires clés du cortex en développement : des cellules progénitrices neurales en division, des neurones excitateurs (glutamatergiques) qui stimulent l'activité cérébrale, et des neurones inhibiteurs (GABAergiques) qui la freinent. Avec une approche CRISPR en pool, ils ont désactivé chaque gène de risque dans des milliers de cellules individuelles, puis mesuré quels autres gènes dans ces cellules s'exprimaient davantage ou étaient réprimés. Cela leur a permis d'observer, à travers de nombreuses mutations différentes, où leurs effets en aval « convergent » sur les mêmes ensembles de gènes ou de voies.
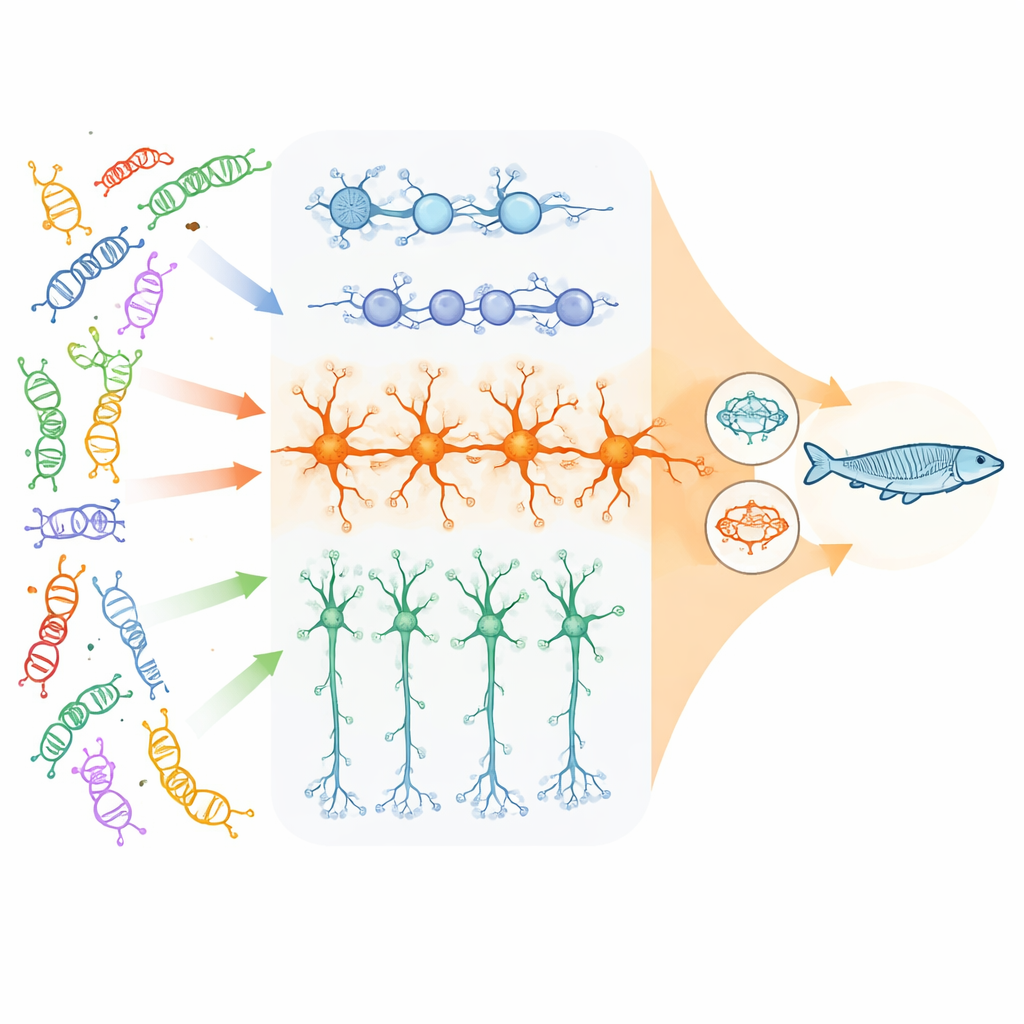
La convergence est la plus marquée chez les neurones excitateurs
L'équipe a constaté que la convergence dépend fortement du type cellulaire et du stade de développement. Si chaque inactivation génique laissait sa propre empreinte, les changements partagés les plus étendus et les mieux connectés apparaissaient dans les neurones excitateurs matures. Là, des milliers de gènes étaient modifiés de manière similaire pour de nombreux gènes de risque différents. Les réseaux affectés se concentraient sur trois thèmes : les synapses (les jonctions où les neurones communiquent), la machinerie cellulaire qui contrôle l'activation ou la répression des gènes, et, de façon inattendue, les mitochondries — les centrales énergétiques de la cellule. En revanche, les progéniteurs neuronaux présentaient surtout des changements partagés liés à la division cellulaire et aux voies de croissance cérébrale précoce, et les neurones inhibiteurs montraient des schémas de convergence plus modestes et distincts.
Des réseaux géniques à la fonction cérébrale et au comportement
Pour vérifier si ces changements convergents ont une importance pour la maladie, les auteurs ont comparé les signatures géniques partagées à de grandes études génétiques des troubles psychiatriques. Les gènes et réseaux convergents dans les neurones excitateurs étaient enrichis en variants de risque associés à l'autisme, à la schizophrénie et à la déficience intellectuelle, ainsi qu'en cibles connues de la protéine Fragile X. Des modèles d'apprentissage automatique entraînés sur ces données ont prédit que, parmi plus de 100 gènes de risque neurodéveloppemental connus, ceux principalement liés à l'autisme ont tendance à converger dans les neurones excitateurs, tandis que ceux davantage associés à un retard développemental global convergent dans les neurones inhibiteurs. L'équipe a aussi montré expérimentalement que plusieurs gènes de risque représentatifs, lorsqu'ils sont perturbés individuellement, provoquaient des problèmes distincts mais liés dans la génération de nouvelles cellules par les neurones et dans la structure et la consommation d'oxygène des mitochondries — concordant avec les schémas convergents observés dans les cribles en pool.
Tester la convergence chez des animaux vivants et avec des médicaments
Parce que les cultures cellulaires ne captent pas les circuits cérébraux complets ni le comportement, les chercheurs se sont tournés vers le poisson zèbre portant des mutations dans un sous-ensemble des mêmes gènes. Le suivi automatisé du sommeil, de l'éveil et des réponses de sursaut a regroupé ces poissons en quatre « ensembles » comportementaux aux profils similaires, comme un sommeil altéré ou une sensibilité accrue aux variations de lumière. En superposant ces groupements comportementaux aux données issues des cellules humaines, les auteurs ont constaté que chaque ensemble s'associait à son propre motif de gènes convergents, là encore le plus marqué chez les neurones excitateurs. Ils ont ensuite utilisé des bases de données de réponses médicamenteuses et des écrans pharmacologiques antérieurs chez le poisson zèbre pour prédire des médicaments susceptibles d'inverser les signatures convergentes et d'atténuer les comportements mutants. Lors des tests complémentaires, 10 des 11 médicaments sélectionnés ont amélioré au moins un comportement anormal chez les mutants de poisson zèbre, et certains ont produit une restauration spectaculaire du sommeil ou des réponses sensorielles.
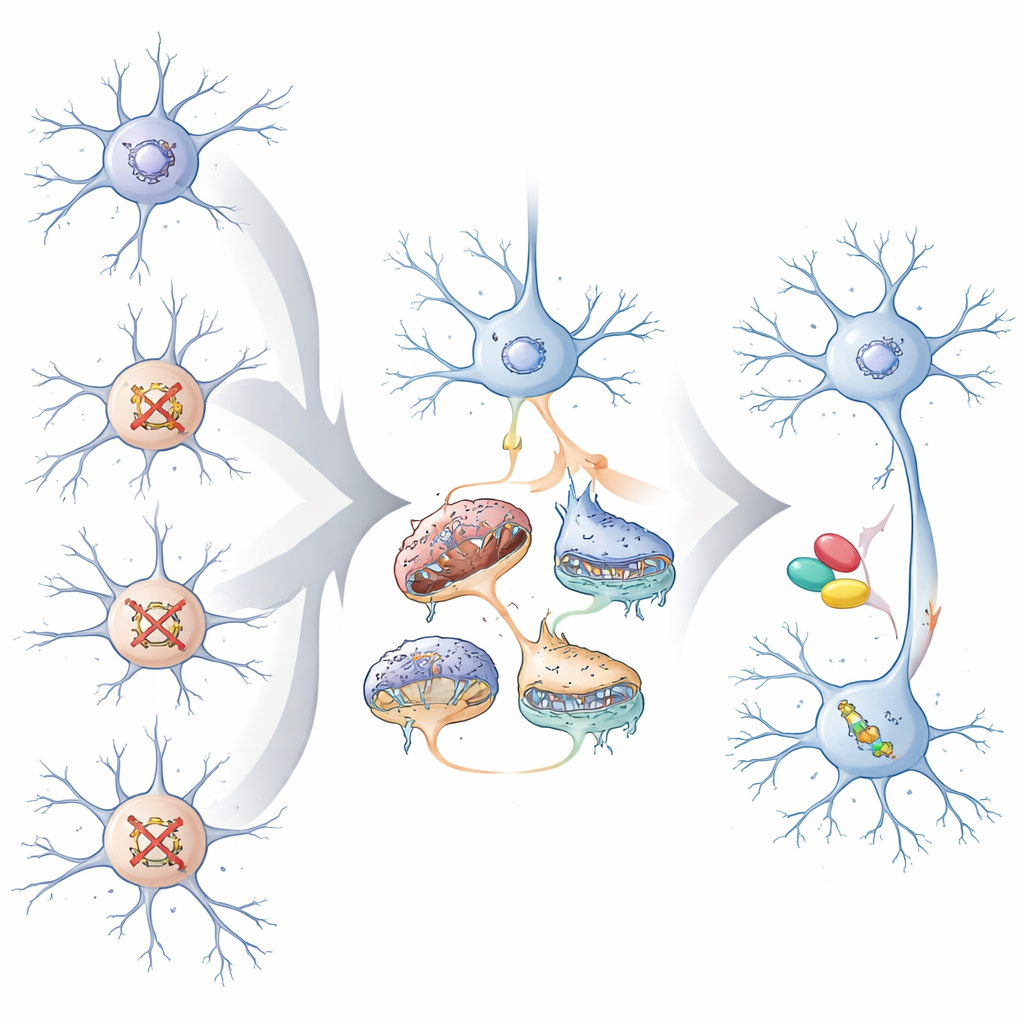
Pourquoi cela compte pour les traitements futurs
Pour un non-spécialiste, le message clé est que des gènes très différents liés à l'autisme et au retard du développement peuvent conduire les cellules cérébrales vers un ensemble plus restreint de problèmes partagés, en particulier dans les neurones excitateurs qui pilotent les circuits corticaux. Ces problèmes communs concernent la fonction synaptique, le contrôle de l'activité génique et l'approvisionnement énergétique par les mitochondries. En cartographiant ces voies convergentes, l'étude suggère que les traitements pourraient un jour être adaptés non seulement à la mutation spécifique d'une personne, mais aussi aux « failles » cellulaires partagées activées par cette mutation. Les expériences chez le poisson zèbre indiquent que cibler ces voies partagées, même après le développement du cerveau, peut en partie normaliser le comportement, ce qui laisse entrevoir que la biologie convergente pourrait orienter des thérapies plus précises et aux applications larges.
Citation: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Mots-clés: génétique de l'autisme, troubles du développement neurologique, neurones excitateurs, fonction mitochondriale, comportement du poisson zèbre