Clear Sky Science · pl
Transkryptomiczna i fenotypowa konwergencja genów ryzyka zaburzeń neuro‑rozwojowych in vitro i in vivo
Dlaczego różne geny mogą powodować podobne problemy mózgowe
Wiele dzieci z rozpoznaniem autyzmu lub opóźnienia rozwojowego ma bardzo różne mutacje genetyczne, a mimo to często wykazuje podobne trudności w uczeniu się, zachowaniu czy przetwarzaniu sensorycznym. To badanie stawia pozornie proste pytanie o dalekosiężnych implikacjach: gdy dziesiątki różnych genów ryzyka są zmienione, czy zakłócają one te same podstawowe procesy w komórkach mózgu, a jeśli tak — czy te wspólne słabe punkty można wykorzystać do opracowania przyszłych terapii?
Analiza wielu genów jednocześnie w komórkach mózgowych
Naukowcy skupili się na 23 genach o dużym wpływie powiązanych z zaburzeniami neurorozwojowymi, które przede wszystkim kontrolują, jak DNA jest pakowane i odczytywane, oraz na kilku genach niezbędnych do komunikacji między komórkami nerwowymi. Przy użyciu ludzkich komórek macierzystych wyhodowali trzy kluczowe typy komórek występujące w rozwijającej się korze: dzielące się progenitory nerwowe, neurony pobudzające (glutamatergiczne), które stymulują aktywność mózgu, oraz neurony hamujące (GABAergiczne), które ją tłumią. Przy zastosowaniu skumulowanego podejścia CRISPR wyłączyli każdy gen ryzyka w tysiącach pojedynczych komórek, a następnie zmierzyli, które inne geny w tych komórkach uległy zwiększeniu lub zmniejszeniu ekspresji. Pozwoliło to zobaczyć, wśród wielu różnych mutacji, gdzie ich efekt „zbiegał się” na tych samych zestawach genów lub szlakach.
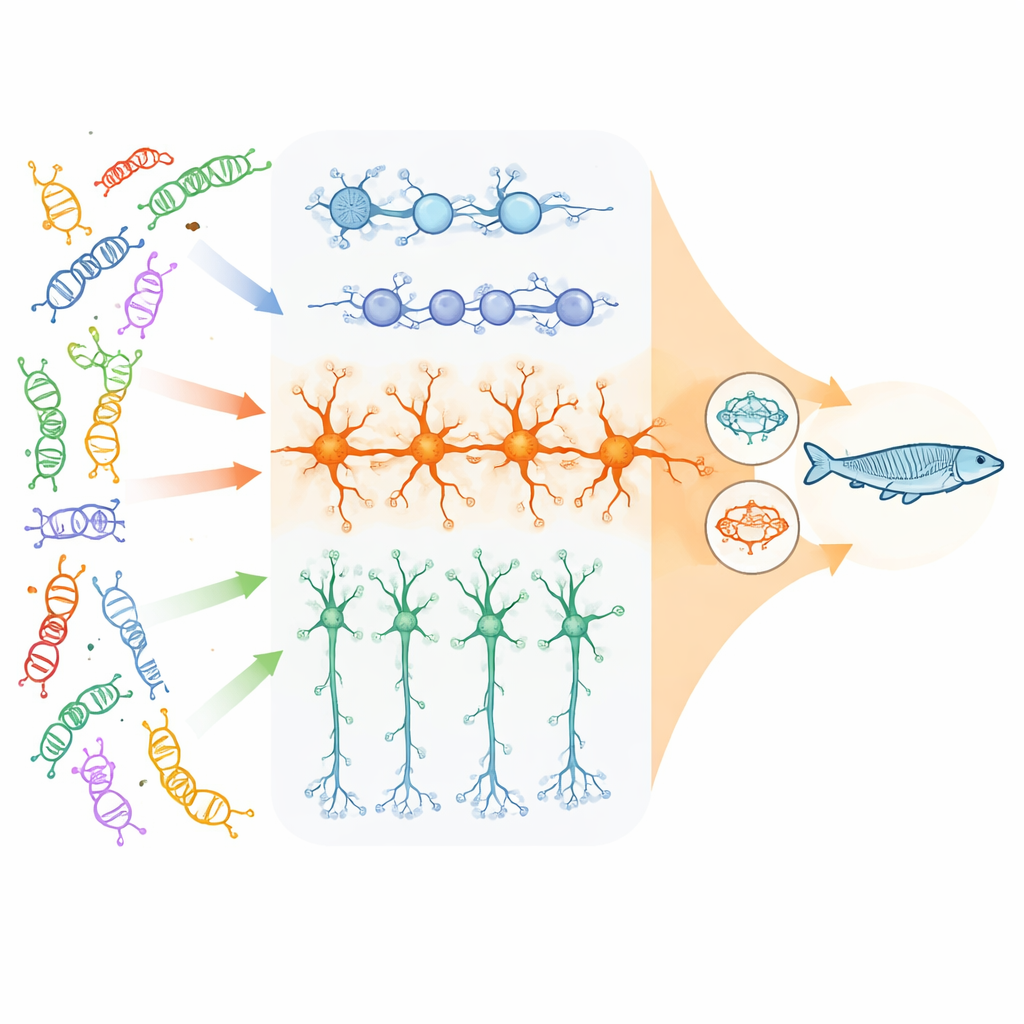
Konwergencja najsilniejsza w neuronach pobudzających
Zespół odkrył, że konwergencja silnie zależy od typu komórki i fazy rozwojowej. Chociaż każdy knockout genu pozostawiał własny odcisk, najbardziej obszerne i ściśle połączone wspólne zmiany pojawiły się w dojrzałych neuronach pobudzających. W tym przypadku tysiące genów były zmienione w podobny sposób w wielu różnych genach ryzyka. Dotknięte sieci skupiały się wokół trzech obszarów: synaps (miejsc, gdzie neurony się komunikują), maszynerii komórkowej kontrolującej, które geny są włączane lub wyłączane, oraz, co zaskakujące, mitochondriów — fabryk energii komórkowej. Dla porównania, progenitory nerwowe wykazywały głównie wspólne zmiany w szlakach związanych z podziałem komórkowym i wczesnym rozwojem mózgu, a neurony hamujące ujawniały skromniejsze i odmienne wzorce konwergencji.
Od sieci genowych do funkcji mózgu i zachowania
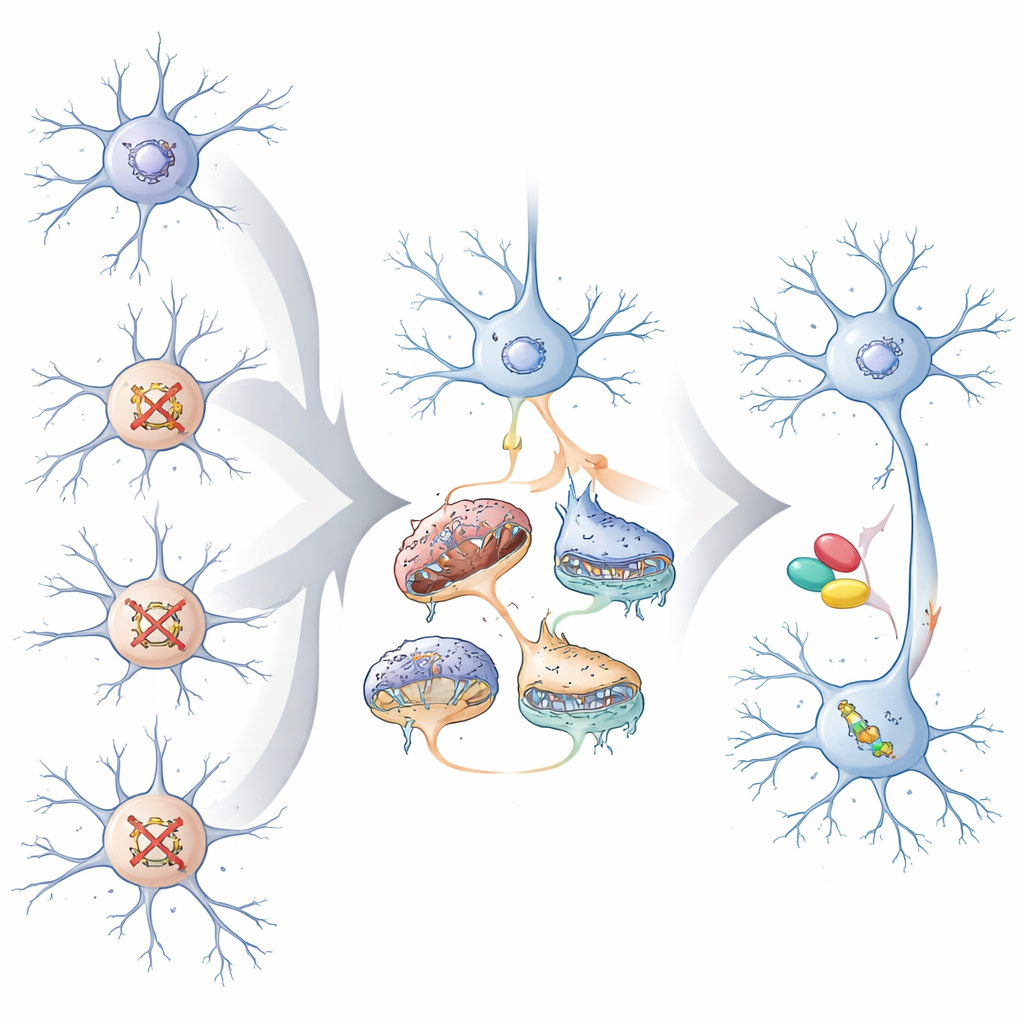
Aby sprawdzić, czy te zbieżne zmiany mają znaczenie dla choroby, autorzy porównali wspólne sygnatury genowe z dużymi badaniami genetycznymi schorzeń psychiatrycznych. Geny i sieci konwergentne w neuronach pobudzających były wzbogacone o warianty ryzyka powiązane z autyzmem, schizofrenią i niepełnosprawnością intelektualną, a także o znane cele białka Fragile X. Modele uczone maszynowo na tych danych przewidziały, że spośród ponad 100 znanych genów ryzyka neurorozwojowego te powiązane głównie z autyzmem mają tendencję do konwergencji w neuronach pobudzających, podczas gdy geny bardziej związane z ogólnym opóźnieniem rozwoju konwergują w neuronach hamujących. Zespół wykazał również eksperymentalnie, że kilka reprezentatywnych genów ryzyka, gdy są zaburzone pojedynczo, powodowało odrębne, lecz powiązane problemy w tym, jak neurony generują nowe komórki oraz w strukturze i zużyciu tlenu przez ich mitochondria — co odpowiada wzorcom konwergencji zaobserwowanym w badaniach skumulowanych.
Testowanie konwergencji w żywych zwierzętach i przy użyciu leków
Ponieważ hodowle komórkowe nie odzwierciedlają całych obwodów mózgowych ani zachowania, badacze zwrócili się do danio pręgowanego (zebrafish) noszącego mutacje w podzbiorze tych samych genów. Zautomatyzowane śledzenie snu, pobudzenia i reakcji na zaskoczenie pogrupowało te ryby w cztery „zbiory” behawioralne o podobnych wzorcach, takie jak zmieniony sen czy zwiększona wrażliwość na zmiany światła. Po nałożeniu tych grup behawioralnych na dane z ludzkich komórek autorzy odkryli, że każdy zestaw wiąże się z własnym wzorcem zbieżnych genów, ponownie najsilniej w neuronach pobudzających. Następnie skorzystali z baz danych reakcji na leki i wcześniejszych ekranów leków w zebrafish, aby przewidzieć substancje, które mogłyby odwrócić zbieżne sygnatury i przeciwdziałać zmienionym zachowaniom mutantów. W testach follow‑up 10 z 11 wybranych leków poprawiło przynajmniej jedno nieprawidłowe zachowanie u mutantów zebrafish, a niektóre dały uderzające przywrócenie snu lub reakcji sensorycznych.
Dlaczego to ma znaczenie dla przyszłych terapii
Dla laika główny przekaz jest taki, że bardzo różne geny związane z autyzmem i opóźnieniem rozwoju mogą popychać komórki mózgowe w kierunku ograniczonego zestawu wspólnych problemów, szczególnie w neuronach pobudzających, które napędzają obwody kory. Te wspólne problemy obejmują funkcjonowanie synaps, kontrolę aktywności genów oraz dostarczanie energii przez mitochondria. Mapując te zbieżne szlaki, badanie sugeruje, że leczenie w przyszłości mogłoby być dobrane nie tylko do konkretnej mutacji danej osoby, lecz także do wspólnych „uskoków” komórkowych, które ta mutacja uruchamia. Eksperymenty w zebrafish sugerują, że ukierunkowanie tych wspólnych szlaków, nawet po ukształtowaniu mózgu, może częściowo znormalizować zachowanie — co daje nadzieję, że konwergentna biologia może poprowadzić do bardziej precyzyjnych i szeroko użytecznych terapii.
Cytowanie: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
Słowa kluczowe: genetyka autyzmu, zaburzenia neurorozwojowe, neurony pobudzające, funkcja mitochondriów, zachowanie danio pręgowanego