Clear Sky Science · he
התכנסות טרנסקריפטומית ופנוטיפית של גנים מסכני הפרעות בהתפתחות העצבית במבחנה ובחי
מדוע גנים שונים עלולים לגרום לאותן בעיות מוחיות
ילדים רבים המאובחנים עם אוטיזם או עיכוב התפתחותי נושאים מוטציות גנטיות שונות מאוד, אך לעתים קרובות חווים בעיות דומות בלמידה, בהתנהגות או בתחושות. המחקר שואל שאלה שנראית פשוטה אך בעלת משמעויות רחבות: כאשר עשרות גני סיכון משתנים, האם הם מפריעים בסופו של דבר לאותן תהליכים בסיסיים בתאי המוח, והאם נקודות תורפה משותפות אלה יכולות להנחות טיפולים עתידיים?
מסתכלים על הרבה גנים בתאי מוח בבת אחת
החוקרים התמקדו ב-23 גנים בעלי השפעה גבוהה הקושרים להפרעות בהתפתחות העצבית, שרובם מעורבים בשליטה על אריזת ה-DNA וקריאתו, וכן בכמה גנים חיוניים לתקשורת בין תאי עצב. בעזרת תאי גזע אנושיים גידלו שלושה סוגי תאים מרכזיים שנמצאים בקורטקס המתפתח: תאי פרוגניטורים נוירליים מתחלקים, נוירונים מעוררים (גלוטאמטרגיים) שמגבירים פעילות מוחית, ונוירונים מעכבים (GABAergic) שמרגיעים אותה. בגישה בריכתית של CRISPR כיבו כל גן סיכון באלפי תאים בודדים, ואז מדדו אילו גנים אחרים בתאים האלה הועלו או הורדו. זה איפשר להם לראות, לאורך מוטציות רבות ושונות, היכן ההשפעות ההורדניות "התכנסו" לאותן קבוצות גנים או מסלולים.
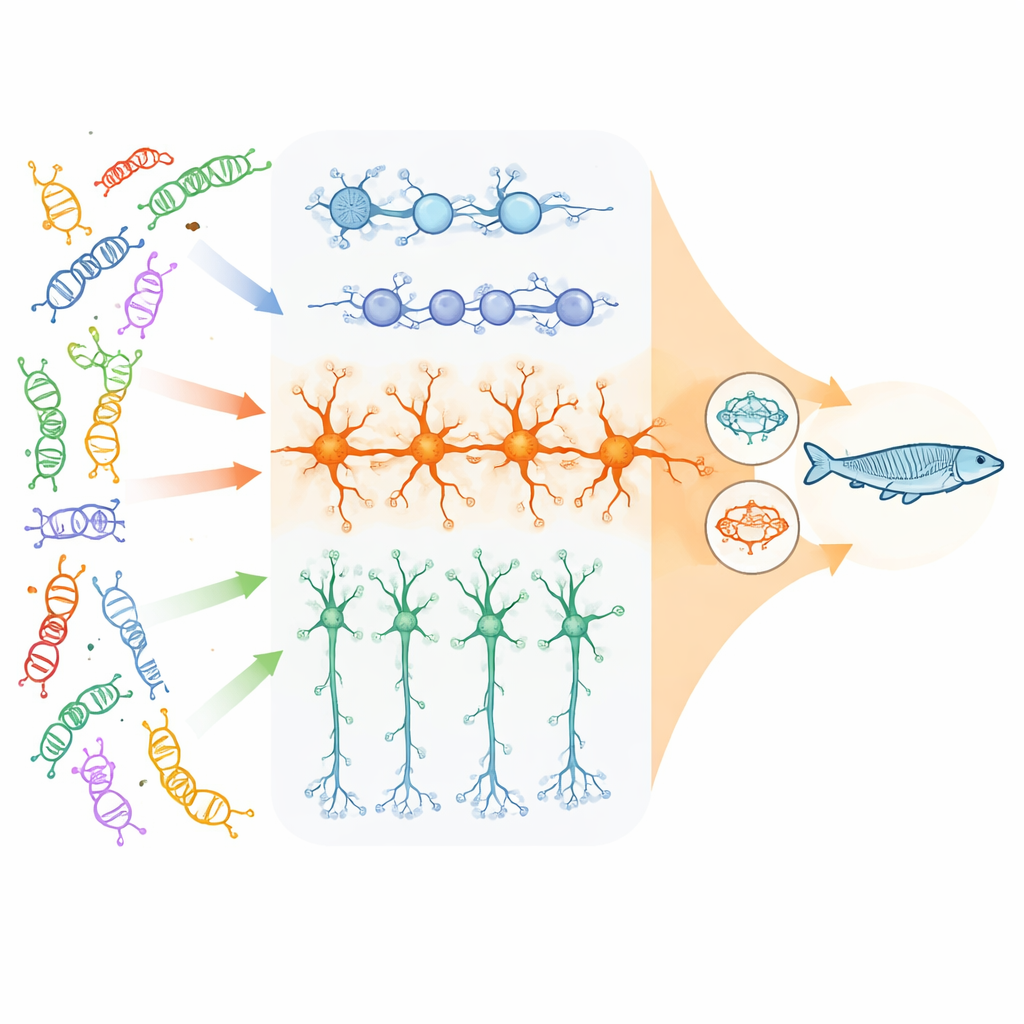
ההתכנסות חזקה ביותר בנוירונים מעוררים
הצוות מצא כי ההתכנסות תלוית סוג תא ושלב התפתחותי. כל ניתוק גן השאיר טביעת אצבע ייחודית, אך השינויים המשותפים הנרחבים והקושרים ביותר הופיעו בנוירונים המעוררים בשלים. כאן אלפי גנים שונו באופן דומה על-ידי גנים מסכנים רבים ושונים. הרשתות המושפעות התרכזו בשלושה נושאים: סינפסות (המפגשים שבהם נוירונים מתקשרים), המכאניזם התאי ששולט אילו גנים פעילים וכבויים, ובמפתיע — מיטוכונדריות, 'מפעלי האנרגיה' של התא. לעומת זאת, פרוגניטורים נוירליים הראו בעיקר שינויים משותפים בחלוקה תאית ובמסלולי צמיחת מוח מוקדמים, והנוירונים המעכבים הציגו דפוסי התכנסות צנועים ומובחנים יותר.
מרשתות גנים לתפקוד מוחי ולהתנהגות
כדי לבדוק האם השינויים המתכנסים אלה רלוונטיים למחלה, המחברים השוו את החתימות הגנטיות המשותפות למחקרים גנטיים נרחבים של מצבים פסיכיאטריים. הגנים והרשתות המתכנסות בנוירונים המעוררים היו מועשרים בווריאנטים סיכון הקשורים לאוטיזם, סכיזופרניה ובינה לקויה, וכן ביעדים ידועים של חלבון Fragile X. מודלים של למידת מכונה שאומנו על הנתונים האלה חזו שעבור מעל ל-100 גני סיכון ידועים, אלה הקשורים בעיקר לאוטיזם נוטים להתכנס בנוירונים מעוררים, בעוד אלה הקשורים לעיכוב התפתחותי גלובלי מתכנסים יותר בנוירונים מעכבים. הצוות גם הראה בניסויים שכמה גני סיכון מייצגים, כשהם מופרעים באופן פרטני, יצרו בעיות מובחנות אך קשורות באופן שבו נוירונים יוצרים תאים חדשים ובאופן שבו מיטוכונדריותיהם בנויות וצורכות חמצן — התאמה לדפוסי ההתכנסות שנראו במסכים הברקתיים.
בדיקת ההתכנסות בחיות חיות ובתרופות
מכיוון שתרביות תאים אינן יכולות ללכוד מעגלי מוח שלמים או התנהגות, החוקרים פנו לדגי זברה הנושאים מוטציות בתת־קבוצה מאותם גנים. מעקב אוטומטי אחר שינה, עוררות ותשובת הלם קיבץ את הדגים לארבע "קבוצות" התנהגותיות עם דפוסים דומים, כגון שינה משונת או רגישות מוגברת לשינויים באור. כאשר המחברים חיפו את הקיבוצים ההתנהגותיים האלה עם נתוני תאים אנושיים, הם מצאו שכל קבוצה הייתה מקושרת לדפוס משלה של גנים מתכנסים, שוב בעוצמה הגבוהה ביותר בנוירונים המעוררים. לאחר מכן השתמשו במסדי נתוני תגובת תרופות ובמסכי תרופות מוקדמים על זבובים/זברה כדי לחזות תרופות שעשויות להפוך את החתימות המתכנסות ולנגד את ההתנהגויות המוטנטיות. בבדיקות המשך, 10 מתוך 11 תרופות שנבחרו שיפרו לפחות התנהגות אחת חריגה בדגי הזברה המוטנטים, ובחלק מהמקרים נרשמה החלמה מרשימה של שינה או תגובות חישתיות.
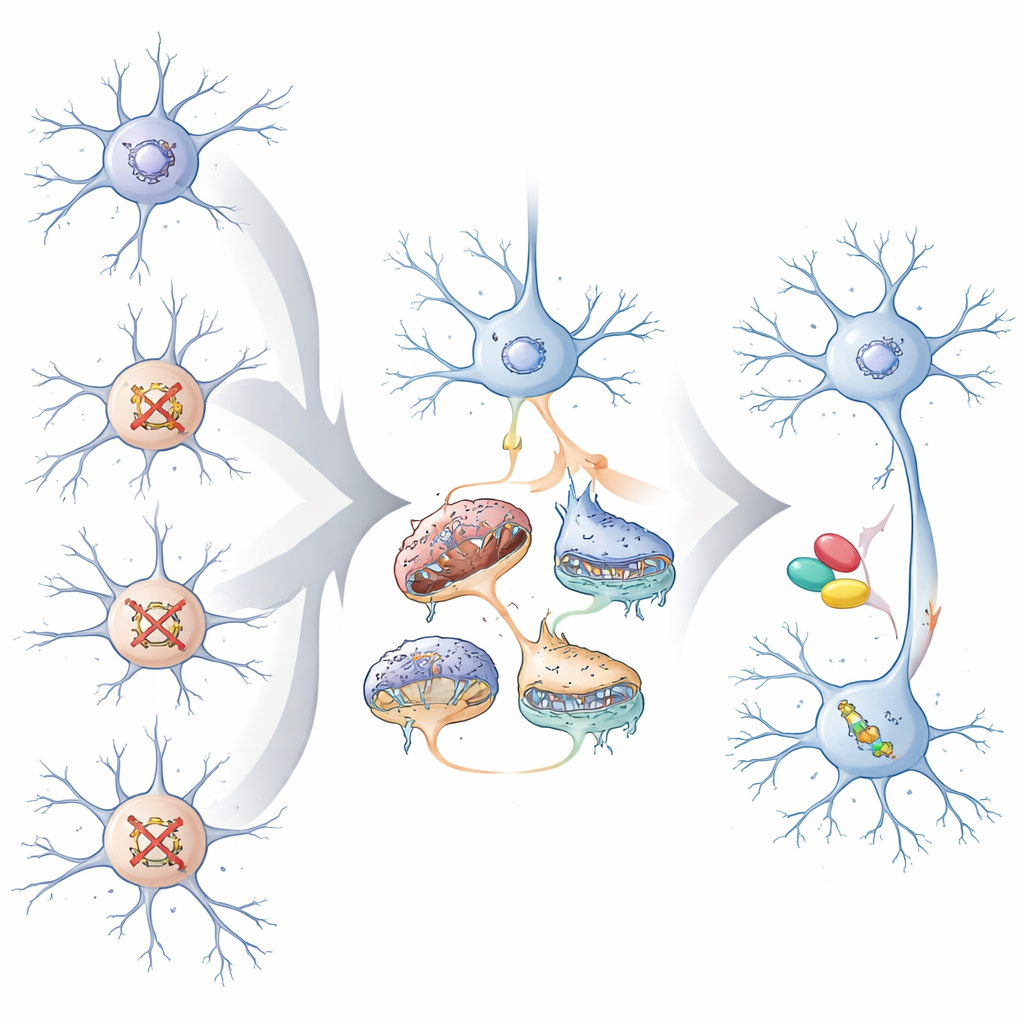
מדוע זה חשוב לטיפולים עתידיים
להדיוט, המסר המרכזי הוא שגנים שונים מאוד הקשורים לאוטיזם ולעיכוב התפתחותי יכולים לדחוף תאי מוח לקבוצת בעיות משותפת מצומצמת יותר, במיוחד בנוירונים המעוררים שמניעים מעגלי קורטקס. בעיות משותפות אלה כוללות את תפקוד הסינפסות, בקרה על פעילות גנים וכיצד המיטוכונדריות מספקות אנרגיה. באמצעות מיפוי מסלולי ההתכנסות הללו, המחקר מרמז שיום אחד טיפולים עשויים להיות מותאמים לא רק למוטציה ספציפית של אדם, אלא לקווי השבר התאית המשותפים שהמוטציה מפעילה. ניסויי דגי הזברה מרמזים כי מיקוד במסלולים המשותפים האלה, אפילו אחרי שבמוח כבר התפתח, יכול לנרמל במידה מסוימת התנהגות, מה שמעלה תקווה שהתכנסות ביולוגית תוכל להנחות טיפולים מדויקים ועם היקף שימוש רחב יותר.
ציטוט: Fernandez Garcia, M., Retallick-Townsley, K., Pruitt, A. et al. Transcriptomic and phenotypic convergence of neurodevelopmental disorder risk genes in vitro and in vivo. Nat Neurosci 29, 1079–1094 (2026). https://doi.org/10.1038/s41593-026-02247-7
מילות מפתח: גנטיקה של אוטיזם, הפרעות בהתפתחות העצבית, נוירונים מעוררים, תפקוד מיטוכונדריאלי, התנהגות של דגי זברה