Clear Sky Science · tr
KDM3A, histon H3K9 üzerindeki asetil-lizin grubunu hidroksiasetil-lizine oksitlemektedir
Hücreler Küçük Kimyasal Anahtarlarla Genleri Nasıl Ayarlar
Vücudunuzdaki her hücre aynı DNA’yı taşır, ama kalp hücreleri, beyin hücreleri ve deri hücreleri çok farklı davranır. Bunun bir nedeni, hücrelerin DNA’yı paketleyen proteinler olan histonları, genleri açıp kapatan anahtarlar gibi davranan küçük kimyasal etiketlerle süslemeleridir. Bu makale, önemli bir histon bölgesinde şaşırtıcı yeni bir anahtarı ortaya koyuyor ve bunun doğrudan oksijen tarafından kontrol edildiğini göstererek hücrelerin gen okumalarını soludukları havayı hissetmelerine bağlayan bir ilişki kuruyor.
İyi Bilinen Bir Histon İşaretine Yeni Bir Bükülme
Histonlar, DNA’nın sarıldığı makara benzeri yapılardır. Hücreler, DNA’yı gevşetip sıkılaştırmak ve hangi genlerin etkin olduğunu etkilemek için histonların belirli noktalarına asetil veya metil gibi kimyasal gruplar ekler. Ünlü bir sıcak nokta, histon H3’ün 9. pozisyonundaki lizin (H3K9) olup, burada asetilasyon gen aktivitesini teşvik etme eğilimindeyken bazı metil işaretleri gen susturulmasıyla ilişkilidir. Histon asetiltransferazlar asetil gruplarını ekler, deasetilazlar ise bunları çıkarır; diğer enzimler ise metilleri ekleyip siler. Bugüne dek bu değişikliklerin “redoks-özgür” olduğu—yani açıkça oksijene bağımlı olmadığı—düşünülüyordu. 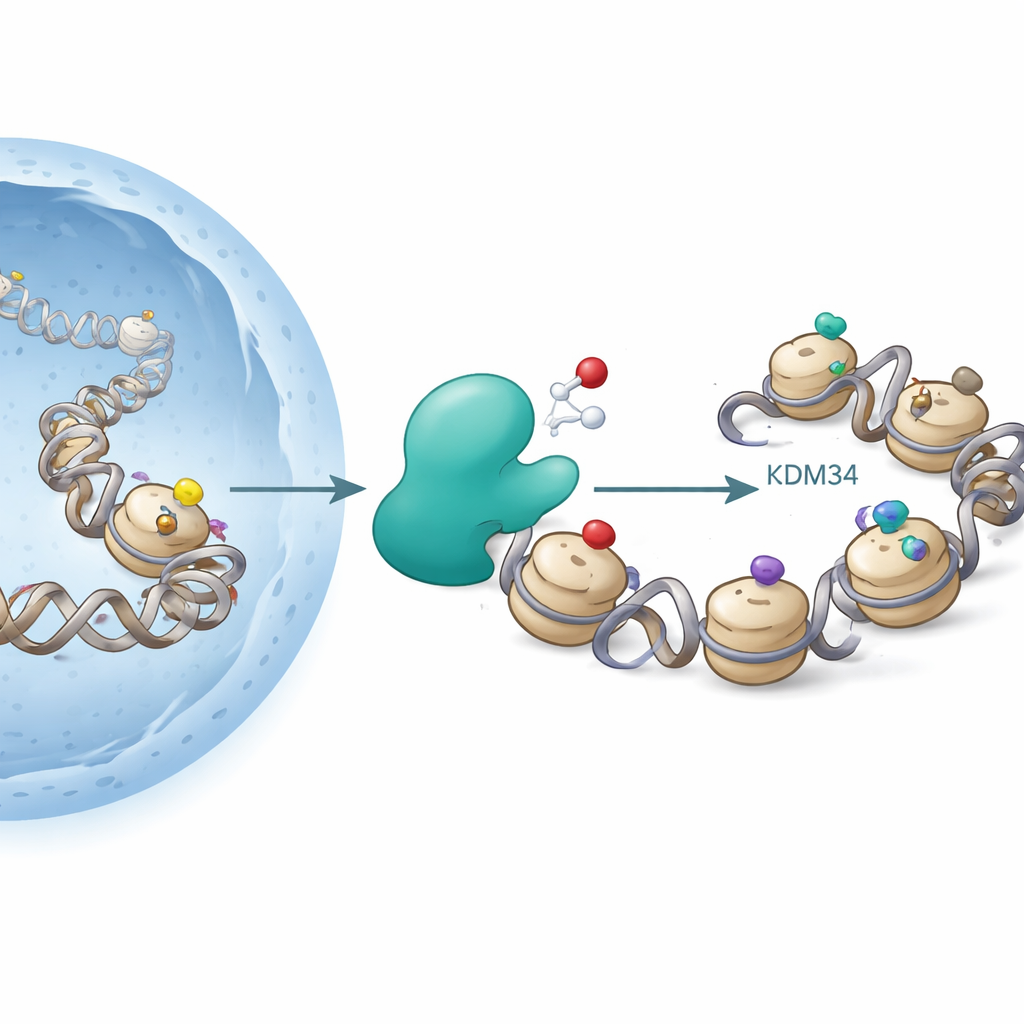
Oksijenle Bağlantılı Bir Histon İşaretinin Keşfi
Yazarlar, H3K9’daki metil grupları kaldırmasıyla zaten bilinen bir enzim olan KDM3A’ya odaklandı. KDM3A, demir ve 2-oksoglutarat adlı küçük bir kofaktörü gerektiren, oksijene bağımlı enzim ailesine aittir; bu aile, dokularımızdaki düşük oksijeni (hipoksi) algılayan enzimlere benzer. Araştırmacılar, KDM3A hedefi olabilecek çeşitli modifiye histon parçalarını taradıklarında, KDM3A’nın H3K9 üzerindeki belirli metil işaretlerini etkili şekilde sildiğini doğruladılar. Beklenmedik şekilde, saflaştırılmış KDM3A’nın H3K9’daki asetil grubunu oksitleyebildiğini, bunu hidroksiasetil-lizine dönüştürdüğünü de buldular. Bu değişim, asetil grubuna bir oksijen atomu eklenmesine karşılık gelir ve daha ileri deneyler enzimin bazı koşullar altında daha ileri oksitasyonlar da gerçekleştirebileceğini göstererek daha egzotik kimyasal dönüşümlere işaret etti.
Yeni İşaretin Hücrelerde Var Olduğunu Kanıtlama
Bir test tüpünde yeni bir kimyasal ürün bulmak sadece ilk adımdır; ekip ayrıca hidroksiasetil-lizinin canlı hücrelerde histonlarda göründüğünü de göstermek zorundaydı. Bunun için standart asetil formunu değil, hidroksiasetil grubunu tanıyan özel bir antikor geliştirdiler. Bu araçla, izole histonlara saflaştırılmış KDM3A eklemenin yeni işaretin sinyalini artırdığını, aynı zamanda KDM3A’nın çift etkinliğine uygun olarak H3K9’daki tanımlı metil işaretlerinin azaldığını gösterdiler. İnsan hücrelerinde KDM3A’yı aşırı ifade etmek benzer etkilere yol açtı: metil işaretleri düştü ve toplu histonlarda ve tek hücre düzeyinde hidroksiasetil sinyali yükseldi. Molekülleri tartmada çok hassas bir teknik olan kütle spektrometrisi, KDM3A etkin olduğunda hidroksiasetil-lizin taşıyan spesifik H3K9 peptidinin hücrelerde var olduğunu bağımsız olarak doğruladı.
Yeni İşaretin Genom Üzerindeki Konumu
Bu işaretin DNA boyunca nerede ortaya çıktığını görmek için araştırmacılar ChIP-seq, yani genom çapında haritalama yöntemi uyguladılar. H3K9 hidroksiasetilasyonunun, özellikle zaten yüksek düzeyde ifade edilen genlerin başlangıç bölgeleri çevresinde kümelendiğini buldular. Deseni, klasik “aktif” işaretler olan H3K9 asetilasyonu ve H3K4 trimetilasyonunun izini yakından takip ediyor; bu da yeni etiketin aktif kromatin araç setine ait olduğunu düşündürüyor. Hücreleri histon deasetilaz inhibitörü ile muamele etmek—kanser tedavisinde zaten kullanılan bir ilaç türü—hem standart asetilasyonu hem de yeni hidroksiasetil işaretini artırdı; muhtemelen bu, KDM3A için substrat bulunabilirliğini artırıp bu asil grupların uzaklaştırılmasını yavaşlattığı içindir. 
Diğer Proteinler Yeni İşareti Nasıl Okuyor ve İşliyor
Çalışma ayrıca mevcut kromatin “okuyucu” ve “silici” proteinlerin bu yeni işarete nasıl yanıt verdiğini test etti. Normalde asetil ve krotonil işaretlerini tanıyan AF9 proteininden bir okuyucu domaini, hidroksiasetil versiyonuna yalnızca hafifçe azalmış bir afiniteyle bağlandı; bu, bilinen okuyucuların bu modifikasyonu algılayabildiğini ima ediyor. İki deasetilaz enzim olan SIRT1 ve HDAC8, hidroksiasetil-lizini farklı şekilde işledi: SIRT1 yeni işareti standart asetil grubuna kıyasla çok daha az verimli şekilde uzaklaştırırken, HDAC8’in belirgin bir tercih göstermediği görüldü. Bu farklılıklar, hidroksiasetilasyonun bir işaretin ne kadar süre kaldığını ve hangi enzimlerin onunla etkileştiğini ince ayar yaparak kromatin manzarasını ince bir şekilde değiştirebileceğini gösteriyor.
Bu Oksijene Bağımlı Anahtar Neden Önemli
Genel olarak, çalışma KDM3A tarafından üretilen ve muhtemelen bazı durumlarda yakın akrabası KDM3B tarafından da oluşturulan daha önce tanınmamış bir histon işareti olarak H3K9 hidroksiasetilasyonunu ortaya koyuyor. KDM3A’nın kendisi hipoksi-indüklenebilir faktör yolu aracılığıyla düşük oksijen tarafından aktive edildiğinden, bu durum oksijen seviyeleri ile histon asetilasyon durumları arasında doğrudan kimyasal bir bağ oluşturuyor. Basitçe söylemek gerekirse, enzim hem baskılayıcı metil etiketleri çıkarabilir hem de aynı histon bölgesindeki etkinleştirici asetil etiketleri hafifçe farklı, oksijen içeren bir forma dönüştürebilir; bu da stres, gelişim veya kanser sırasında gen programlarını yeniden şekillendirebilir. Bu keşif, “demetilaz” enzimlerinin neler yapabileceği hakkındaki görüşümüzü genişletiyor ve diğer proteinlerde benzer hidroksiasetil işaretlerini ve bunların sağlık ile hastalık durumlarındaki rollerini keşfetmeye kapı aralıyor.
Atıf: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Anahtar kelimeler: histon modifikasyonu, epigenetik, oksijen algılama, KDM3A enzimi, gen regülasyonu