Clear Sky Science · ru
KDM3A катализирует окисление ацетил-лизина до гидроксиацетил-лизина на гистоне H3K9
Как клетки настраивают гены с помощью крошечных химических переключателей
Каждая клетка вашего тела несет одну и ту же ДНК, но клетки сердца, мозга и кожи ведут себя по‑разному. Одна из причин — то, что клетки отмечают белки, упаковивающие ДНК (гистоны), небольшими химическими метками, которые работают как переключатели включения или выключения генов. В этой работе описан неожиданный новый тип такого переключателя на важном сайте гистона и показано, что он напрямую регулируется кислородом, связывая то, как клетки читают свои гены, с тем, как они ощущают воздух, которым дышат.
Новый поворот в известной метке гистона
Гистоны — это шпульки, вокруг которых наматывается ДНК. Клетки присоединяют к гистонам химические группы, такие как ацетил или метил, в определенных позициях, чтобы ослабить или уплотнить ДНК и тем самым влиять на активность генов. Известный «горячий» участок — лизин 9 на гистоне H3 (H3K9): ацетилирование здесь обычно способствует активности генов, тогда как некоторые метки метилирования связаны с подавлением. Ферменты, называемые гистонными ацетилтрансферазами, добавляют ацетилы, а деацетилазы удаляют их; другие ферменты добавляют или стирают метильные метки. До недавнего времени считалось, что эти превращения «редокс‑нейтральны» — они явно не зависят от кислорода. 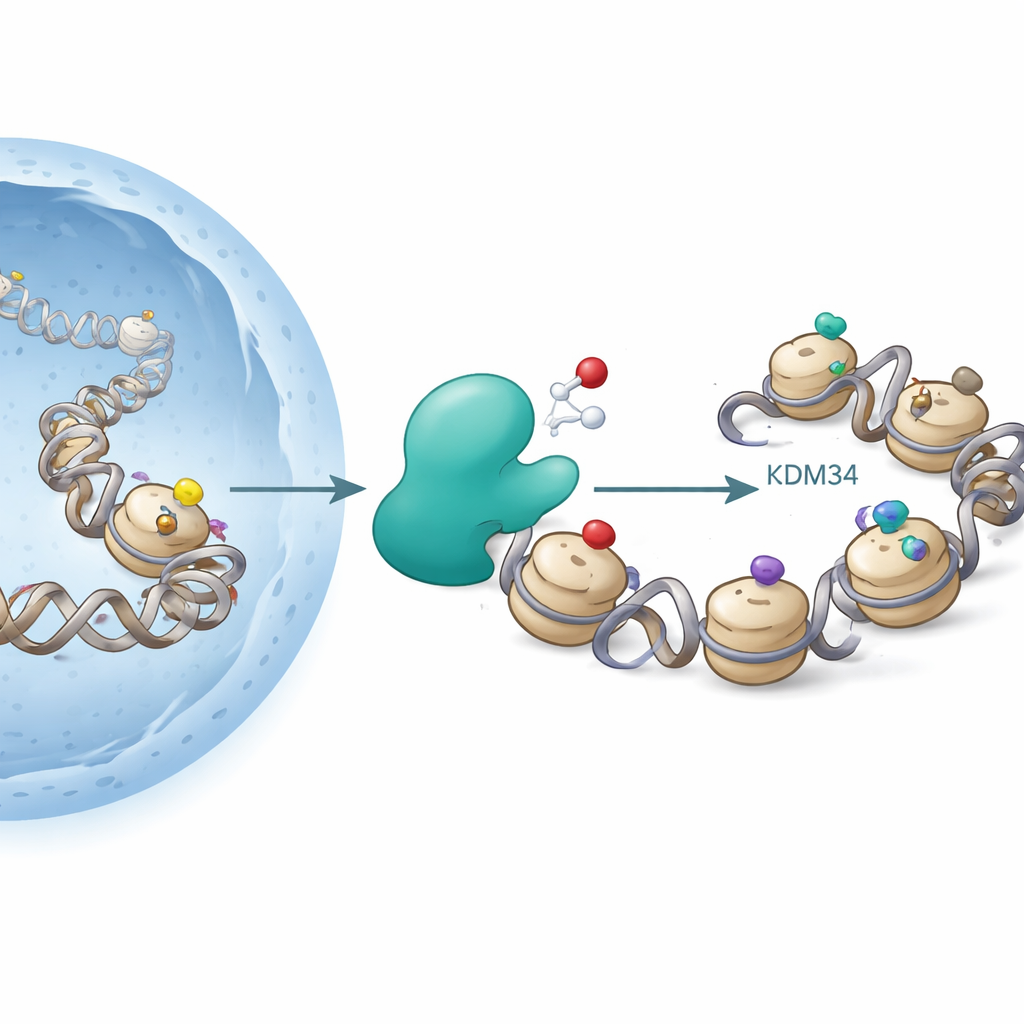
Открытие метки, связанной с кислородом
Авторы сосредоточились на KDM3A — ферменте, уже известном как деметилаза H3K9. KDM3A принадлежит к семейству кислородзависимых ферментов, которым для работы требуются железо и малый кофактор (2‑оксоглутарат), подобно ферментам, чувствующим гипоксию в тканях. При скрининге различных модифицированных фрагментов гистонов как потенциальных мишеней KDM3A они подтвердили, что KDM3A эффективно удаляет определенные метильные метки на H3K9. Неожиданно они также обнаружили, что очищенный KDM3A способен окислять ацетильную группу на H3K9, превращая её в новую форму — гидроксиацетил‑лизин. Это изменение соответствует добавлению атома кислорода в ацетильную группу, и дальнейшие эксперименты показали, что при некоторых условиях фермент может окислять ещё дальше, наводя на мысль о пути к более экзотическим химическим преобразованиям.
Доказательство существования новой метки в клетках
Найти новый химический продукт в пробирке — только первый шаг; группе также нужно было показать, что гидроксиацетил‑лизин встречается на гистонах живых клеток. Они получили специфичную антитело, распознающее H3K9 с гидроксиацетильной группой, но не стандартный ацетил. С помощью этого инструмента показали, что добавление очищенного KDM3A к изолированным гистонам повышает сигнал новой метки, в то время как ожидаемо снижаются известные метильные метки на H3K9, отражая двойную активность KDM3A. Переэкспрессия KDM3A в человеческих клетках дала похожие эффекты: метильные метки уменьшились, а сигнал гидроксиацетиля увеличился как на массивных гистонах, так и на уровне отдельных клеток. Масс‑спектрометрия, чувствительный метод для взвешивания молекул, независимо подтвердила наличие точного пептида H3K9 с гидроксиацетил‑лизином в клетках при активности KDM3A.
Где на геноме располагается новая метка
Чтобы выяснить, где эта метка появляется вдоль ДНК, исследователи провели ChIP‑seq — метод картирования по всему геному. Они обнаружили, что гидроксиацетилирование H3K9 концентрируется вокруг сайтов начала транскрипции, особенно у генов с высокой экспрессией. Его профиль тесно совпадает с классическими «активными» метками, такими как ацетилирование H3K9 и три‑метилирование H3K4, что позволяет предположить, что новая метка также относится к набору признаков активной хроматиновой области. Обработка клеток ингибитором гистонных деацетилаз, классом лекарств, уже применяемых в онкологии, усиливала и стандартное ацетилирование, и новую гидроксиацетильную метку, вероятно, за счёт увеличения доступности субстрата для KDM3A и замедления удаления этих ацилированных групп. 
Как другие белки «читают» и перерабатывают новую метку
В работе также протестировали, как существующие белки‑«ридеры» и «стирающие» ферменты реагируют на новую метку. Ридерный домен белка AF9, который обычно распознаёт ацетильные и кротонильные метки, связывался с гидроксиацетил‑версией лишь с умеренно пониженным сродством, что означает: известные ридеры могут считывать эту модификацию. Два деацетилирующих фермента — SIRT1 и HDAC8 — по‑разному обрабатывали гидроксиацетил‑лизин: SIRT1 был намного менее эффективен в удалении новой метки, чем стандартного ацетила, тогда как HDAC8 проявлял мало предпочтений. Эти различия указывают на то, что гидроксиацетилирование может тонко изменять длительность существования метки и набор ферментов, которые с ней взаимодействуют, уточняя ландшафт хроматина.
Почему этот кислород‑зависимый переключатель важен
В целом работа выявляет H3K9‑гидроксиацетилирование как ранее нераспознанную метку гистонов, которую продуцирует KDM3A и, вероятно, в некоторых контекстах — её близкий родственник KDM3B. Поскольку сам KDM3A регулируется по уровню кислорода через путь фактора, индуцируемого гипоксией, это создает прямую химическую связь между концентрацией кислорода и состоянием ацетилирования гистонов. Проще говоря, фермент может одновременно удалять репрессивные метильные метки и превращать активирующие ацетил‑метки в слегка отличную кислородсодержащую форму в одном и том же положении гистона, что потенциально перестраивает генетические программы при стрессе, развитии или раке. Открытие расширяет наше представление о возможностях «деметилаз» и открывает пути к изучению похожих гидроксиацетильных меток на других белках и их ролей в здоровье и болезни.
Цитирование: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Ключевые слова: модификация гистонов, эпигенетика, сенсоры кислорода, фермент KDM3A, регуляция генов