Clear Sky Science · pl
KDM3A katalizuje utlenianie acetyl-lizyny do hydroxyacetyl-lizyny na histonie H3K9
Jak komórki dostrajają geny za pomocą drobnych chemicznych przełączników
Każda komórka w twoim ciele nosi tę samą DNA, a mimo to komórki serca, mózgu i skóry zachowują się bardzo różnie. Jednym z powodów jest to, że komórki dekorują białka pakujące DNA, zwane histonami, małymi znacznikami chemicznymi, które działają jak przełączniki włączające lub wyłączające geny. Ten artykuł ujawnia zaskakująco nowy rodzaj przełącznika w kluczowym miejscu histonu i pokazuje, że jest on bezpośrednio regulowany przez tlen, łącząc sposób odczytu genów przez komórki z tym, jak wyczuwają powietrze, którym oddychają.
Nowy wariant dobrze znanego znacznika histonowego
Histony są szpulami, wokół których owinięte jest DNA. Komórki przyłączają grupy chemiczne, takie jak grupy acetylowe czy metylowe, do konkretnych miejsc na histonach, aby poluzować lub zacisnąć DNA, wpływając na to, które geny są aktywne. Słynnym punktem jest lizyna 9 na histonie H3 (H3K9), gdzie acetylacja zazwyczaj promuje aktywność genów, podczas gdy niektóre metylacje wiążą się z uciskiem genów. Enzymy zwane histonowymi acetylotransferazami dodają grupy acetylowe, a deacetylazy je usuwały; inne enzymy dodają lub usuwają grupy metylowe. Do tej pory sądzono, że te zmiany są „redoksowo neutralne” — nie zależą wprost od tlenu. 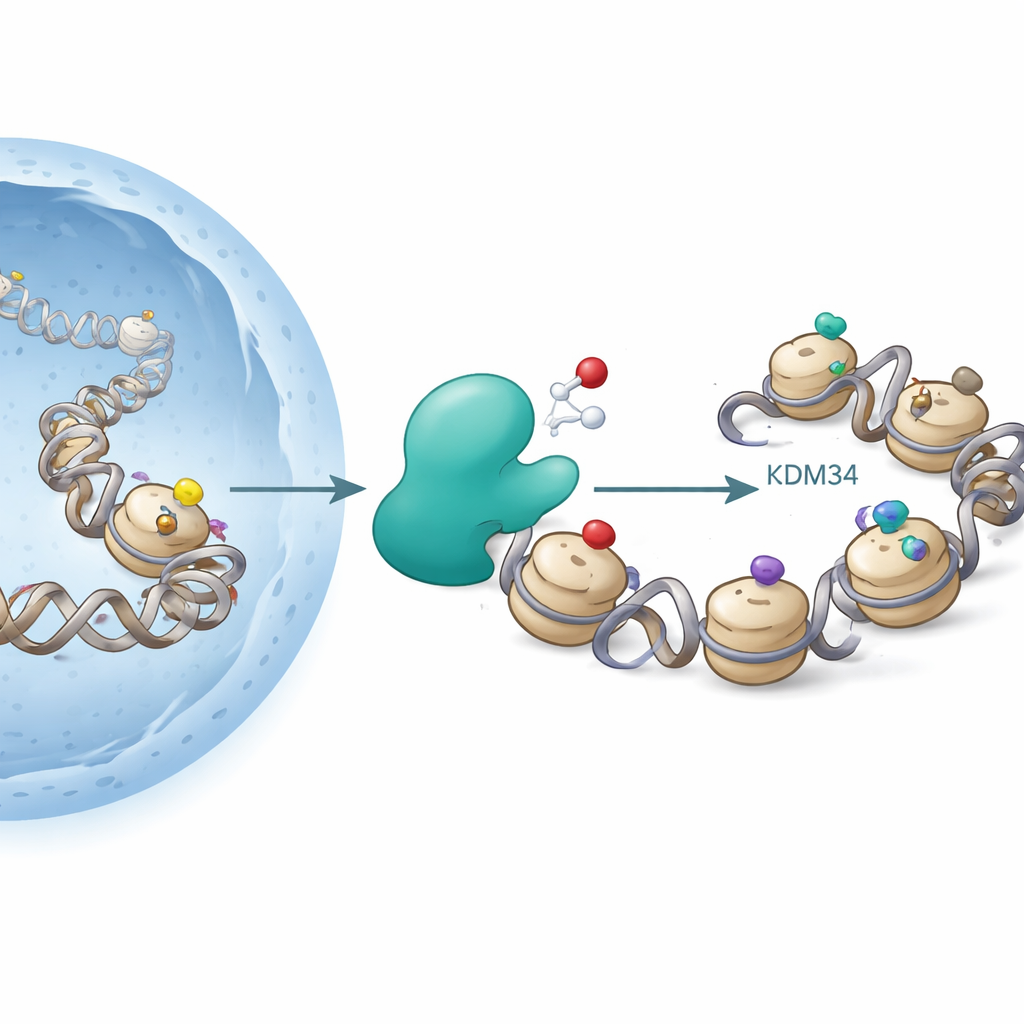
Odkrycie markera powiązanego z tlenem
Autorzy skupili się na KDM3A, enzymie już znanym z usuwania grup metylowych z H3K9. KDM3A należy do rodziny enzymów zależnych od tlenu, które do działania wymagają żelaza i małego kofaktora (2-oksoglutaranu), podobnie jak enzymy wyczuwające niski poziom tlenu (hipoksję) w tkankach. Gdy badacze przesiewali różne zmodyfikowane fragmenty histonów jako potencjalne cele KDM3A, potwierdzili, że KDM3A wydajnie usuwa niektóre metylacje na H3K9. Niespodziewanie stwierdzili także, że oczyszczony KDM3A może utlenić grupę acetylową na H3K9, przekształcając ją w nową formę nazwaną hydroxyacetyl-lizyną. Ta zmiana odpowiada dodaniu atomu tlenu do grupy acetylowej, a dalsze eksperymenty wykazały, że w pewnych warunkach enzym może utleniać jeszcze dalej, sugerując ścieżkę do bardziej egzotycznych reakcji chemicznych.
Udowodnienie istnienia nowego markera w komórkach
Wykrycie nowego produktu chemicznego w probówce to tylko pierwszy krok; zespół musiał także pokazać, że hydroxyacetyl-lizyna występuje na histonach wewnątrz żywych komórek. Wytworzyli przeciwciało specyficzne dla H3K9 niosącego grupę hydroxyacetylową, które nie rozpoznaje standardowej formy acetylowej. Korzystając z tego narzędzia, wykazali, że dodanie oczyszczonego KDM3A do izolowanych histonów zwiększa sygnał dla nowego markera, podczas gdy znane markery metylowe na H3K9 malały, zgodnie z oczekiwaną, podwójną aktywnością KDM3A. Nadekspresja KDM3A w komórkach ludzkich dała podobne efekty: znaczniki metylowe spadły, a sygnał hydroxyacetylowy wzrósł zarówno na histonach ogólnego składu, jak i na poziomie pojedynczych komórek. Spektrometria mas, wysoce czuła technika ważenia cząsteczek, niezależnie potwierdziła obecność precyzyjnego peptydu H3K9 niosącego hydroxyacetyl-lizynę w komórkach, gdy KDM3A jest aktywny.
Gdzie nowy znacznik znajduje się na genomie
Aby zobaczyć, gdzie ten znacznik pojawia się wzdłuż DNA, badacze przeprowadzili ChIP-seq, metodę mapowania w skali genomu. Odkryli, że hydroxyacetylacja H3K9 skupia się wokół miejsc startu genów, szczególnie w genach już wysoko eksprymowanych. Wzor jej występowania ściśle odpowiada klasycznym „aktywnym” znacznikom, takim jak acetylacja H3K9 i trimetylacja H3K4, co sugeruje, że nowy znacznik także należy do zestawu aktywnej chromatyny. Leczenie komórek inhibitorem deacetylaz histonowych, typem leku stosowanym już w terapii nowotworów, zwiększało zarówno standardową acetylację, jak i nowy znak hydroxyacetylowy, prawdopodobnie przez zwiększenie dostępności substratu dla KDM3A i spowolnienie usuwania tych grup acylowych. 
Jak inne białka odczytują i przetwarzają nowy znacznik
Badanie sprawdziło również, jak istniejące „czytniki” chromatyny i enzymy „zmazywacze” reagują na nowy znacznik. Domeny czytające z białka AF9, które normalnie rozpoznają m.in. acetyl i crotonyl, wiązały wersję hydroxyacetylową z jedynie nieznacznie zmniejszonym powinowactwem, co sugeruje, że znane czytniki potrafią wyczuć tę modyfikację. Dwa enzymy deacetylujące, SIRT1 i HDAC8, przetwarzały hydroxyacetyl-lizynę inaczej: SIRT1 był znacznie mniej wydajny w usuwaniu nowego markera niż standardowej grupy acetylowej, podczas gdy HDAC8 praktycznie nie wykazywał preferencji. Te różnice sugerują, że hydroxyacetylacja może subtelnie zmieniać czas trwania znaku i który enzym się nim zajmie, precyzyjnie dostrajając krajobraz chromatyny.
Dlaczego ten zależny od tlenu przełącznik ma znaczenie
Podsumowując, praca ujawnia H3K9 hydroxyacetylację jako wcześniej nierozpoznany znacznik histonowy produkowany przez KDM3A, a prawdopodobnie w niektórych kontekstach także przez jego bliskiego krewniaka KDM3B. Ponieważ KDM3A sam jest aktywowany przez niski poziom tlenu za pośrednictwem szlaku czynnika indukowanego hipoksją, tworzy to bezpośrednie chemiczne połączenie między poziomami tlenu a stanami acetylacji histonów. Mówiąc prościej, enzym może zarówno usuwać represyjne znaki metylowe, jak i przekształcać aktywujące grupy acetylowe w nieco odmienną formę zawierającą tlen w tym samym miejscu histonu, co potencjalnie przekształca programy genowe podczas stresu, rozwoju lub nowotworzenia. Odkrycie poszerza nasze rozumienie tego, co enzymy „demetylujące” potrafią zrobić, i otwiera drogę do badania podobnych hydroxyacetylowych znaczników na innych białkach oraz ich roli w zdrowiu i chorobie.
Cytowanie: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Słowa kluczowe: modyfikacja histonów, epigenetyka, czucie tlenu, enzym KDM3A, regulacja genów