Clear Sky Science · de
KDM3A katalysiert die Oxidation von Acetyl‑Lysin zu Hydroxyacetyl‑Lysin an Histon H3K9
Wie Zellen Gene mit winzigen chemischen Schaltern regulieren
Jede Zelle Ihres Körpers trägt dieselbe DNA, trotzdem verhalten sich Herz-, Hirn‑ und Hautzellen sehr unterschiedlich. Ein Grund dafür ist, dass Zellen ihre DNA‑verpackenden Proteine, die Histone, mit kleinen chemischen Markierungen versehen, die wie Schalter funktionieren und Gene ein‑ oder ausschalten können. Diese Studie zeigt eine überraschende neue Art von Schalter an einer wichtigen Histonstelle und belegt, dass er direkt vom Sauerstoff abhängig ist — sie verbindet damit, wie Zellen ihre Gene lesen, mit der Art, wie sie die Luft, die sie atmen, wahrnehmen.
Eine neue Wendung an einem bekannten Histon‑Marker
Histone sind Spulen, um die die DNA gewickelt ist. Zellen heften chemische Gruppen wie Acetyl‑ oder Methylgruppen an bestimmte Stellen der Histone, um die DNA zu lockern oder zu verdichten und so zu beeinflussen, welche Gene aktiv sind. Ein bekannter Hotspot ist Lysin 9 am Histon H3 (H3K9): Acetylierung fördert meist Genaktivität, während bestimmte Methylmarken mit Genstilllegung einhergehen. Enzyme, die Histonacetyltransferasen genannt werden, fügen Acetylgruppen hinzu, Deacetylasen entfernen sie; andere Enzyme fügen Methylgruppen hinzu oder löschen sie. Bislang gingen Forscher davon aus, dass diese Veränderungen „redox‑neutral“ sind — sie hängen nicht explizit vom Sauerstoff ab. 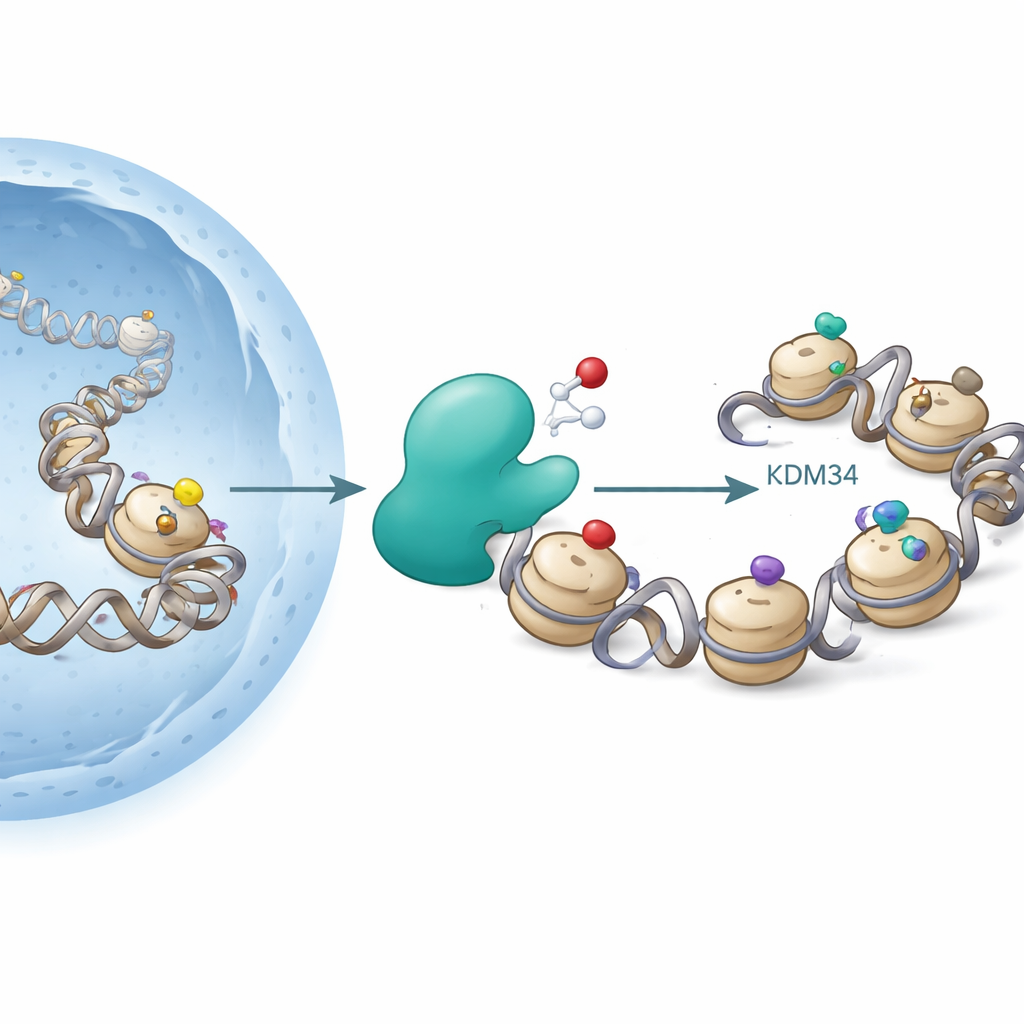
Entdeckung einer sauerstoffgebundenen Histonmarkierung
Die Autor:innen konzentrierten sich auf KDM3A, ein Enzym, das bereits dafür bekannt war, Methylgruppen von H3K9 zu entfernen. KDM3A gehört zu einer Familie sauerstoffabhängiger Enzyme, die Eisen und einen kleinen Cofaktor (2‑Oxoglutarat) benötigen, ähnlich den Enzymen, die niedrigen Sauerstoffspiegel (Hypoxie) in Geweben erkennen. Als die Forschenden verschiedene modifizierte Histonfragmente als mögliche KDM3A‑Ziele untersuchten, bestätigten sie, dass KDM3A bestimmte Methylmarken auf H3K9 effizient entfernte. Unerwartet fanden sie außerdem, dass gereinigtes KDM3A die Acetylgruppe an H3K9 oxidieren kann und sie so in eine neue Form umwandelt, die Hydroxyacetyl‑Lysin genannt wird. Diese Veränderung entspricht der Einfügung eines Sauerstoffatoms in die Acetylgruppe; weitere Experimente zeigten, dass das Enzym unter bestimmten Bedingungen noch weiter oxidieren kann, was auf einen Weg zu noch exotischeren Chemien hindeutet.
Nachweis der neuen Markierung in Zellen
Ein neues chemisches Produkt im Reagenzglas zu finden, ist nur der erste Schritt; das Team musste auch zeigen, dass Hydroxyacetyl‑Lysin auf Histonen in lebenden Zellen vorkommt. Sie erzeugten einen spezifischen Antikörper, der H3K9 mit der Hydroxyacetylgruppe erkennt, aber nicht die Standard‑Acetylform. Mit diesem Werkzeug zeigten sie, dass das Hinzufügen von gereinigtem KDM3A zu isolierten Histonen das Signal für die neue Markierung verstärkte, während bekannte Methylmarken auf H3K9 abnahmen — wie zu erwarten bei der zweifachen Aktivität von KDM3A. Die Überexpression von KDM3A in menschlichen Zellen zeigte ähnliche Effekte: Methylmarken fielen, und das Hydroxyacetylsignal stieg sowohl bei Gesamthistonproben als auch auf Einzelzellebene. Massenspektrometrie, eine sehr empfindliche Technik zum Bestimmen von Molekülmassen, bestätigte unabhängig, dass das präzise H3K9‑Peptid mit Hydroxyacetyl‑Lysin in Zellen vorhanden ist, wenn KDM3A aktiv ist.
Wo die neue Markierung im Genom sitzt
Um zu sehen, wo entlang der DNA diese Markierung vorkommt, führten die Forschenden ChIP‑seq durch, eine genombreite Kartierungsmethode. Sie fanden, dass H3K9‑Hydroxyacetylierung um Genstartstellen herum gehäuft vorkommt, insbesondere bei Genen, die bereits stark exprimiert sind. Das Verteilungsmuster folgt eng dem klassischer „aktiver“ Marker wie H3K9‑Acetylierung und H3K4‑Trimethylierung, was darauf hindeutet, dass die neue Markierung ebenfalls zum Werkzeugkasten aktiver Chromatinzustände gehört. Die Behandlung von Zellen mit einem Histon‑Deacetylase‑Inhibitor, einer Arzneistoffklasse, die bereits in der Krebstherapie eingesetzt wird, erhöhte sowohl die Standard‑Acetylierung als auch die neue Hydroxyacetylmarke — vermutlich durch erhöhte Verfügbarkeit des Substrats für KDM3A und verlangsamten Abbau dieser Acylgruppen. 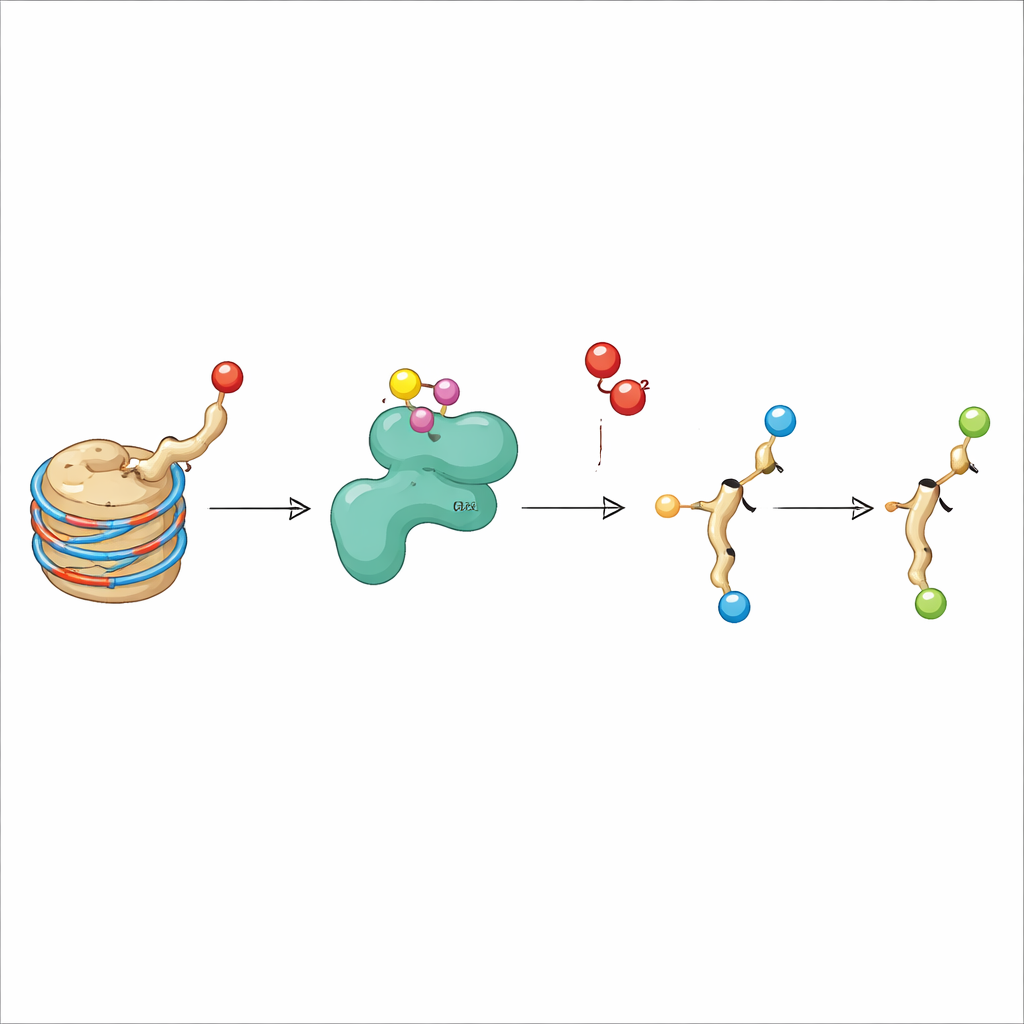
Wie andere Proteine die neue Markierung lesen und verarbeiten
Die Studie prüfte außerdem, wie bestehende Chromatin‑„Reader“ und „Eraser“‑Proteine auf die neuartige Markierung reagieren. Eine Reader‑Domäne des Proteins AF9, die normalerweise Acetyl‑ und Crotonylmarken erkennt, band die Hydroxyacetyl‑Variante mit nur mäßig verminderter Affinität, was nahelegt, dass bekannte Reader diese Modifikation wahrnehmen können. Zwei deacetylierende Enzyme, SIRT1 und HDAC8, verarbeiteten Hydroxyacetyl‑Lysin unterschiedlich: SIRT1 war deutlich weniger effizient beim Entfernen der neuen Markierung als bei der Standard‑Acetylgruppe, während HDAC8 kaum Präferenz zeigte. Diese Unterschiede deuten darauf hin, dass Hydroxyacetylierung die Verweildauer einer Markierung und die Auswahl der beteiligten Enzyme subtil verändern kann und so die Chromatinlandschaft feinjustiert.
Warum dieser sauerstoffabhängige Schalter wichtig ist
Insgesamt deckt die Arbeit H3K9‑Hydroxyacetylierung als bislang unerkannte Histonmarke auf, die von KDM3A und wahrscheinlich in bestimmten Kontexten auch von dem nahen Verwandten KDM3B erzeugt wird. Da KDM3A selbst durch niedrigen Sauerstoff über den hypoxieinduzierbaren Faktorweg aktiviert wird, schafft dies eine direkte chemische Verbindung zwischen Sauerstoffspiegeln und Histonacetylierungszuständen. Einfach ausgedrückt kann das Enzym zugleich repressive Methylmarken entfernen und aktivierende Acetylmarken an derselben Histonstelle in eine leicht andere, sauerstoffhaltige Form umwandeln, was Genprogramme bei Stress, Entwicklung oder Krebs potenziell umgestalten kann. Die Entdeckung erweitert unser Verständnis dessen, was „Demethylase“‑Enzyme leisten können, und öffnet die Tür, ähnliche Hydroxyacetyl‑Marken auf anderen Proteinen sowie deren Rollen in Gesundheit und Krankheit zu erforschen.
Zitation: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Schlüsselwörter: Histonmodifikation, Epigenetik, Sauerstoffwahrnehmung, KDM3A‑Enzym, Genregulation