Clear Sky Science · it
KDM3A catalizza l’ossidazione della acetil-lisina in idrossiacetil-lisina sull’istone H3K9
Come le cellule regolano i geni con piccoli interruttori chimici
Ogni cellula del tuo corpo contiene lo stesso DNA, eppure le cellule del cuore, del cervello e della pelle si comportano in modo molto diverso. Una ragione è che le cellule decorano le proteine che impacchettano il DNA, chiamate istoni, con piccoli segnalini chimici che funzionano come interruttori per accendere o spegnere i geni. Questo articolo rivela un sorprendente nuovo tipo di interruttore su un sito chiave dell’istone e mostra che è controllato direttamente dall’ossigeno, collegando il modo in cui le cellule leggono i loro geni a come percepiscono l’aria che respirano.
Una nuova variazione su un noto segno dell’istone
Gli istoni sono spool attorno ai quali il DNA è avvolto. Le cellule attaccano gruppi chimici come acetil o metil a punti specifici sugli istoni per allentare o stringere il DNA, influenzando quali geni sono attivi. Un punto caldo famoso è la lisina 9 sull’istone H3 (H3K9), dove l’acetilazione tende a promuovere l’attività genica, mentre alcune marche metiliche sono associate al silenziamento genico. Enzimi chiamati istone acetiltransferasi aggiungono gruppi acetilici, e le deacetilasi li rimuovono; altri enzimi aggiungono o cancellano gruppi metilici. Fino ad ora, si pensava che questi cambiamenti fossero “redox-neutral” – non dipendessero esplicitamente dall’ossigeno. 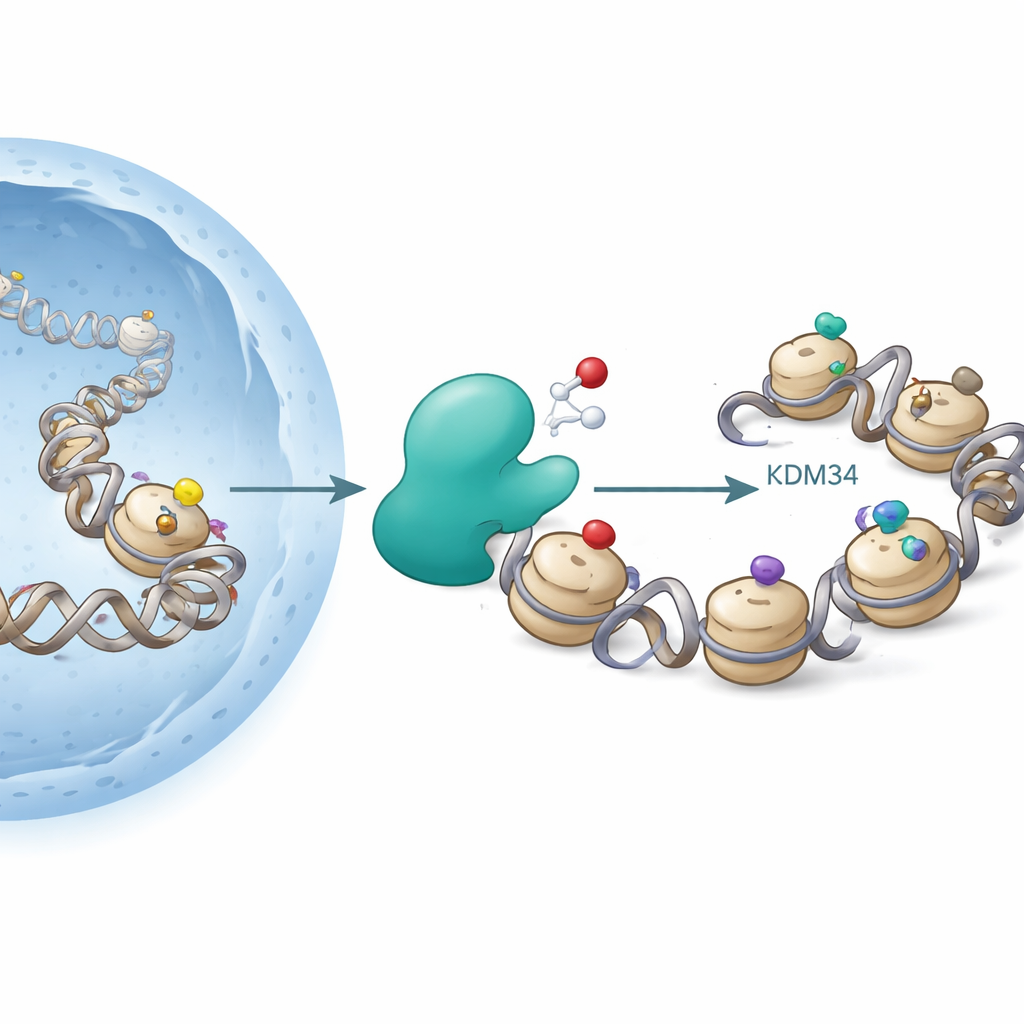
Scoprire una marca degli istoni legata all’ossigeno
Gli autori si sono concentrati su KDM3A, un enzima già noto per rimuovere gruppi metilici da H3K9. KDM3A appartiene a una famiglia di enzimi dipendenti dall’ossigeno che richiedono ferro e un piccolo cofattore (2-ossoglutarato) per funzionare, simili agli enzimi che rilevano la bassa ossigenazione (ipossia) nei nostri tessuti. Quando i ricercatori hanno esaminato vari frammenti di istoni modificati come possibili bersagli di KDM3A, hanno confermato che KDM3A cancella efficacemente certe marche metiliche su H3K9. In modo inaspettato, hanno anche scoperto che la KDM3A purificata può ossidare il gruppo acetilico su H3K9, convertendolo in una nuova forma chiamata idrossiacetil-lisina. Questo cambiamento corrisponde all’aggiunta di un atomo di ossigeno al gruppo acetile, e ulteriori esperimenti hanno mostrato che in alcune condizioni l’enzima può ossidare ancora di più, suggerendo una via verso chimiche più esotiche.
Dimostrare che la nuova marca esiste nelle cellule
Individuare un nuovo prodotto chimico in provetta è solo il primo passo; il team doveva anche dimostrare che l’idrossiacetil-lisina appare sugli istoni all’interno delle cellule vive. Hanno generato un anticorpo dedicato che riconosce H3K9 portatore del gruppo idrossiacetil ma non della forma acetil standard. Usando questo strumento, hanno mostrato che aggiungere KDM3A purificata a istoni isolati aumentava il segnale per la nuova marca, mentre le note marche metiliche su H3K9 diminuivano, come ci si aspetta dalla doppia attività di KDM3A. L’iperespressione di KDM3A in cellule umane ha prodotto effetti simili: le marche metiliche sono diminuite e il segnale di idrossiacetil è aumentato su istoni complessivi e a livello di singola cellula. La spettrometria di massa, una tecnica altamente sensibile per pesare le molecole, ha confermato in modo indipendente che il preciso peptide H3K9 contenente idrossiacetil-lisina è presente nelle cellule quando KDM3A è attivo.
Dove si trova la nuova marca sul genoma
Per vedere dove questa marca compare lungo il DNA, i ricercatori hanno eseguito ChIP-seq, un metodo di mappatura a livello genomico. Hanno trovato che l’idrossiacetilazione di H3K9 si concentra attorno ai siti di inizio dei geni, soprattutto nei geni già fortemente espressi. Il suo profilo segue da vicino quello delle classiche marche “attive” come l’acetilazione di H3K9 e la trimetilazione di H3K4, suggerendo che il nuovo segnalino appartiene anch’esso al kit della cromatina attiva. Il trattamento delle cellule con un inibitore delle deacetilasi degli istoni, un tipo di farmaco già usato in terapia contro il cancro, ha aumentato sia l’acetilazione standard sia la nuova marca idrossiacetil, probabilmente aumentando la disponibilità del substrato per KDM3A e rallentando la rimozione di questi gruppi acilici. 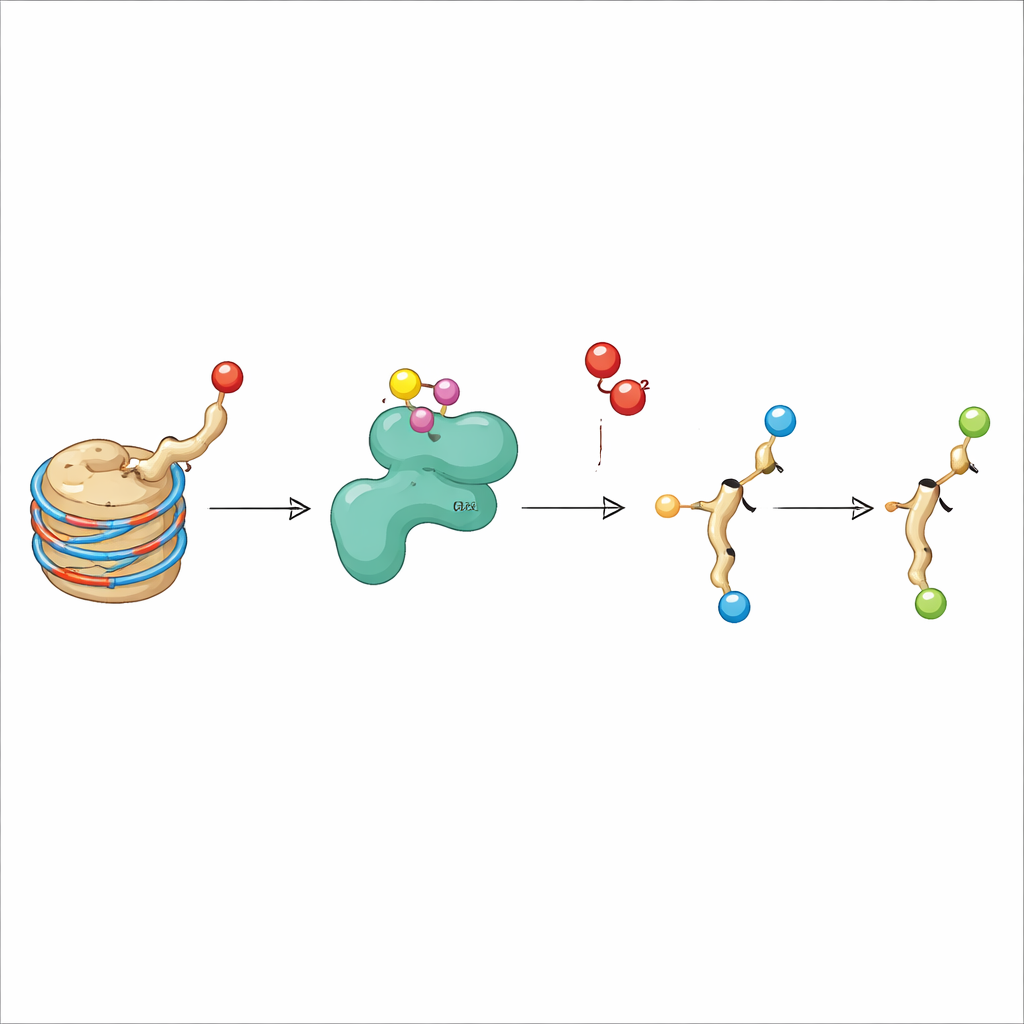
Come altri proteine leggono e processano la nuova marca
Lo studio ha anche testato come i domini “reader” e gli enzimi “eraser” della cromatina conosciuti rispondono alla nuova marca. Un dominio lettore della proteina AF9, che normalmente riconosce marche acetil e crotonil, si è legato alla versione idrossiacetil con un’affinità solo moderatamente ridotta, implicando che i reader noti possono percepire questa modifica. Due enzimi deacetilanti, SIRT1 e HDAC8, hanno processato l’idrossiacetil-lisina in modo diverso: SIRT1 è stato molto meno efficiente nel rimuovere la nuova marca rispetto al gruppo acetilico standard, mentre HDAC8 ha mostrato poca preferenza. Queste differenze suggeriscono che l’idrossiacetilazione può alterare sottilmente la durata di un segno e quali enzimi vi intervengono, modulando finemente il paesaggio della cromatina.
Perché questo interruttore dipendente dall’ossigeno è importante
Nel complesso, il lavoro scopre l’idrossiacetilazione di H3K9 come una marca degli istoni precedentemente non riconosciuta prodotta da KDM3A, e probabilmente in alcuni contesti anche dal suo parente stretto KDM3B. Poiché KDM3A è esso stesso regolato dalla bassa ossigenazione tramite la via del fattore inducibile dall’ipossia, questo crea un legame chimico diretto tra i livelli di ossigeno e gli stati di acetilazione degli istoni. In termini semplici, l’enzima può sia rimuovere marche metiliche repressorie sia convertire marche acetilative in una forma contenente ossigeno sullo stesso sito dell’istone, rimodellando potenzialmente i programmi genici durante stress, sviluppo o cancro. La scoperta amplia la nostra visione di ciò che gli enzimi “demetilasi” possono fare e apre la strada all’esplorazione di simili marche idrossiacetil su altre proteine, così come dei loro ruoli nella salute e nella malattia.
Citazione: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Parole chiave: modificazione degli istoni, epigenetica, rilevamento dell’ossigeno, enzima KDM3A, regolazione genica