Clear Sky Science · ja
KDM3AはヒストンH3K9のアセチルリジンを酸化してヒドロキシアセチルリジンを生成する
細胞が小さな化学スイッチで遺伝子を調節する仕組み
体内のすべての細胞は同じDNAを持っていますが、心臓細胞、脳細胞、皮膚細胞はそれぞれまったく異なる振る舞いをします。その一因は、ヒストンと呼ばれるDNAを包むタンパク質に小さな化学タグが付けられ、遺伝子のオン・オフを切り替えるスイッチのように働くためです。本論文は、重要なヒストン部位に存在する意外な新型のスイッチを明らかにし、それが酸素によって直接制御されることを示して、細胞が遺伝子を読む仕組みと呼吸する空気の感知が結びついていることを示しています。
よく知られたヒストンタグに加わる新たなひねり
ヒストンはDNAが巻き付く糸巻きのような役割を果たします。細胞はヒストンの特定部位にアセチルやメチルなどの化学基を付加してDNAの緩み具合を変え、どの遺伝子が活性化されるかに影響を与えます。よく知られたホットスポットの一つがヒストンH3のリジン9(H3K9)で、アセチル化は遺伝子活性化を促す傾向があり、特定のメチル化は遺伝子サイレンシングと関連します。ヒストンアセチルトランスフェラーゼがアセチル基を付け、脱アセチラーゼがそれを除去し、別の酵素がメチル基を付けたり消したりします。これまでは、これらの変化は「レドックスに中立」つまり明示的に酸素に依存しないと考えられてきました。 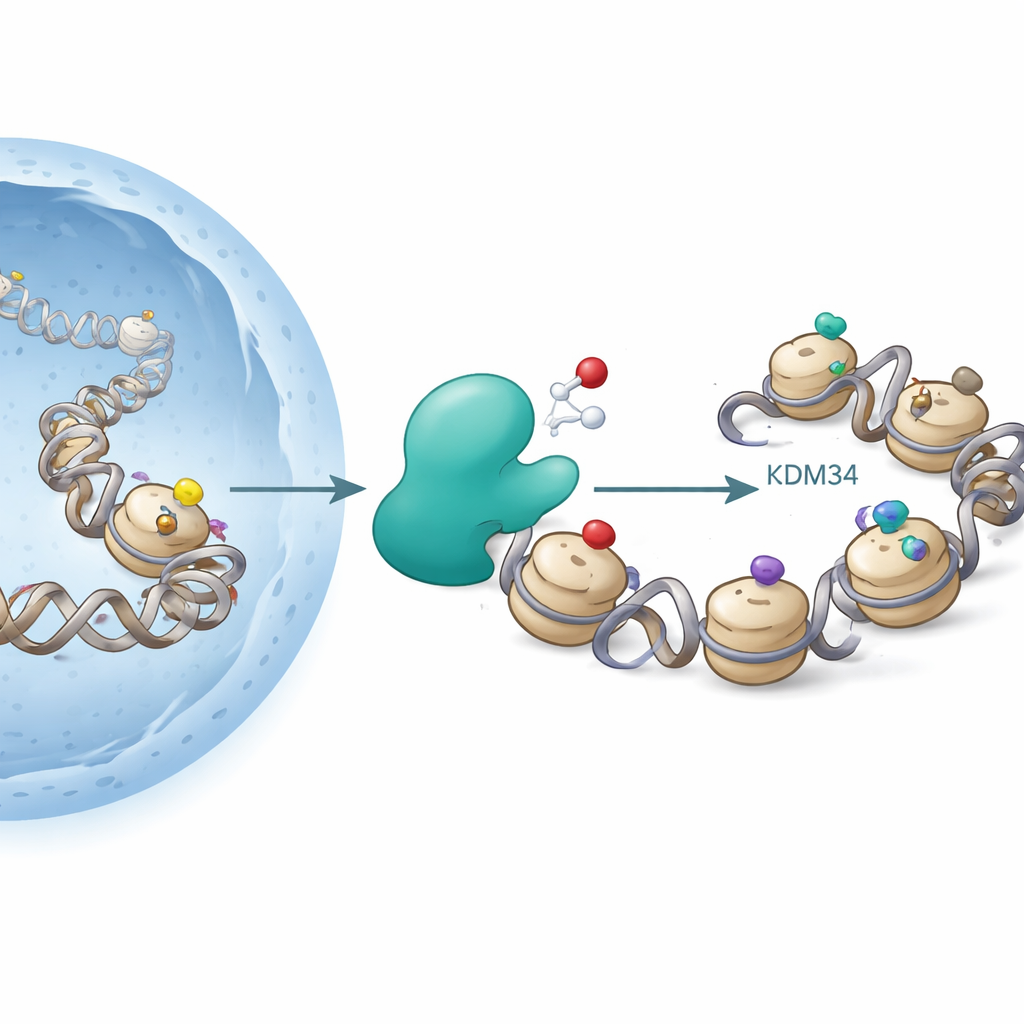
酸素に結びついたヒストンマークの発見
著者らは、もともとH3K9のメチル基を除去することが知られていた酵素KDM3Aに着目しました。KDM3Aは鉄と補酵素(2-オキソグルタル酸)を必要とする酸素依存性酵素のファミリーに属し、組織の低酸素(低酸素状態)を感知する酵素に似ています。研究者たちがKDM3Aの標的となり得る修飾ヒストン断片をスクリーニングしたところ、KDM3AがH3K9の特定のメチルマークを効率的に消去することが確認されました。予期しないことに、精製したKDM3AはH3K9のアセチル基を酸化してヒドロキシアセチル-リジンという新しい形に変換できることも見つかりました。この変化はアセチル基に酸素原子が付加されることに相当し、さらに条件によっては酵素がより一段と酸化を進めることができることが示され、より珍しい化学変化への経路を示唆します。
細胞内で新しいマークが存在することの証明
試験管内で新しい化学生成物を見つけることは第一歩に過ぎません。研究チームはヒドロキシアセチル-リジンが生細胞のヒストン上にも現れることを示す必要がありました。彼らは標準のアセチル体ではなくヒドロキシアセチルを認識する専用抗体を作製しました。このツールを用い、精製KDM3Aを分離ヒストンに加えると新しいマークのシグナルが増加し、同時にKDM3Aの二重活性により予測される通りH3K9の既知のメチルマークは減少することを示しました。ヒト細胞でKDM3Aを過剰発現させても同様の効果が得られ、メチルマークは減少し、バルクヒストンや単一細胞レベルでヒドロキシアセチルのシグナルが上昇しました。質量分析法という分子の質量を高感度に測る手法も独立に、KDM3Aが活性化されているときにH3K9ペプチドがヒドロキシアセチル-リジンを担っていることを確認しました。
ゲノム上で新しいマークがどこに位置するか
このマークがDNA上のどこに現れるかを調べるため、研究者らはChIP-seqという全ゲノムマッピング法を実行しました。H3K9ヒドロキシアセチル化は遺伝子の開始部位の周辺、特に既に高く発現している遺伝子でクラスターを形成することがわかりました。そのパターンは古典的な「活性」マークであるH3K9アセチル化やH3K4三量化と密接に一致し、この新しいタグも活性クロマチンのツールキットに属していることを示唆します。ヒストン脱アセチラーゼ阻害剤という既にがん治療でも用いられる薬で処理すると、標準的なアセチル化と新しいヒドロキシアセチルマークの両方が増加しました。これはおそらくKDM3Aの基質供給が増え、これらのアシル基の除去が遅くなるためです。 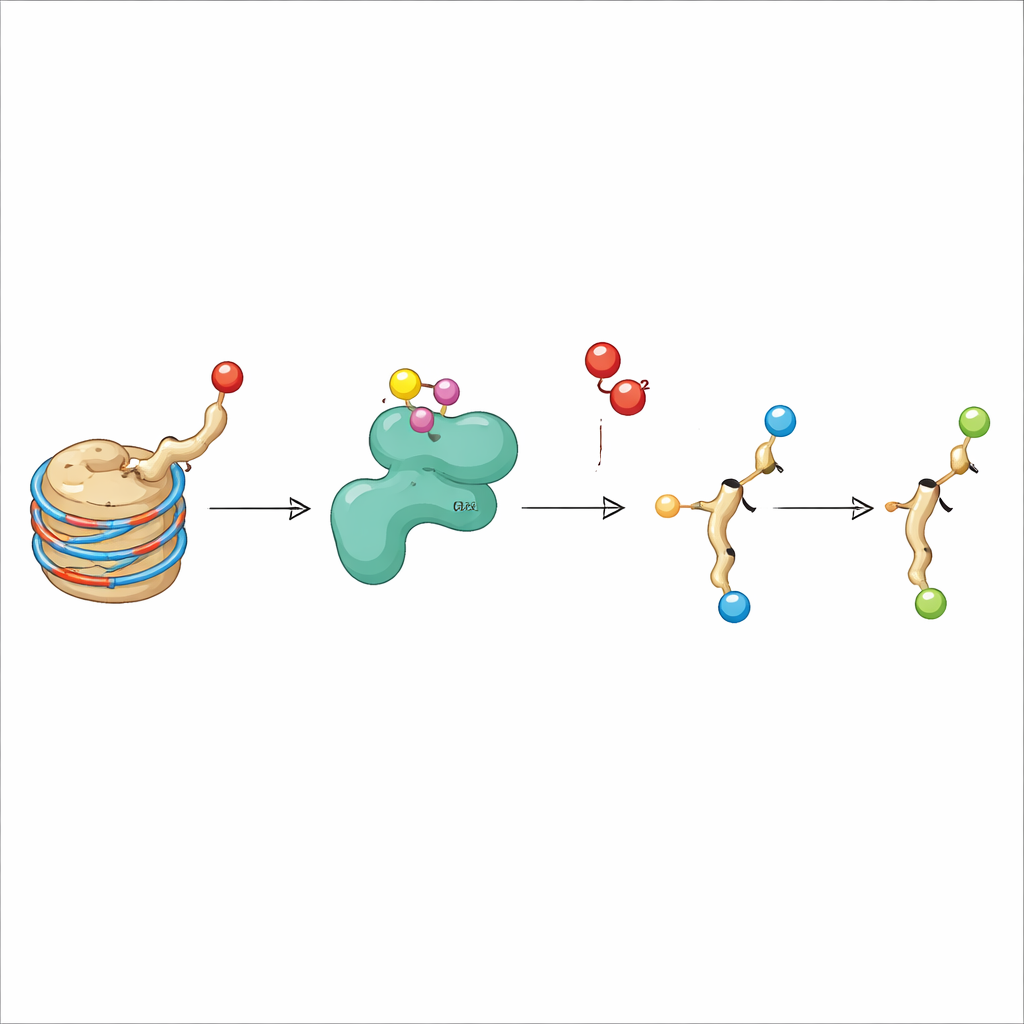
他のタンパク質が新しいタグをどう読むか・処理するか
研究は既存のクロマチン「リーダー」や「イレイザー」タンパク質がこの新規マークにどう反応するかも検討しました。通常アセチルやクレトニル基を認識するAF9タンパク質のリーダードメインは、ヒドロキシアセチル版にもわずかに低下した親和性で結合し、既知のリーダーがこの修飾を感知し得ることを示しました。脱アセチル酵素のうちSIRT1とHDAC8はヒドロキシアセチル-リジンを異なって処理しました。SIRT1は新しいタグを標準的なアセチル基よりも除去する効率が大幅に低く、一方HDAC8はほとんど選好性を示しませんでした。これらの違いは、ヒドロキシアセチル化がマークの持続時間やどの酵素が関与するかを微妙に変え、クロマチンの景観を精密に調節し得ることを示唆します。
この酸素依存的スイッチが重要な理由
総じて、本研究はH3K9ヒドロキシアセチル化をKDM3Aによって生成されるこれまで認識されていなかったヒストンマークとして明らかにし、場合によっては近縁のKDM3Bも関与する可能性を示します。KDM3A自身が低酸素応答因子経路を通じて低酸素で活性化されるため、これにより酸素レベルとヒストンのアセチル化状態の間に直接的な化学的結びつきが生じます。簡単に言えば、この酵素は抑制的なメチルマークを除去すると同時に、活性化的なアセチルマークを同じヒストン部位でわずかに酸素を含む別の形に変換でき、ストレス、発生、がんの際に遺伝子プログラムを再形成する可能性があります。この発見は「デメチラーゼ」酵素ができることの見方を広げ、他のタンパク質上の類似するヒドロキシアセチルマークやそれらの健康・疾患における役割の探索への道を開きます。
引用: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
キーワード: ヒストン修飾, エピジェネティクス, 酸素感知, KDM3A酵素, 遺伝子制御