Clear Sky Science · pt
KDM3A catalisa a oxidação de acetil-lisina a hidroxiacetil-lisina na histona H3K9
Como as células ajustam genes com pequenos interruptores químicos
Cada célula do seu corpo carrega o mesmo DNA, mas células do coração, do cérebro e da pele se comportam de maneiras muito diferentes. Um motivo é que as células decoram as proteínas que empacotam o DNA, chamadas histonas, com pequenas marcas químicas que agem como interruptores para ligar ou desligar genes. Este artigo revela um tipo surpreendente de interruptor em um sítio importante da histona e mostra que ele é controlado diretamente pelo oxigênio, ligando a forma como as células leem seus genes à forma como elas sentem o ar que respiram.
Uma reviravolta num marcador de histona bem conhecido
As histonas são carretéis em torno dos quais o DNA se enrola. As células anexam grupos químicos, como acetil ou metil, a pontos específicos das histonas para afrouxar ou apertar o DNA, influenciando quais genes estão ativos. Um ponto famoso é a lisina 9 na histona H3 (H3K9), onde a acetilação tende a promover a atividade gênica, enquanto certas marcas de metilação se associam ao silenciamento gênico. Enzimas chamadas histona acetiltransferases adicionam grupos acetil, e desacetilases os removem; outras enzimas adicionam ou apagam grupos metil. Até agora, achava-se que essas mudanças eram “redox-neutras” — não dependiam explicitamente do oxigênio. 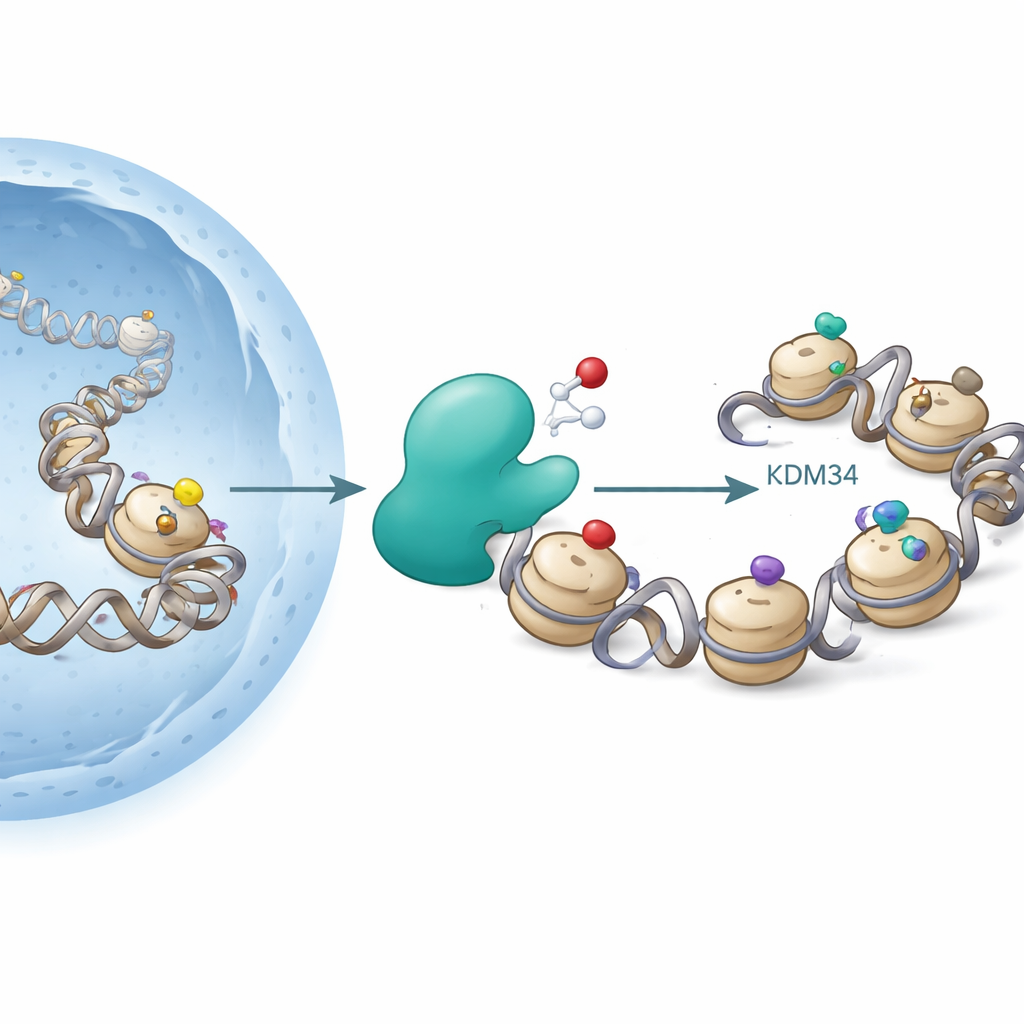
Descobrindo uma marca de histona ligada ao oxigênio
Os autores focaram na KDM3A, uma enzima já conhecida por remover grupos metil da H3K9. A KDM3A pertence a uma família de enzimas dependentes de oxigênio que requerem ferro e um cofator pequeno (2-oxoglutarato) para funcionar, semelhante às enzimas que detectam baixo oxigênio (hipóxia) em nossos tecidos. Quando os pesquisadores testaram vários fragmentos de histona modificados como possíveis alvos da KDM3A, confirmaram que a KDM3A apagava de forma eficiente certas marcas de metil na H3K9. Inesperadamente, também descobriram que a KDM3A purificada podia oxidar o grupo acetil na H3K9, convertendo-o em uma nova forma chamada hidroxiacetil-lisina. Essa mudança corresponde à adição de um átomo de oxigênio ao grupo acetil, e experimentos adicionais mostraram que, sob algumas condições, a enzima pode oxidar ainda mais, sugerindo uma via para químicas mais exóticas.
Provando que a nova marca existe nas células
Encontrar um novo produto químico em um tubo de ensaio é apenas o primeiro passo; a equipe também precisava mostrar que a hidroxiacetil-lisina aparece nas histonas dentro de células vivas. Eles geraram um anticorpo dedicado que reconhece H3K9 carregando o grupo hidroxiacetil, mas não a forma acetil padrão. Usando essa ferramenta, mostraram que adicionar KDM3A purificada a histonas isoladas aumentava o sinal da nova marca, enquanto as marcas de metil conhecidas na H3K9 diminuíam, conforme esperado pela atividade dupla da KDM3A. Superexpressão de KDM3A em células humanas teve efeitos semelhantes: as marcas de metil caíram e o sinal de hidroxiacetil aumentou nas histonas em massa e ao nível de célula única. Espectrometria de massas, uma técnica altamente sensível para pesar moléculas, confirmou de forma independente que o peptídeo preciso H3K9 carregando hidroxiacetil-lisina está presente em células quando a KDM3A está ativa.
Onde a nova marca se localiza no genoma
Para ver onde essa marca aparece ao longo do DNA, os pesquisadores realizaram ChIP-seq, um método de mapeamento em todo o genoma. Eles descobriram que a hidroxiacetilação da H3K9 se concentra ao redor dos sítios de início dos genes, especialmente em genes que já são altamente expressos. Seu padrão acompanha de perto o de marcas clássicas “ativas”, como acetilação de H3K9 e trimetilação de H3K4, sugerindo que a nova etiqueta também pertence ao conjunto de ferramentas da cromatina ativa. Tratar células com um inibidor de histona desacetilase, um tipo de fármaco já utilizado na terapia do câncer, aumentou tanto a acetilação padrão quanto a nova marca hidroxiacetil, provavelmente ao aumentar a disponibilidade de substrato para a KDM3A e retardar a remoção desses grupos acila. 
Como outras proteínas leem e processam a nova marca
O estudo também testou como domínios “leitores” e proteínas “apagadoras” da cromatina existentes respondem à marca inédita. Um domínio leitor da proteína AF9, que normalmente reconhece marcas acetil e crotonil, ligou-se à versão hidroxiacetil com afinidade apenas modestamente reduzida, implicando que leitores conhecidos podem detectar essa modificação. Duas enzimas desacetilantes, SIRT1 e HDAC8, processaram a hidroxiacetil-lisina de maneiras diferentes: a SIRT1 foi muito menos eficiente em remover a nova marca do que o grupo acetil padrão, enquanto a HDAC8 teve pouca preferência. Essas diferenças sugerem que a hidroxiacetilação pode alterar sutilmente quanto tempo uma marca persiste e quais enzimas a interagem, ajustando finamente o cenário da cromatina.
Por que esse interruptor dependente de oxigênio importa
No geral, o trabalho descobre a hidroxiacetilação de H3K9 como uma marca de histona antes não reconhecida produzida pela KDM3A, e provavelmente em alguns contextos por sua parente próxima KDM3B. Porque a própria KDM3A é ativada por baixo oxigênio via a via do fator induzível por hipóxia, isso cria um elo químico direto entre os níveis de oxigênio e os estados de acetilação das histonas. Em termos simples, a enzima pode tanto remover marcas metil repressor as quanto converter marcas acetil ativadoras em uma forma ligeiramente diferente contendo oxigênio no mesmo sítio da histona, potencialmente remodelando programas gênicos durante estresse, desenvolvimento ou câncer. A descoberta amplia nossa visão do que enzimas “desmetilases” podem fazer e abre a porta para explorar marcas hidroxiacetil semelhantes em outras proteínas, bem como seus papéis na saúde e na doença.
Citação: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Palavras-chave: modificação de histona, epigenética, sensoriamento de oxigênio, enzima KDM3A, regulação gênica